
4. 氨基乙酸在水溶液中存在如下平衡:
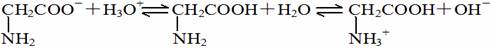
若以Pt为电极,以强酸溶液或以强碱溶液为介质中电解氨基乙酸溶液,均能在电极上析出氨基乙酸,则析出的电极分别为
A.阳极、阴极 B. 阴极、阳极 C. 均在阴极 D. 均在阳极
3.如图所示装置中都盛有0.lmol/L 的NaCl溶液,放置一段时间后装置中的四块相同锌片腐蚀速率由快到慢的正确顺序是( )。
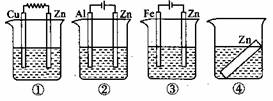 A.③①④②
A.③①④②
B. ①②④③
C. ①②③④
D. ②①④③
2.下列各方法中:①金属表面涂抹油漆②改变金属内部结构③保持金属表面清洁干燥④在金属表面进行电镀⑤使金属表面形成致密的氧化物薄膜,能对金属起到防止或减缓腐蚀作用的是
A. ①②③④ B. ①③④⑤ C. ①②④⑤ D. ①②③④⑤
1.能用电解原理说明的问题是 ( )
① 电解是把电能转变成化学能 ② 电解就是化学物质发生分解反应 ③ 电解质溶液导电是化学变化,金属导电是物理变化 ④ 不能自发进行的氧化还原反应,通过电解的原理可以实现 ⑤ 任何溶液被电解时必然导致氧化还原反应的发生
A.①②③④ B.②③⑤ C. ①③④⑤ D. ③④⑤
15.有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20。其中:X、Z是金属元素;V和Z元素原子的最外层都只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素最外层电子数的一半。试回答下列问题:
(1)由此推知各种元素的元素符号分别是:
V__________;W________;X________;Y________;Z__________。
(2)由这些元素组成的一种结晶水合物R的化学式为________________________,
俗名是______________。在日常生活中可用于____________________________。
(3)实验室用R为原料,制备含X的氢氧化物,其反应的离子方程式为:
____________________________________________________________________。
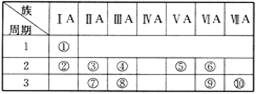
14.下表是元素周期表的一部分。
(1)表中元素⑩的氢化物的化学式
为 ______,此氢化
物的还原性比元素⑨的氢化物
的还原性 ____(填强或弱)。
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是 _,其单质的电子式为 。
(3)俗称为“矾”的一类化合物通常含有共同的元素是 。
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式:
。
又如表中与元素⑦的性质相似的不同族元素是 (填元素符号)
13.某金属若干克,其原子核外共有2mol电子,核内共有1.204×1024个中子;同质量的该金属跟足量稀盐酸反应,有0.2mol电子发生转移,生成6.02×1022个阳离子。
 则:该金属原子的组成符号为__________;摩尔质量为__________;原子核中,中子数有_______个;质子数有_______个。
则:该金属原子的组成符号为__________;摩尔质量为__________;原子核中,中子数有_______个;质子数有_______个。
12.人们常将在同一原子轨道上运动的,自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”。以下有关主族元素原子的“未成对电子”的说法,错误的是:
A.核外电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子”
B.核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子”
C.核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子”
D.核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子”
11.据中学化学教材所附元素周期表判断,下列叙述不正确的是:
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
10.下列各组原子中,彼此化学性质一定相似的是:
A.x原子:1s2 y原子:1s22s2
B.x原子:M层上有两个电子 y原子:N层上有两个电子
C.x原子:2p亚层上有一个未成对电子 y原子:3p亚层上有一个未成对电子
D.x原子:L层上只有一个空轨道 y原子:M层上只有一个空轨道
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com