
5.烯烃通过臭氧化并经锌和水处理得到醛和酮。例如:
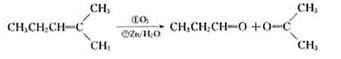
Ⅰ.已知丙醛的燃烧热为1815kJ/mol,丙酮的燃烧为1789 kJ/mol,试写出丙醛燃烧的热化学方程式 。
 Ⅱ.上述反应可用来推断烯烃的结构,一种链状单烯烃A通过臭氧化并经锌和水处理得到B和C。化合物B含碳69.8%,含氢11.6%,B无银镜反应,催化加氢生成D,D在浓硫酸存在下加热,可得到能使溴水褪色且只有一种结构的物质E 反应图示如下:
Ⅱ.上述反应可用来推断烯烃的结构,一种链状单烯烃A通过臭氧化并经锌和水处理得到B和C。化合物B含碳69.8%,含氢11.6%,B无银镜反应,催化加氢生成D,D在浓硫酸存在下加热,可得到能使溴水褪色且只有一种结构的物质E 反应图示如下:
回答下列问题:
(1)B的相对分子质量是 ;C→F的反应类型为 。
D中含有官能团的名称 。
(2)D+F→G的化学方程式是: 。
(3)A的结构简式为 。
(4)化合物A的某种同分异构体通过臭氧化并经锌和水处理得到一种产物,符合该条件的异构体的结构简式有 种。
4.(1)化合物A(C4H10O)。O是一种有机溶剂。A可以发生以下变化:
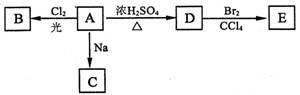
①A分子中的官能团名称是 ;
②A只有一种一氯取代物B。写出由A转化为B的化学方程式
③A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种。F的结构简式是 。
(2)化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与三氯化铁溶液发生显色反应。“HQ”还能发生的反应是(选填序号) 。
①加成反应 ②氧化反应 ③加聚反应 ④水解反应
“HQ”的一硝基取代物只有一种。“HQ”的结构简式是 。
(3)A与“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”。“TBHQ”与氢氧化钠溶液作用得到化学式为C10H12O2Na2的化合物。
“TBHQ”的结构简式是 。
3.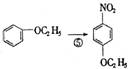 药物菲那西汀的一种合成路线如下:
药物菲那西汀的一种合成路线如下:
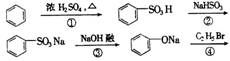
反应②中生成的无机物的化学式是 。
反应③中生成的无机物的化学式是 。
反应⑤的化学方程式是 。
非那西汀水解的化学方程式是 。
2.化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图所示的反应。试写出:

化合物的结构简式:A B
C D
化学方程式: A→E A→F
反应类型: A→E A→F
1.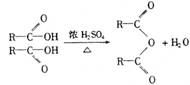 已知两个羧基之间在浓硫酸作用下脱去一分子水生成酸酐,如:
已知两个羧基之间在浓硫酸作用下脱去一分子水生成酸酐,如:
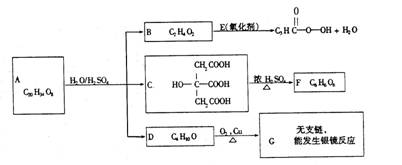 某酯类化合物A是广泛使用的塑料增塑剂。A在酸性条件下能够生成B、C、D。
某酯类化合物A是广泛使用的塑料增塑剂。A在酸性条件下能够生成B、C、D。
(1)CH3COOOH称为过氧乙酸,写出它的一种用途 。
(2)写出B+E→CH3C00H+H2O的化学方程式
(3)写出F可能的结构简式
(4)写出A的结构简式
(5)1摩尔C分别和足量的金属Na、NaOH反应,消耗Na与NaOH物质的量之比是 。
(6)写出D跟氢溴酸(用溴化钠和浓硫酸的混合物)加热反应的化学方程式:
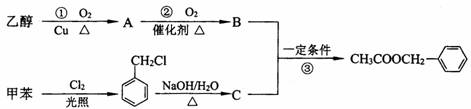
(1)C的结构简式为__________________________。
(2)写出反应①的化学方程式:_______________________________。
(3)反应③的反应类型为______________________________。
(4)反应__________(填序号)原子的理论利用率为100%,符合绿色化学的要求。
2. 原电池的原理
负极----较活泼的金属--- 电子------发生 反应
正极----较不活泼的金属---- 电子----发生 反应
试题枚举
[例1]下列叙述中正确的是
A.构成原电池正极和负极的材料必须是两种金属。
B.由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极。
C.马口铁(镀锡铁)破损时与电解质溶液接触锡先被腐蚀。
D.铜锌原电池工作时,若有13克锌被溶解,电路中就有0.4mol电子通过。
解析: 两种活动性不同的金属与电解质溶液能够组成原电池,但不能因此说构成原电池电极的材料一定都是金属,例如锌和石墨电极也能跟电解质溶液组成原电池。在原电池中,活动金属中的电子流向不活动的电极,因此活动金属是负极。镀锡铁表皮破损后与电解质溶液组成原电池,铁较锡活泼,铁先失电子被腐蚀。铜锌原电池工作时,锌负极失电子,电极反应为Zn –2e==Zn2+,1molZn失去2mol电子,0.2mol锌(质量为13克)被溶解电路中有0.4mol电子通过。故选D。
答案:D
[例2]把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若A、B相连时,A为负极;C、D相连,D上有气泡逸出;A、C相连时A极减轻;B、D相连,B为正极。则四种金属的活泼性顺序由大到小排列为
A.A>B>C>D B.A>C>B>D C.A>C>D>B D.B>D>C>A
解析:金属组成原电池,相对活泼金属失去电子作负极,相对不活泼金属作正极。负极被氧化质量减轻,正极上发生还原反应,有物质析出,由题意得活泼性 A>B、A>C、C>D 、D>B,故正确答案为B。
答案:B
[例3]电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是: Zn + 2 OH- -2e=ZnO + H2O Ag2O +H2O + 2e=2Ag +2 OH-
下列判断正确的是
A.锌为正极,Ag2O为负极。 B.锌为负极,Ag2O为正极。
C.原电池工作时,负极区溶液PH减小。 D.原电池工作时,负极区溶液PH增大。
解析:本题考查原电池和PH的概念。
原电池中失去电子的极为负极,所以锌为负极,Ag2O为正极。B是正确答案。因为 Zn + 2 OH- -2e=ZnO + H2O ,负极区域溶液中[OH-] 不断减少,故PH减小,所以C也正确。故选B、C。
答案:BC
[变式]化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:Cd+2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,
2Ni(OH)2+Cd(OH)2已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,
以下说法中正确的是
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
A.①③ B.②④ C.①④ D.②③
(2).废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值。在酸性土壤中这种污染尤为严重。这是因为
。
(3).另一种常用的电池是锂电池(锂是一种碱金属元素,其相对原子质量为7),由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年。它的负极用金属锂制成,电池总反应可表示为:Li+MnO2→LiMnO2试回答:锂电池比容量特别大的原因是 。锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液?请用化学方程式表示其原因 。
答案:(1)B (2)Ni(OH)2和Cd(OH)2能溶于酸性溶液。
(3)锂的摩尔质量小;2Li+2H2O→2LiOH+H2↑
2.能正确书写原电池的正、负极的电极反应式及电池反应方程式。
知识梳理
1:组成原电池的条件。
① 有两种活性不同的金属(或一种是非金属导体)。
② 电极材料均插入电解质溶液中。
③ 两电极相连形成闭合电路。
1.通过进行化学能转化为电能的探究活动,了解原电池工作原理.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com