
2.在电解饱和食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,不正确的操作顺序是 ( )
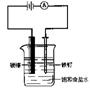 ①过滤 ②加稍过量的NaOH溶液 ③加适量的盐酸
①过滤 ②加稍过量的NaOH溶液 ③加适量的盐酸
④加稍过量的碳酸钠溶液 ⑤加稍过量的氯化钡溶液
A.⑤④②①③ B.④⑤②①③
C.②⑤④①③ D.⑤②④①③
1.海水中含量最多的离子是 ( )
A.钠离子 B.氯离子 C.钙离子 D.镁离子
3、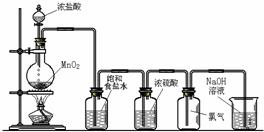 利用上述制Cl2的实验装置图收集到的氯气中常混有杂质气体
和
,为此有人设计右图,在制Cl2时常分别用
除 ___ ,用
利用上述制Cl2的实验装置图收集到的氯气中常混有杂质气体
和
,为此有人设计右图,在制Cl2时常分别用
除 ___ ,用
除 。对比上述实验室制Cl2的装置图,右侧装置图的优点是
。
[当堂训练]
某学生设计如右下实验装置用于制备干燥纯净的氯气,装置中有几处错误,请指出(可不写满)。
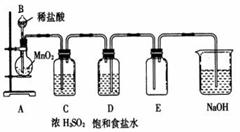 ⑴
;
⑴
;
⑵ ;
⑶ ;
⑷ ;
⑸ ;
⑹ ;
[课堂小结]
[课外练习](选择题每题有1-2个答案)
2、使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
1、如何知道Cl2是否收满?
2、两电极产生的气体体积比为____;电解食盐水除了得到氯气以外,还能得到___________ 。人们把以电解食盐水为基础制取氯气、烧碱(NaOH)等产品的工业称为 ,它是目前化学工业的重要支柱之一。
[知识形成2]学习了工业制氯气的原理,在实验室里氯气可以用 和 在__________条件下反应来制取。实验室制取氯气的化学方程式: 。
根据上述反应原理,人们设计了如下图实验装置,用于实验室制备少量的Cl2 。
 ⑴实验仪器:a:
;b: ;
⑴实验仪器:a:
;b: ;
⑵各部分装置所起作用
A: 装置;B: 装置,利用Cl2密度比空气密度 且 (填 “能”或“不能”)溶于水,难溶于饱和食盐水,可用 排空气法或排饱和食盐水法。C: 装置,因Cl2有毒污染空气,用
吸收多余的氯气。
A B C
[问题解决2]
1、b端为何要通入氢氧化钠溶液?
2、了解氯气的实验室制法;
[调查研究]浩瀚的大海,巨大的宝藏。在众多的自然资源中,海水是十分重要的资源之一,能利用的海水中富含的化学物质如:NaCl、MgCl2、NaBr、NaI等。椐估计:每立方千米的海水中含NaCl 4×107t,查阅有关资料,了解人们是如何从海水中获得氯化钠和使用氯化钠的。并将有关情况与同学们交流讨论。
[新课导入]从海水晒盐得到的食盐,除去杂质后,不仅可以作调料,还可以作为工业原料。19世纪,科学家发明了电解饱和食盐水制取氯气的方法,为工业制氯气奠定了基础。
[知识形成1]
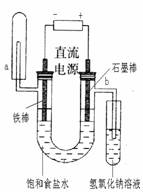 ⑴接通电源,观察两极现象;
⑴接通电源,观察两极现象;
⑵通电一段时间后,用小试管收集U形管左端产生的气体,2min后,提起小试管,并迅速用拇指堵住试管口,移近点燃的酒精灯,松开拇指,检验收集到的气体;
⑶取一只小试管,用向上排空法收集从U形管右端导出的气体,观察收集到气体的颜色;
⑷关闭电源,打开U形管两端的橡皮塞,分别向溶液中滴加1-2滴酚酞溶液,观察现象;
将上述实验中观察到的现象和所得结论填入下表。
|
|
实验现象 |
结论 |
|
⑴ |
|
|
|
⑵ |
|
|
|
⑶ |
|
|
|
⑷ |
|
|
根据实验现象推断,电解饱和食盐水:
①化学方程式:__________________________
②与电源正极相连的电极(阳极)上产生__气;与电源负极相连的电极(阴极)上产生__气。
[问题解决1]
1、了解从海水中获得Cl2的基本原理和方法;
10、(10、29)下列有关种群“J”型增长的叙述,正确的是
A.“J”型增长的种群都有K值 B.“J”型增长的种群生存条件是有限的
C.自然界中绝大多数种群呈“J”型增长 D.“J”型增长的种群个体数一定不断增加
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com