
10.
 ( 9分) 某化学兴趣小组用含铝、铁、铜的合金废料制取纯净的氯化铝溶液、绿矾晶体(FeSO4•7H2O)和胆矾晶体(CuSO4•5H2O),方案如下:
( 9分) 某化学兴趣小组用含铝、铁、铜的合金废料制取纯净的氯化铝溶液、绿矾晶体(FeSO4•7H2O)和胆矾晶体(CuSO4•5H2O),方案如下:

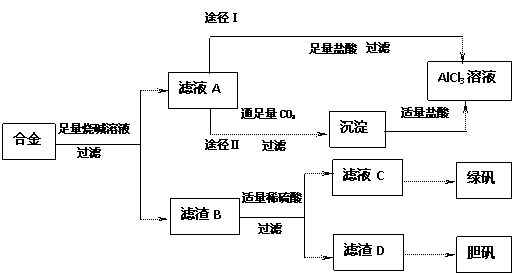









 ⑴该方案中进行了多次过滤、洗涤,过滤时需要用到的玻璃仪器除烧杯外还有
。
⑴该方案中进行了多次过滤、洗涤,过滤时需要用到的玻璃仪器除烧杯外还有
。

 ⑵从滤液C中得到绿矾晶体的操作是 _____
_____ 。
⑵从滤液C中得到绿矾晶体的操作是 _____
_____ 。
 ⑶H2O2是一种应用广泛的绿色氧化剂,往滤渣D中加入稀硫酸和H2O2可以制备胆矾晶体,该反应的总化学方程式为
__
_
。
⑶H2O2是一种应用广泛的绿色氧化剂,往滤渣D中加入稀硫酸和H2O2可以制备胆矾晶体,该反应的总化学方程式为
__
_
。
 ⑷由滤液A通过途径I和途径II都可得到AlCl3溶液,你认为最合理的是 (填“途径I”或“途径II”),理由是
。
⑷由滤液A通过途径I和途径II都可得到AlCl3溶液,你认为最合理的是 (填“途径I”或“途径II”),理由是
。
9. (13分)
(13分)
(1)第4周期 第VIII族 (2分)
2Al+2OH-+2H2O=2AlO2-+3H2↑
(2)①3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g);
△H=-akJ/mol(3分)
②2Fe3++SO2+2H2O=2Fe2++SO42-+4H+(2分)
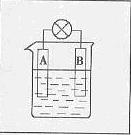
(3)示意图见右 (2分)
(4)b (2分)
9.(13分)A-E五种元素中,除A、B外其他均为短周期元素,它们的性质或原子结构如下表:
|
元素 |
元素性质或原子结构 |
|
A |
 单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160 单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160 |
|
B |
单质为生活中常见的金属,其相对原子质量比A大8 |
|
C |
地壳中含量最多的金属元素 |
|
D |
元素的主族序数是其所在周期序数的3倍 |
|
E |
E的某种原子的原子核内没有中子 |
(1)请写出A在元素周期表中的位置 ;C单质在强碱溶液反应的离子方程式是 。
 (2)①在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和相应的固态化合物时,放出a
kJ热量,此反应的热化学方程式是
。
(2)①在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和相应的固态化合物时,放出a
kJ热量,此反应的热化学方程式是
。
 ②A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是
。
②A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是
。

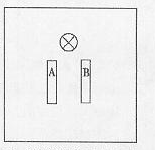 (3)已知化学反应A+2E+=A2++E2能自发进行,若将上述A、
(3)已知化学反应A+2E+=A2++E2能自发进行,若将上述A、
 B两种金属,插入含大量E+的电解质溶液的烧杯中,
B两种金属,插入含大量E+的电解质溶液的烧杯中,
 可组成原电池。
可组成原电池。
 请在右侧方框内相应位置上画出烧杯等,完成原电池电
请在右侧方框内相应位置上画出烧杯等,完成原电池电
 极与用电器连接的示意图。
极与用电器连接的示意图。
 (4)向2mL
0.5mol/L的Acl3溶液中加入3mL 3mol/L KF溶液,
(4)向2mL
0.5mol/L的Acl3溶液中加入3mL 3mol/L KF溶液,
 ACl2溶液褪成无色,再加入KI溶液和CCl4振荡后静置,
ACl2溶液褪成无色,再加入KI溶液和CCl4振荡后静置,
 CCl4层不显色,则下列说法正确的是(已知氧化性
CCl4层不显色,则下列说法正确的是(已知氧化性
 Fe3+>I2)
(填字母)。
Fe3+>I2)
(填字母)。
 a. A3+不与I-发生反应 b.
A3+与F-结合生成不与I-反应的物质
a. A3+不与I-发生反应 b.
A3+与F-结合生成不与I-反应的物质
 c. F-使I-的氧化性减弱 d.
A3+被F-还原为A2+,使溶液中不再存在A3+
c. F-使I-的氧化性减弱 d.
A3+被F-还原为A2+,使溶液中不再存在A3+
8.每个方程式3分,其余每空2分,共14分
(1)离子 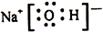 H-O-H
H-O-H
(2)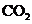
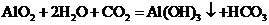 或
或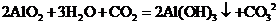
 (3)
(3)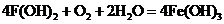
8.(共14分)
已知:A-N为中学化学中常见物质,有如下图所示的转化关系。其中,反应①和②都是重要的工业反应。D为红棕色粉末;H常温下为固体,部分反应物和生成物及反应条件未列出。
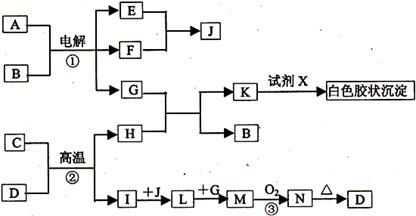
请根据以上信息回答下列问题:
(1)固体H属于_______晶体;G的电子式为_________;B的结构式为________。
(2)实验室实现K→白色胶状沉淀转化最理想的试剂X是_________(填化学式);
其反应的离子方程式是______________________________________________________
(3)反应③的化学方程式是____________________________________________
7.下列离子能大量共存,且加入盐酸有气泡,加入氢氧化钠有白色沉淀的一组是C
 A.
A.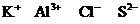 B.
B.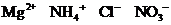
 C.
C.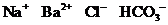 D.
D.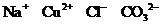
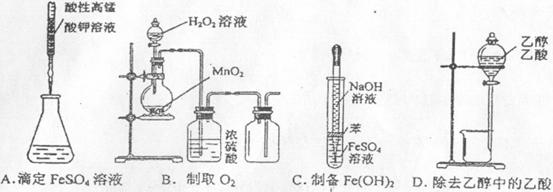
6.下列操作或一起的选用正确的是C

5. 几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( B )
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( B )
|
元素代号 |
A |
B |
D |
E |
G |
X |
Y |
Z |
|
化合价 |
-1 |
-2 |
+4、-4 |
-1 |
+5、-3 |
+3 |
+2 |
+1 |
|
原子半径/nm |
0.071 |
0.074 |
0.077 |
0.099 |
0.110 |
0.143 |
0.160 |
0.186 |
A.A元素的单质能将E单质从XE3的溶液中置换出来

 B.A、X、Z的离子半径由大到小顺序是A->Z+>X3+
B.A、X、Z的离子半径由大到小顺序是A->Z+>X3+
 C.G元素的单质不存在同素异形体
C.G元素的单质不存在同素异形体
 D.Y元素的单在DB2中燃烧生成两种化合物
D.Y元素的单在DB2中燃烧生成两种化合物
4. 某工业生产中有一主要反应CuFeS2 + 4Fe3+
= 5Fe2+ + Cu2+ + 2S。下列说法正确的是( C )
某工业生产中有一主要反应CuFeS2 + 4Fe3+
= 5Fe2+ + Cu2+ + 2S。下列说法正确的是( C )
 A.氧化剂为Fe3+,还原剂为Cu2+和S2-
A.氧化剂为Fe3+,还原剂为Cu2+和S2-
 B.氧化产物是S,还原产物是Fe2+和Cu2+
B.氧化产物是S,还原产物是Fe2+和Cu2+
 C.当转移1mol电子时,有46g CuFeS2参加反应
C.当转移1mol电子时,有46g CuFeS2参加反应
 D.氧化性由强到弱到顺序Fe3+
> Fe2+ > Cu2+
D.氧化性由强到弱到顺序Fe3+
> Fe2+ > Cu2+
3.下列表达式书写正确的是C
 A.
A.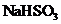 的水溶液显酸性,其原因是
的水溶液显酸性,其原因是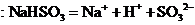
 B.在
B.在 溶液中逐滴滴入
溶液中逐滴滴入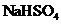 溶液至
溶液至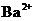 恰好完全沉淀时
恰好完全沉淀时

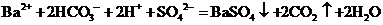
 C.以硫酸为电解质的氢氧燃料电池的正极反映式:
C.以硫酸为电解质的氢氧燃料电池的正极反映式: 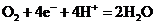
 D.在
D.在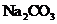 溶液中滴入过量的苯酚水溶液
溶液中滴入过量的苯酚水溶液

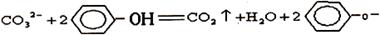
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com