
15.下列叙述正确的是 ( )
A.将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入NaNO3固体,铜粉仍不溶
C.向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO4溶液,沉淀消失
D.纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量CuSO4固体,速率不改变
14.下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比为11:1,则Cl2与KOH反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 ( )
A.1:3 B.4:3 C.2:1 D.3:1
13.下列反应的离子方程式正确的是 ( )
A.向含1mol碘化亚铁的溶液中通入标况下44.8L氯气:
2Fe2++2I-+2Cl2=2Fe3++2I2+4Cl-
B.铝铵矾[NH4Al(SO4)2·12H2O]溶液中加入过量Ba(OH)2溶液:
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
C.H2O2溶液中滴加酸性KMnO4溶液:2 MnO4-+5 H2O2+6H+=2Mn2++5O2↑+8H2O
D.NaHCO3溶液水解的离子方程式为: HCO3-+H2O
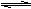 CO32-+H3O+
CO32-+H3O+
12.在标准状况下,将密度为(10/7)g/L CO2和CO混合气体充满一盛有足量Na2O2的密闭容器中(容积为22.4L,固体体积忽略不计),用间断的点火花引发至充分反应,下列对反应完全后容器里残留物的叙述正确的是 ( )
A.有0.15molO2 B.有1molNa2CO3
C.有0. 5moCO D.有0.25molNa2CO3
11.下列各组离子能在指定溶液中大量共存的是 ( )
①酸性溶液中:Fe2+,Al3+,NO3-,I-,S2-
②在pH=11的溶液中:Na+,AlO2-,NO3-,S2-,SO32-
③由水电离的c(H+)=1×10-13mol/L的溶液中:Cl-,HCO3-,NO3-,NH4+,S2O32--
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
⑤使甲基橙变红的溶液中:Fe3+,MnO4-,NO3-,Na+,SO42-
⑥无色溶液中:K+,Cl-,Na+,H2PO4-,PO43-
A.①②⑤ B.①③⑥ C.②④⑤ D.①②④
10.电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1,Y的最外层电子数比K层多l,Z的单质是一种半导体材料,常用于制造太阳能电池,W的原子半径是同周期中最小的。下列推断中正确的是 ( )
A.Z的氢化物的热稳定性强于w的氢化物
B.Z的氧化物与水反应可制得相应的含氧酸
C.X、Y、W的原子半径依次减小,对应的离子半径依次增大
D.X、Y、W的最高价氧化物对应水化物之间互相都能发生反应
9.下列实验能达到预期目的是 ( )
A.从含I-的溶液中提取碘:加入硫酸酸化的H2O2溶液,再用酒精萃取
B.检验溶液中是否一定含有CO32-:滴加稀盐酸,将产生的气体通入澄清石灰水
C.检验蔗糖水解产物是否具有还原性:向水解后的溶液中加入新制Cu(OH)2并加热
D.除去粗盐中的Ca2+、SO42-:依次加入过量BaCl2溶液、Na2CO3溶液,过滤后再加
适量盐酸
8.下列叙述中,正确的是 ( )
A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.晶体中只要有阳离子就会有阴离子
D.电子数相同的阳离子和阴离子一定不具有相同的质子数
7.设NA为阿伏加德罗常数,下列叙述正确的是 ( )
①lmolCH3CH2C(CH3)3所含甲基个数为4NA
②2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA
③1.0L1.0mol/LCH3COOH溶液中,CH3COOH分子数为NA
④8.8g乙酸乙酯中含共用电子对数为1.4NA
⑤标准状况下,22.4L乙醇完全燃烧后生成CO2的分子数为2NA
⑥常温常压下,17g甲基(一14CH3)所含的中子数为9NA
⑦标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA
⑧lmolC15H32分子中含碳碳键数目为14NA
A.①③⑤⑦ B.②③⑥⑧ C.①②④⑧ D.①②⑥⑧
6.磷酸氢二铵[(NH4)2HPO4]可用作复合肥料。关于该物质的下列说法不正确的是( )
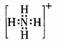 A.HPO42-中含有共价键,其中P的化合价为+5价
A.HPO42-中含有共价键,其中P的化合价为+5价
B.是一种离子化合物,其中铵根离子的电子式为
C.该化合物中所有原子均满足8电子稳定结构
D.其中P元素的质量分数比N元素的质量分数高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com