
12.(2009·芜湖模拟)镁铝合金5.1 g溶于300 mL 2 mol/L的盐酸,在标准状况下放出气体的体积为5.6 L。向反应后的溶液中加入足量氨水,产生沉淀的质量为 ( )
A.5.1 g B.10.2 g
C.13.6 g D.15.3 g
解析:0.6 mol HCl足可以使5.1 g Mg-Al合金完全溶解,共失电子×2=0.5 mol,即5.1 g镁、铝离子正电荷总物质的量为0.5 mol,沉淀时结合OH- 0.5 mol,故沉淀质量为:
11.下列各反应的离子方程式中,错误的是 ( )
A.硫酸铝溶液中加入过量的氨水:
Al3++3NH3·H2O===Al(OH)3↓+3NH
B.铁片放入过量的稀硝酸中:
3Fe+8H++2NO===3Fe2++2NO2↑+4H2O
C.将铝片放入过量NaOH溶液中:
2Al+2OH-+2H2O===2AlO+3H2↑
D.偏铝酸钠与过量盐酸反应:
AlO+4H+===Al3++2H2O
答案:B
10.双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3。关于该物质的说法正确的是 ( )
A.该物质属于两性氢氧化物
B.该物质是Al(OH)3和Na2CO3的混合物
C.1 mol NaAl(OH)2CO3最多可消耗3 mol H+
D.该药剂不适合于胃溃疡患者服用
解析:双羟基铝碳酸钠属于盐类,A错误;它是一种化合物,属于纯净物,不是混合物,B错误;1 mol NaAl(OH)2CO3最多可消耗4 mol H+,C错误;由于能与胃酸反应放出CO2气体,故不适合于胃溃疡患者服用。
答案:D
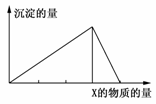
9.将物质X逐渐加入(或通入)Y溶液中,生成沉淀的量与加入X的物质的量关系如图所示,符合图示情况的是 ( )
|
|
A |
B |
C |
D |
|
X |
CO2 |
HCl |
NaOH |
AlCl3 |
|
Y |
Ca(OH)2 |
NaAlO2 |
AlCl3 |
NaOH |
答案:C
8.(2009·平顶山模拟)下列操作所得物质为纯净物的是 ( )
A.将一块带有氧化膜的铝片与过量的浓NaOH溶液完全反应后,取澄清溶液将其蒸干,得纯净的NaAlO2固体
B.向NaAlO2溶液中加入过量的AlCl3溶液,将所得沉淀过滤洗涤,加热灼烧去掉水分,可得纯净的Al(OH)3固体
C.把铝块与适量的稀盐酸完全反应,将所得溶液蒸干,可得AlCl3固体
D.把AlCl3溶液与足量氨水反应,将沉淀过滤、洗涤、灼烧去掉水分可得Al2O3固体
答案:D
7.(2009·潍坊模拟)元素的性质包含金属性和非金属性,其强弱可以通过该元素对应的某些化学性质体现出来。某同学认为铝元素是金属元素,但是有一定的非金属性。下列化学反应中,你认为能支持该同学观点的是 ( )
A.铝片与盐酸反应生成氢气
B.氢氧化铝溶于强碱溶液
C.氢氧化铝溶于强酸溶液
D.铝热反应
答案:B
6.下列有关叙述正确的是 ( )
A.铝和铁在常温下遇硫酸或硝酸发生钝化现象
B.金属钠除保存在煤油中,也可以保存在汽油中
C.湿法冶炼就是指金属在溶液中的置换反应,如金属钠置换硫酸铜溶液中的铜
D.涂油层、电镀金属层、制合金等都是保护金属的措施
答案:D
5.用稀硫酸、NaOH溶液、Al为原料制取Al(OH)3,甲、乙、丙3个学生分别用3种不同途径:
甲:AlAl2(SO4)3Al(OH)3
乙:AlNaAlO2Al(OH)3
Al(OH)3
制得等量Al(OH)3,下列结论正确的是 ( )
A.甲用原料最少 B.乙用原料最少
C.丙用原料最少 D.三人用原料的量相同
解析:例如制取1 mol的Al(OH)3,甲用mol的H2SO4和3 mol的NaOH;乙用1 mol的NaOH和 mol的H2SO4;丙用 mol的H2SO4和 mol的NaOH。
答案:C
4.用下列装置不能达到有关实验目的的是 ( )
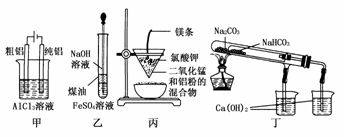
A.用甲图装置电解精炼铝
B.用乙图装置制备Fe(OH)2
C.用丙图装置可制得金属锰
D.用丁图装置验证NaHCO3和Na2CO3的热稳定性
解析:甲中实际发生反应为:阳极:2Al-6e-===2Al3+;阴极:6H++6e- ===3H2↑;电池总反应为2Al+6H2O2Al(OH)3↓+3H2↑。
===3H2↑;电池总反应为2Al+6H2O2Al(OH)3↓+3H2↑。
答案:A
3.(2005·北京理综)将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是( )
A.Mg、AlCl3、NaAlO2
B.KNO3、NaCl、CH3COONa
C.NaClO、Na2SO3、BaCl2
D.Ba(NO3)2、FeSO4、NH4HCO3
解析:B项中只发生反应CH3COO-+H+CH3COOH。
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com