
27.⑴探究氯气具有漂白性的条件(其它合理描述也可) (2分)
⑵吸收气体A中的水 (2分)
⑶干燥的布条不褪色,湿润的布条褪色 (2分) ⑷尾气处理 (2分)
26.⑴5.3g (2分) ⑵容量瓶(250mL)、 (2分) 胶头滴管 (2分)
⑶5.6L、 (2分) 2 mol·L-1 (2分)
25.⑴Fe(OH)3 (2分) Cl2 (2分)
⑵2Na +2H2O =2NaOH + H2 ↑ (2分)
⑶2Fe2+ + Cl2 = 2Fe3+ +2 Cl- (2分)
24.⑴平面形 (2分)
⑵CH2=CH2+H2O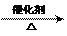 CH3CH2OH (2分)
CH3CH2OH (2分)
⑶CH3CH2OH+CH3COOH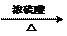 CH3COOC2H5+H2O
(2分)
CH3COOC2H5+H2O
(2分)
23.⑴2Al+Cr2O3=2Cr + Al2O3 (2分) ⑵3Si +2V2O5=4V+3SiO2 (2分)
⑶使之与生成的SiO2结合生成CaSiO3,使反应更易进行 (2分)
22.⑴Zn+Cu2+=Zn2++Cu,构成Zn(-)盐酸Cu(+)原电池,使产生H2速率加快; (2分)
⑵CH3COO-+H+=CH3COOH,降低c(H+),使产生H2速率减慢。 (2分)
21.⑴④⑧⑩ (2分) ⑵①③⑤⑧ (2分) ⑶④⑨ (2分)
|
题目 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
答案 |
|
|
|
|
|
|
|
|
|
|
|
题目 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
答案 |
|
|
|
|
|
|
|
|
|
|
(1)6MnO4-+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O (2分) 6(1分)
(2)设Cu2S、CuS的物质的量分别为x、y
与Cu2S、CuS反应后剩余KMnO4的物质的量:
10×0.1 mol/L×0.035 L×1/5 = 0.007 mol
160x + 96y = 2
8x/5 + 6y/5 = 0.4×0.075 – 0.007 (1分)
解之:y = 0.0125 mol (1分)
CuS的质量分数:(0.0125 mol ×96 g/mol)÷2 g ×100%(1分)
= 60% (1分)
28.2gCu2S和CuS的混合物在酸性溶液中用400mL0.075mol/LKMnO4溶液处理,反应均生成Cu2+、Mn2+、SO2和H2O,其中Cu2S与酸性KMnO4溶液反应的离子方程式为:8MnO4-- + 5Cu2S + 44H+=== 10Cu2+ + 5SO2 + 8Mn2+ + 22H2O
反应后煮沸溶液,赶尽SO2,取出剩余溶液的十分之一,与0.1mol/L(NH4)2Fe(SO4)2溶液反应,恰好消耗35.00mL,反应的离子方程式为:
MnO4-- + 5Fe2+ + 8H+ === Mn2+ + 5Fe3+ + 4H2O
⑴写出该条件下CuS与酸性KMnO4溶液反应的离子方程式: ;在此反应中,若生成22.4LSO2(标准状况),则反应中转移的电子为 mol。
⑵求混合物中CuS的质量分数。
2009年长沙市高中化学竞赛
|
27.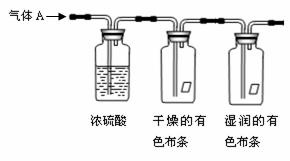 某同学用如下所示装置探究物质的性质。其中气体A的主要成分是氯气,还含有少量水蒸气。请回答下列问题:
某同学用如下所示装置探究物质的性质。其中气体A的主要成分是氯气,还含有少量水蒸气。请回答下列问题:
⑴该实验探究的主要目的是 。
⑵浓硫酸的作用是 。
⑶观察到的实验现象是
⑷从物质性质方面来看,这样的实验设计还
存在事故隐患,因此还需增加 装置。
⑴探究氯气具有漂白性的条件(其它合理描述也可)(2分)
⑵吸收气体A中的水(2分)
⑶干燥的布条不褪色,湿润的布条褪色(2分) ⑷尾气处理(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com