
4.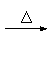 (广东省梅州市曾宪梓中学2009届高三11月月考 )(10分)分子式为C13H16O2的惕各酸苯乙酯广泛用于香精的调香剂。已知:
(广东省梅州市曾宪梓中学2009届高三11月月考 )(10分)分子式为C13H16O2的惕各酸苯乙酯广泛用于香精的调香剂。已知:
① R-CH2Cl + NaOH R-CH2OH + NaCl
②
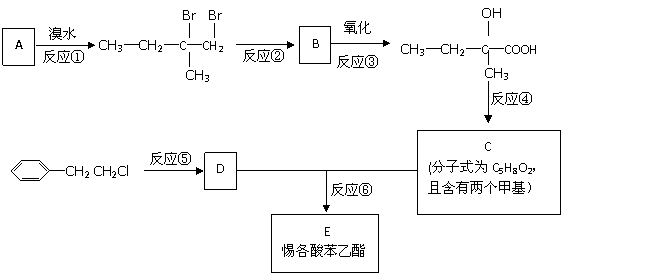 为了合成该物,某实验室的科技人员设计了下列合成路线:
为了合成该物,某实验室的科技人员设计了下列合成路线:
试回答下列问题:
(1)试写出:A的名称_______________;E的结构简式__________。
(2)反应④的一般条件是______________。
(3)上述合成路线中属于取代反应的是 (填编号)。
(4)反应①的化学方程式为 。
答案(1)2-甲基-1-丁烯 (2分)
(2分)
(2)浓H2SO4/△ (1分)
(3)② ⑤ ⑥ (3分,多选、错选不得分)
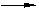 (4)CH3CH2C(CH3)=CH2
+ Br2
CH3CH2C(CH3)BrCH2Br
(2分)
(4)CH3CH2C(CH3)=CH2
+ Br2
CH3CH2C(CH3)BrCH2Br
(2分)
5 (广东省六校2009届高三第二次联考试卷)(10分)肉桂酸甲酯(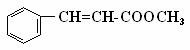 )常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
(1)肉桂酸甲酯的分子式是 ;
 (2)有关肉桂酸甲酯的叙述中,正确的是 (填标号);
(2)有关肉桂酸甲酯的叙述中,正确的是 (填标号);
A.能与溴的四氯化碳溶液发生加成反应 B.无法使酸性高锰酸钾溶液褪色
 C.在碱性条件下能发生水解反应 D.不可能发生加聚反应
C.在碱性条件下能发生水解反应 D.不可能发生加聚反应
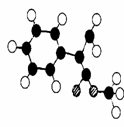
(3)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如
右图所示(图中球与球之间连线表示单键或双键)。G的
结构简式为 ;
(4)用芳香烃A为原料合成G的路线如下:
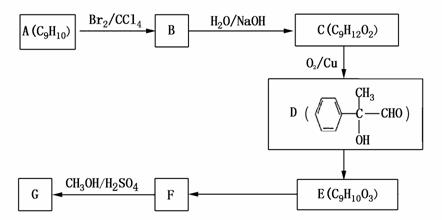
① 化合物E中的官能团有 (填名称)。
② F→G的反应类型是 ,该反应的化学方程式为 。
③ 写出符合下列条件的F的同分异构体的结构简式 。
ⅰ.分子内含苯环,且苯环上只有一个支链;
ⅱ.一定条件下,1mol该物质与足量银氨溶液充分反应,生成4mol银单质。
答案(1)C10H10O2 (2)A、C (3)
(4)①羧基、羟基 ②酯化反应“或取代反应”,

③ 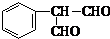
3. (广东省佛山市禅城实验高中2009届高三第二次月考)(10分)由丙烯经下列反应可得到F、G两种高分子化合物,它们都是常用的塑料。
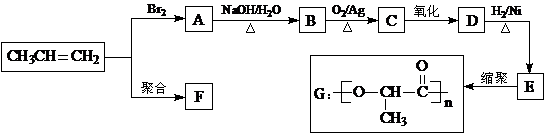
(1)聚合物F的结构简式是_____________________________________。
(2)D的结构简式是___________________________________________。
(3)B转化为C的化学方程式是__________________________________________________。
(4)在一定条件下,两分子E能脱去两分子水形成一种六元环化合物,该化合物的结构简式是_________________________________________。
(5)E有多种同分异构体,其中一种能发生银镜反应,1mol该种同分异构体与足量的金属钠反应产生1mol H2,则该种同分异构体为_____________________________________。
答案。(1)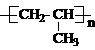 (2)
(2)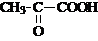
 (3)
(3)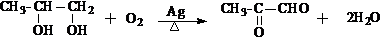
(4)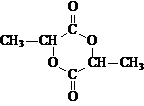 (5)
(5)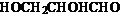
1、(广东广州花都区2009届高三期初调研试题化学卷)(10分)请根据下图作答:
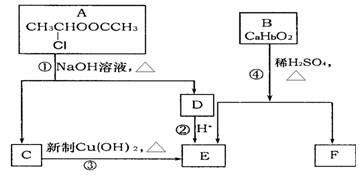
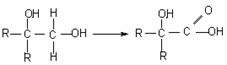
已知:一个碳原子上连有两个羟基时,易发生下列转化:
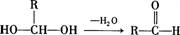
(1)E中含有的官能团是 。
(2)反应③的化学方 。
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1,则B的分子式为 。
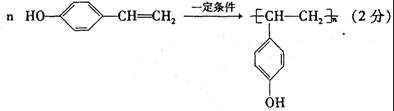
(4)F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有多种结构,写出其中一种的结构简式 。
答案(1) 羧基 (2分)
(2)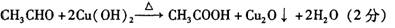
(3)C10H10O2 (2分)
(4)
(5)
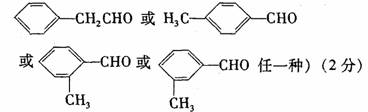
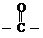 2.(广东省汕头金山中学2009届高三化学期中考试)(10分)已知:①卤代烃在一定条件下可以和金属反应,生成烃基金属有机化合物,该有机
2.(广东省汕头金山中学2009届高三化学期中考试)(10分)已知:①卤代烃在一定条件下可以和金属反应,生成烃基金属有机化合物,该有机
化合物又
|
|
|
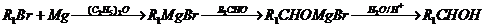
(-R1、、-R2表示烃基)
②有机酸和PCl3反应可以得到羧酸的衍生物酰卤: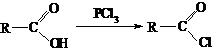
③苯在AlCl3催化下能与酰卤作用生成含羰基的化合物:

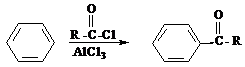
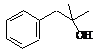
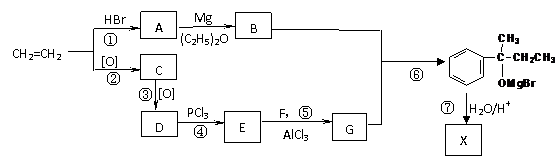 科学研究发现,有机物X、Y在医学、化工等方面具有重要的作用,其分子式均为C10H14O,都能与钠反应放出氢气,并均可经上述反应合成,但X、Y又不能从羰基化合物直接加氢还原得到。X与浓硫酸加热可得到M和M',而Y与浓硫酸加热得到N和N'。M、N分子中含有两个甲基,而M'和N'分子中含有一个甲基。下列是以最基础的石油产品(乙烯、丙烯、丙烷、苯等)及无机试剂为原料合成X的路线:
科学研究发现,有机物X、Y在医学、化工等方面具有重要的作用,其分子式均为C10H14O,都能与钠反应放出氢气,并均可经上述反应合成,但X、Y又不能从羰基化合物直接加氢还原得到。X与浓硫酸加热可得到M和M',而Y与浓硫酸加热得到N和N'。M、N分子中含有两个甲基,而M'和N'分子中含有一个甲基。下列是以最基础的石油产品(乙烯、丙烯、丙烷、苯等)及无机试剂为原料合成X的路线:
其中C溶液能发生银镜发应。请回答下列问题:
(1)上述反应中属于加成反应的是____________________(填写序号)
(2)写出C、Y的结构简式:C_________ _____ Y ______________
(3)写出X与浓硫酸加热得到M的化学反应方程式为__________________ ______________
过程⑤中物质E+F→G的化学反应方程式为______________________ _________________
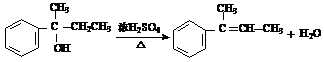
 答案(1)①⑥(共2分,写对1个给1分,错1个扣1分,扣完为止)
答案(1)①⑥(共2分,写对1个给1分,错1个扣1分,扣完为止)
(2)C:CH3CHO Y: (3)
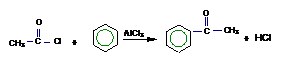
(三)卤素单质的化学性质(相似性及递变性)
由于最外层均为 个电子,极易 电子,因此碱金属都是 剂,但随着电子层数递增,原子半径渐 ,核对最外外层电子的引力渐 ,失电子能力渐 ,其还原性逐渐 。
试题枚举
[例1]:把小块金属钠分别投入饱和NaCl溶液、NH4Cl溶液、FeCl3的烧杯里的现象和反应?
|
|
现象 |
化学方程式 |
|
饱和NaCl |
|
|
|
饱和NH4Cl |
|
|
|
FeCl3溶液 |
|
|
(二)单质的物理性质
随碱金属元素核电荷数增加,原子结构的递变而使碱金属单质的物理性质呈规律性变化.
归纳:从Li →Cs
1.除 外,颜色都是 且都较 ,密度都比较 ,且呈 趋势, 熔趋势沸点逐渐(原因是 。)
2.焰色反应
钠的焰色是 ,钾的焰色是
(一)碱金属元素的原子结构
共同点:原子的最外层均为 个电子,都易 1个电子而表现 性;
不同点:核电荷数逐渐 ;电子层数逐渐 ;原子半径依次 ,得电子能力逐渐 ;单质还原性逐渐 。
3.Na2CO3与NaHCO3比较与鉴别
(1)Na2CO3与NaHCO3比较
|
名 称 |
碳酸钠 |
碳酸氢钠 |
|
|
俗 名 |
|
|
|
|
主要性质 |
色态 |
|
|
|
水溶性 |
|
|
|
|
稳定性 |
|
|
|
|
与H+反应 |
|
|
|
|
与碱NaOH和Ca(OH)2反应 |
|
|
|
|
主要用途 |
|
|
|
|
相互转化 |
|
|
思考:Na2CO3溶液与盐酸作用时,滴加顺序不同,现象一样吗?
(2)根据上叙性质用多种方法区别Na2CO3与NaHCO3
2.氢氧化钠(俗称: 、 、 )
(1)电子式: ,所含化学键为 、
(2)物理性质:有很强的 性,易 (用作 剂),溶于水时会 。
(3)化学性质:具有 碱性。
(4)制法(工业制法):
(5)保存:溶液 ; 固体 。
1.11、氧化钠和过氧化钠的比较
|
|
氧化钠 |
过氧化钠 |
|
化学式 |
|
|
|
氧元素的化合价 |
|
|
|
电子式 |
|
|
|
阴阳离子个数比 |
|
|
|
化合物类型 |
|
|
|
颜色状态 |
|
|
|
与H2O反应的方程式 |
|
|
|
与CO2反应的方程式 |
|
|
|
用途 |
|
|
2.钠的化学性质
Na - e- → Na+ 化学反应中表现为 性
(1)与非金属单质的反应(写出下列方程式)
a.与氯气反应:
b.与硫反应 :
c.与氧气反应①常温下,现象: 化学方程式:
②加热时,现象: 化学方程式:
(2)与水的反应、与醇、酚、羧酸等含-OH的有机物反应。
a.与水反应现象:
化学方程式:
思考:钠与水反应的现象说明钠具有哪些性质?
b.与乙醇反应 现象:
化学方程式: 。
c.与乙酸反应 : 。
(3)与稀酸溶液的反应
与盐酸反应 。
(4)与某些盐的反应
a.与熔融盐 Na+TiCl4 。
b.与盐溶液 (CuSO4溶液) 。
思考:钠在空气中放置一段时间,将发生哪些变化?最终产物是什么?如何保存?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com