
15£Æ»°50.0mL Na2CO3∫ÕNa2SO4µƒªÏ∫œ»Ð“∫£¨º”»Îπ˝¡øµƒBaCl2»Ð“∫∫Û£¨µ√µΩ≥¡µÌ14.51g£¨Ω´≥¡µÌ”√π˝¡øœ°HNO3¥¶¿Ì∫Û£¨≥¡µÌ÷ ¡øºı…ŸµΩ4.66g£¨≤¢”–∆¯ÃÂ∑≈≥ˆ°£
‘º∆À„£∫
(1)‘≠»Ð“∫÷–Na2CO3∫ÕNa2SO4µƒŒÔ÷ µƒ¡ø≈®∂»°£
(2)≤˙…˙∆¯ÃµƒÃª˝(±Í◊º◊¥øˆ)°£
14£Æ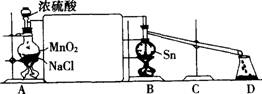 µ—È “”√∏…‘Ô°¢¥ø檵ƒCl2”λ€»⁄µƒSn∑¥”¶÷∆SnCl4£∫Sn+2Cl2
µ—È “”√∏…‘Ô°¢¥ø檵ƒCl2”λ€»⁄µƒSn∑¥”¶÷∆SnCl4£∫Sn+2Cl2 SnCl4Õ¨ ±∑≈¥Û¡øµƒ»»£¨“—÷™SnCl4≥£Œ¬œ¬ «ŒÞ…´“∫ã¨∑–µ„£∫114°Ê£¨”ˆ≥± ™ø’∆¯±„∑¢…˙ÀÆΩ‚∑¥”¶(SnCl4+2H2O
== SnO2+4HCl)≤˙…˙∞◊…´—Ḭ̀£Snµƒ»€µ„£∫231°Ê£¨œ¬Õº «÷∆»°SnCl4µƒ µ—È◊∞÷√°£ ‘ªÿ¥“‘œ¬Œ £∫
SnCl4Õ¨ ±∑≈¥Û¡øµƒ»»£¨“—÷™SnCl4≥£Œ¬œ¬ «ŒÞ…´“∫ã¨∑–µ„£∫114°Ê£¨”ˆ≥± ™ø’∆¯±„∑¢…˙ÀÆΩ‚∑¥”¶(SnCl4+2H2O
== SnO2+4HCl)≤˙…˙∞◊…´—Ḭ̀£Snµƒ»€µ„£∫231°Ê£¨œ¬Õº «÷∆»°SnCl4µƒ µ—È◊∞÷√°£ ‘ªÿ¥“‘œ¬Œ £∫
(1)◊∞÷√A÷–µƒ∑¥”¶‘≠¿Ìø…“‘»œŒ™ «MnO2Ω´≈®H2SO4 ”Î ≥—Œ∑¥”¶≤˙…˙µƒHCl—ıªØ≥…Cl2£¨≤˙…˙µƒ¡Ω÷÷—Œ «NaHSO4°¢MnSO4°£◊∞÷√A÷–∑¥”¶µƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(2)Œ™ π µ—È≥…𶣨A∫ÕBº‰–Ë“™º” µ±µƒ◊∞÷√£¨«ÎΩ´À¸ª≠‘⁄øÚƒ⁄£¨≤¢◊¢√˜∆‰÷– ¢∑≈µƒ“©∆∑°£
(3)Ω¯–– µ—È ±£¨”¶œ»µ„»º(ÃÓ–¥◊÷ƒ∏£¨œ¬Õ¨)°°°° °° ¥¶µƒæ∆æ´µ∆£¨µ±∑¥”¶…˙≥…SnCl4 ±£¨”¶œ®√ °° ¥¶µƒæ∆æ´µ∆£¨¿Ì”… «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(4)◊∞÷√Cµƒ◊˜”√ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(5)Ω¯––¥À µ—È£¨D◊∞÷√∫Û”¶µ±¡¨Ω”µƒ◊∞÷√º∞◊˜”√ «(∞¥¥”◊ÛµΩ”“µƒÀ≥–Ú–¥≥ˆ“«∆˜√˚≥∆º∞∆‰÷–µƒ“©∆∑)°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
13£Æ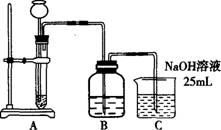 ƒ≥—ß…˙ƒ‚”√50mL NaOH»Ð“∫Œ¸ ’CO2∆¯Ã£¨÷∆±∏Na2CO3°£Œ™¡À∑¿÷πÕ®»ÎµƒCO2∆¯ÃÂπ˝¡ø∂¯…˙≥…NaHCO3£¨À˚…˺∆¡À»Áœ¬ µ—È≤Ω÷Ë£∫¢Ÿ»°25mLNaOH»Ð“∫Œ¸ ’π˝¡øCO2∆¯Ã£¨÷¡CO2∆¯ÃÂ≤ª‘Ÿ»ÐΩ‚£ª¢⁄–°–ƒº”»»»Ð“∫1-2min≈≈≥˝»Ð“∫÷–»ÐΩ‚µƒCO2∆¯Ã£ª¢€‘⁄µ√µΩµƒ»Ð“∫÷–º”»Î¡Ì“ª∞Î(25mL)NaOH»Ð“∫£¨ π»Ð“∫≥‰∑÷ªÏ∫œ°£
ƒ≥—ß…˙ƒ‚”√50mL NaOH»Ð“∫Œ¸ ’CO2∆¯Ã£¨÷∆±∏Na2CO3°£Œ™¡À∑¿÷πÕ®»ÎµƒCO2∆¯ÃÂπ˝¡ø∂¯…˙≥…NaHCO3£¨À˚…˺∆¡À»Áœ¬ µ—È≤Ω÷Ë£∫¢Ÿ»°25mLNaOH»Ð“∫Œ¸ ’π˝¡øCO2∆¯Ã£¨÷¡CO2∆¯ÃÂ≤ª‘Ÿ»ÐΩ‚£ª¢⁄–°–ƒº”»»»Ð“∫1-2min≈≈≥˝»Ð“∫÷–»ÐΩ‚µƒCO2∆¯Ã£ª¢€‘⁄µ√µΩµƒ»Ð“∫÷–º”»Î¡Ì“ª∞Î(25mL)NaOH»Ð“∫£¨ π»Ð“∫≥‰∑÷ªÏ∫œ°£
(1)À˚ƒÐ∑Ò÷∆µ√Ωœ¥ø檵ƒNa2CO3?°°°°°°°°°°°°°°°°°°°° °£∞¥À˚µƒ…˺∆£¨°°°° µ⁄¢Ÿ≤Ω µ—È◊∞÷√»Á…œÕºÀ˘ æ°£
(2)◊∞÷√A π”√µƒ ‘º¡ « ت“ Ø∫Õ—ŒÀ·»Ð“∫£¨ø…∑Ò π”√¥øºÓ¥˙°° ÃÊ Øª“ Ø?°°°°°°°° £¨‘≠“Ú «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°° °£
(3)◊∞÷√B π”√µƒ ‘º¡ «°°°°°°°°°°°°°°°°°°°° £¨◊˜”√ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(4)”–»À»œŒ™ µ—È≤Ω÷Ë¢⁄¢€µƒÀ≥–Ú∂‘µ˜£¨º¥œ»ªÏ∫œ‘Ÿº”»»£¨∏¸∫œ¿Ì£¨ƒ„»œŒ™∂‘¬?Œ™ ≤√¥?
12£Æ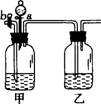 µ—È “ø…”√”“Õº◊∞÷√Ω´CO2∫ÕCOΩ¯––∑÷¿Î∫Õ∏…‘Ô£¨“—÷™a°¢bæ˘Œ™ªÓ»˚£¨ ‘ªÿ¥£∫¢Ÿº◊∆ø÷–”¶◊∞°°°°°°°°°°°°°°°°°°°°°°°°°° £¨∑÷“∫¬©∂∑÷–”¶◊∞°°°°°°°°°°°°°°°°°° °£¢⁄µ±CO2∫ÕCOªÏ∫œ∆¯ÃÂÕ®π˝∏√◊∞÷√ ±£¨œ»∑÷¿Îµ√µΩµƒ∆¯Ã «°°°°°°°° £¨ªÓ»˚≤Ÿ◊˜ «£∫πÿ±’°° °°°°°° ¥Úø™°°°°°° °£»ª∫Ûµ√µΩ∆¯Ã£¨ªÓ»˚≤Ÿ◊˜ «πÿ±’°°°° °° £¨¥Úø™°°°°°° °£
µ—È “ø…”√”“Õº◊∞÷√Ω´CO2∫ÕCOΩ¯––∑÷¿Î∫Õ∏…‘Ô£¨“—÷™a°¢bæ˘Œ™ªÓ»˚£¨ ‘ªÿ¥£∫¢Ÿº◊∆ø÷–”¶◊∞°°°°°°°°°°°°°°°°°°°°°°°°°° £¨∑÷“∫¬©∂∑÷–”¶◊∞°°°°°°°°°°°°°°°°°° °£¢⁄µ±CO2∫ÕCOªÏ∫œ∆¯ÃÂÕ®π˝∏√◊∞÷√ ±£¨œ»∑÷¿Îµ√µΩµƒ∆¯Ã «°°°°°°°° £¨ªÓ»˚≤Ÿ◊˜ «£∫πÿ±’°° °°°°°° ¥Úø™°°°°°° °£»ª∫Ûµ√µΩ∆¯Ã£¨ªÓ»˚≤Ÿ◊˜ «πÿ±’°°°° °° £¨¥Úø™°°°°°° °£
11£Æ‘⁄–¬÷∆µƒ∂˛—ıªØú∆¯ÃÂ÷–≥£ªÏ”–…Ÿ¡øµƒ—ı∆¯°¢¡ÚªØ«‚∫ÕÀÆ’Ù∆¯°¢HClÀƒ÷÷‘”÷ £¨ø…—°”√£∫¢Ÿ≈®¡ÚÀ·£¨¢⁄∫Ï»»Õ≠ÀøÕ¯£¨¢€±•∫ÕNaHCO3»Ð“∫£¨¢Ð¡ÚÀ·Õ≠»Ð“∫£¨÷“ª≥˝»•∏˜÷÷‘”÷ £¨µ√µΩ∏…‘Ôµƒ∂˛—ıªØú∆¯Ã£¨∆‰’˝»∑µƒ≤Ÿ◊˜À≥–Ú «°°°°°°°°°°°°°° °°°°°°°°°°°°°° °£
10£ÆΩ´“ª∂®¡øµƒÃº”Î8g—ı∆¯÷√”⁄√б’»ð∆˜÷–£¨ π÷Æ‘⁄∏þŒ¬œ¬∑¥”¶£¨µ±ª÷∏¥÷¡‘≠Œ¬∂» ±£¨»ð∆˜ƒ⁄—π«ø±»‘≠¿¥‘ˆ¥Û0.4±∂°£‘Ú≤Œº”∑¥”¶µƒÃºµƒ÷ ¡øŒ™(°° )
A£Æ2.4g°°°°°°°°°°°°°°°°°°°°°° B£Æ3g°°°°°°°°°°°°°°°°°°°°°°°°°° C£Æ4.2g°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° D£Æ6g
9£Æ‘⁄ µ—È “÷–£¨”√–ø°¢—ıªØÕ≠°¢œ°¡ÚÀ·Œ™‘≠¡œ÷∆»°Õ≠£¨”–œ¬¡–¡Ω÷÷Õææ∂£∫
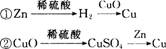
»Ù”√’‚¡Ω÷÷∑Ω∑®÷∆»°Õ≠µƒ÷ ¡øœýµ» ±£¨œ¬¡–∑˚∫œ µ—ÈΩ·π˚µƒ «(°° )
A£Æœ˚∫ƒœýÕ¨÷ À‰µƒ—ıªØÕ≠°°°°°°°°°°°°°°°°°°°°°°°°°°°° B£Æœ˚∫ƒœýÕ¨÷ ¡øµƒ–ø
C£Æœ˚∫ƒœýÕ¨÷ ¡øµƒH2SO4°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°° D£Æ…˙≥…µƒ¡ÚÀ·–øµƒ÷ ¡øœýÕ¨
8£Æ∑≈‘⁄≥®ø⁄»ð∆˜÷–µƒœ¬¡–»Ð“∫£¨æ√÷√∫ۻГ∫÷–∏√»Ð÷ µƒ≈®∂»ª·±‰¥Ûµƒ «(°° )
A£Æ≈®¡ÚÀ·°°°°°°°°°°°°°°°°°° B£Æ«‚—ıªØƒ∆°°°°°°°°°°°°°° C£Æ¬»ÀÆ°°°°°°°°°°°°°°°°°°°°°°°°°°°° D£Æ¬»ªØƒ∆
7£Æœ¬¡– µ—È£¨“ª∂®≤ªª·≥ˆœ÷≥¡µÌœ÷œÛµƒ «(°° )
A£ÆCO2∆¯ÃÂÕ®»ÎNa2SiO3»Ð“∫÷–°°°°°°°°°°°°°°°°°°°° B£ÆCO2∆¯ÃÂÕ®»Î±•∫ÕNa2CO3»Ð“∫÷–
C£ÆSO2∆¯ÃÂÕ®»ÎBaCl2»Ð“∫÷–°°°°°°°°°°°°°°°°°°°°°°°° D£ÆSO2∆¯ÃÂÕ®»ÎBa(NO3)2»Ð“∫÷–
6£Æ”… µ—È≤‚µ√£¨∞—Õ¨ŒÔ÷ µƒ¡ø≈®∂»µƒNaOH»Ð“∫µŒ»ÎCuSO4»Ð“∫÷–£¨¡Ω’þê˝±»Œ™1.5£∫1 ±(≤–¥Ê‘⁄»Ð“∫÷–µƒCu2+º´…Ÿ£¨ø…»œŒ™»´≤ø◊™»Î≥¡µÌ÷–)£¨À˘…˙≥…µƒ≥¡µÌµƒªØ—ß Ω «(°° )
A£ÆCu(OH)2°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° B£ÆCu(OH)2°§CuSO4°°°°°°°°°°°° C£Æ2Cu(OH)2°§CuSO4°°°°°°°°°°°°°°°°°°°°°° D£Æ3Cu(OH)2°§CuSO4
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com