
14.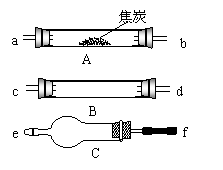 (15 分) 水蒸气通过的灼热的焦炭后,流出气体的主要成分是 CO 是 H2,还有 CO2 和水蒸气等。请用下图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气体中有CO 和 H2。(加热装置和导管等在图中略去)
(15 分) 水蒸气通过的灼热的焦炭后,流出气体的主要成分是 CO 是 H2,还有 CO2 和水蒸气等。请用下图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气体中有CO 和 H2。(加热装置和导管等在图中略去)
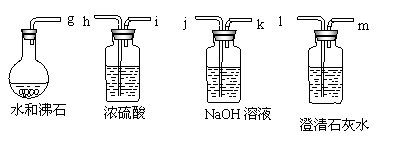
回答下列问题:
(1)盛浓 H2SO4 的装置用途是_____________________, 盛 NaOH 溶液的装置用途是_______________。
(2)仪器 B 中需加入试剂的名称(或化学式)是: _____________________,
所发生反应的化学方程是: _____________________,
(3)仪器 C 中需加入试剂的名称(或化学式)是: ___________________, 其目的是 ___________________。
(4)按气流方向连接各仪器,用字母表示接口的连接顺序:g-ab-_______________。
(5)能证明混合气中含有 CO 的实验依据是___________________.
(6)能证明混合气中含有 H2 的实验依据是___________________。
13.(15 分)
A、B、C、D、E 均为可溶于水的固体,组成它们的离子有
|
阳离子 |
Na + Mg
2+ Al 3+ Ba 2+ |
|
阴离子 |
OH - Cl - CO3 2- SO4 2- HSO4 - |
分别取它们的水溶液进行实验,结果如下:
①A溶液与 B 溶液反应生成白色沉淀,沉淀可溶于 E 溶液;
②A溶液与 C 溶液反应生成白色沉淀,沉淀可溶于 E 溶液;
③A溶液与 D 溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失。
据此推断它们是
A ___________;B_______;C___________;D______________;E_____________;
12.(15 分) W、X、Y 和 Z都是周期表中前 20 号元素,已知:
①W 的阳离子和 Y 的阴离子具有相同的核外电子排布,且能形成组成为 WY 的化合物;②Y 和 Z属同族元素,它们能形成两种常见化合物;
③X 和 Z属同一周期元素,它们能形成两种气态化合物;
④W 和 X 能形成组成的 WX2 的化合物;
⑤X 和 Y 不在同一周期,它们能形成组成为 XY2 的化合物。
请回答: (1)W 元素是 _______________;Z元素是_____________________。
(2)化合物 WY 和 WX2 的化学式分别是 ______________和__________________。
(3)Y 和 Z形成的两种常见化合物的分子式是 ____________和 _______________。
(4)写出 X 和 Z形成的一种气态化合物跟 WZ反应的化学方程式:_____________.
11.(16 分)用 A + 、B- 、C 2- 、D、E、F、G 和 H分别表示含有 18个电子的八种微粒(离子或分子),请回答:
(1)A元素是 ① 、B 元素是 ② 、C 元素是 ③ (用元素符号表示)。
(2)D 是由两种元素组成的双原子分子,其分子式是 ④ 。
(3) E 是所有含 18 个电子的微粒中氧化能力最强的分子,其分子式是 ⑤ 。
(4)F 是由两种元素组成的三原子分子,其分子式是 ⑥ ,电子式是 ⑦ 。
(5)G 分子中含有 4 个原子,其分子式是 ⑧ 。
(6)H 分子中含有 8 个原子,其分子式是 ⑨ 。
10.下列说法正确的是
A.发生化学反应时失去电子越多的金属原子,还原能力越强
B.化合反应可能是氧化还原反应,离子反应不可能是氧化还原反应
C.根据反应PbO2 + 4HCl(浓)=PbCl2+Cl2↑+2H2O可知,PbO2的氧化性强于Cl2
D.在反应NaH+H2O=NaOH+H2↑中,每生成1molH2转移2mol电子
9.等物质的量的下列化合物在相应条件下完全分解后得到氧气最多的是
(A)KClO3(加MnO2催化剂,加热) (B)KMnO4加热
(C)H2O2(水溶液,加MnO2催化剂) (D)HgO(加热)
8.已知氧气还原反应
2Cu(IO3)2+24KI+12H2SO4=2CuI4 +13I2+12K2SO4+12H2O
其中1mol氧化剂在反应中得到的电子为
(A)10 mol (B)11 mol (C)12 mol (D)13 mol
7.在三个密闭容器中分别充入Ne,H2,O2三种气体,当他们的温度和密度都相同时,这三种气体的压强(p),从大到小的顺序是
(A)p(Ne)>p(H2)>p(O2) (B)p(O2)> p(Ne)> p(H2)
(C) p(H2)> p(O2)> p(Ne) (D) p(H2)> p(Ne)> p(O2)
6.以惰性电极电解CuSO4溶液,若阳极上产生的气体的物质的量为0.0100 mol,则阳极上析出Cu的质量为
A.0.64 g B.1.28 g C.2.56 g D.5.12g
5.在盛有稀 H2SO4 的烧杯中放入用导线连接锌片和铜片,下列叙述正确的是
A.正极附近的 SO4 2- 离子浓度逐渐增大 B.电子通过导线由铜片流向锌片
C.正极有 O2 逸出 D.铜片上有 H2 逸出
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com