
10.(2010·哈尔滨模拟)下列叙述中正确的是 ( )
A.O3和NO2都是共价化合物
B.有化学键断裂的变化属于化学变化
C.在离子化合物与共价化合物中,都不存在单个小分子
D.在反应O3+2KI+H2O===2KOH+I2+O2中,参加反应的所有臭氧都作氧化剂
解析:O3为单质,A项错误;化学变化的实质是旧化学键断裂和新化学键生成,仅有化学键断裂不是化学反应,如氯化钠溶于水,离子键断裂,属于物理变化,B项错误;离子化合物中不存在分子,共价化合物中有的不含有分子,如二氧化硅,有的却含有分子,如水、氯化氢等,C项错误;臭氧中的三个氧原子是按照一定方式结合的,虽然反应后有两个氧原子化合价没有变化,但臭氧作为一个整体,化合价发生了变化,D项正确.
答案:D
9.下列物质按只含离子键、只含共价键、既含离子键又含共价键的顺序排列的是( )
A.氯气 二氧化碳 氢氧化钠
B.氯化钠 过氧化氢 氯化铵
C.氯化钠 过氧化钠 氯化铵
D.氯化钠 氦气 氢氧化钠
解析:A项,Cl2中只含共价键;C项,Na2O2中既含离子键,又含共价键;D项,氦气中不含任何化学键.
答案:B
8.下列物质中,只含有极性键的共价化合物是 ( )
A.Na2O2 B.Ba(OH)2
C.HClO D.H2O2
解析:A项,Na2O2是含有非极性共价键和离子键的离子化合物;B项,Ba(OH)2是含有极性共价键和离子键的离子化合物;C项,HClO中氢原子和氧原子、氧原子和氯原子之间形成的都是极性共价键,HClO为共价化合物;D项H2O2既含极性键又含 非极性键.
答案:C
7.下列各分子中,所有原子都满足最外层为8电子结构的是 ( )
A.H2O B.BF3
C.CCl4 D.PCl5
解析:水分子中每个氢原子都与氧原子形成一个共价键,此时氧原子最外层为8电子结构,但氢原子外层只有2个电子,A不正确;BF3分子中3个氟原子与硼原子最外层的3个电子形成3个共价键,硼原子最外层共有6个电子,B不正确;碳原子最外层有4个电子,可与4个氯原子形成4个共价键,此时碳、氯皆达到8电子结构,C正确;PCl5中磷原子最外层有5个电子,若与5个氯原子形成共价键时,磷原子最外层有10个电子,D不正确.
答案:C
6.(2009·长春模拟)氯化钠是日常生活中人们常用的调味品.下列性质可以证明氯化钠中一定存在离子键的是 ( )
A.具有较高的熔点 B.熔融状态下能导电
C.水溶液能导电 D.常温下能溶于水
解析:只要化合物中存在离子键必为离子化合物,而离子化合物区别于共价化合物的突出特点是:熔融状态下能导电,故B正确;至于A具有较高的熔点,也可能为共价化合物,如SiO2;C项水溶液能导电,可以是共价化合物如硫酸等;D项可溶于水的化合物可以是离子化合物也可以是共价化合物.
答案:B
5.某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键( )
A.一定是离子键
B.一定是共价键
C.可能是离子键,也可能是共价键
D.可能不形成化学键
解析:最外层只有一个电子的元素可能是氢元素,也可能是碱金属元素,与卤素结合时可能形成离子键,也可能形成共价健.
答案:C
4.现有如下各种说法:
①在水中氢、氧原子间均以化学键相结合
②金属和非金属化合时一定形成离子键
③离子键是阳离子、阴离子的相互吸引力
④根据电离方程式HCl===H++Cl-,判断HCl分子里存在离子键
⑤H2分子和Cl2分子的反应过程是H2、Cl2分子里共价键发生断裂生成H原子、Cl原子,而后H原子、Cl原子形成离子键的过程.
上述各种说法正确的是 ( )
A.①②⑤ B.都不正确
C.④ D.①
解析:水分子内H、O原子之间形成化学键,分子间的H、O原子的作用是分子间作用力(氢键),故①不正确;活泼金属和活泼非金属化合时才形成离子键,故②不正确;在离子化合物中,阴、阳离子间存在相互作用,不单指相互吸引,还有相互排斥,故③不正确;HCl属于共价化合物,分子中没有离子键,故④不正确;化学反应的本质是旧键断裂,新键形成的过程,但HCl中存在共价键而非离子键,故⑤不正确.
答案:B
3.下列电子式中,正确的是 ( )
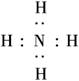

A.[ ]+Cl- B.Na+[ ?H]
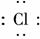
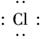

C.Na+[? ?]2-Na+ D. ?-[Ca2+]? ?-
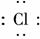
解析:A中Cl-的电子式,应为[? ]-,B中OH-漏标电荷数,C项正确,D中[ ]
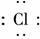
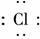
标错,应为[? ?]-Ca2+[? ?]-.
答案:C
2.关于化学键的下列叙述中,正确的是 ( )
A.离子化合物可能含共价键,共价化合物中不含离子键
B.共价化合物可能含离子键,离子化合物中只含离子键
C.构成单质分子的粒子一定含有共价键
D.离子键的实质是阴、阳离子的静电吸引作用
解析:含有离子键的化合物是离子化合物,只含共价键的化合物是共价化合物,A项正确,B项错误.稀有气体分子内不含化学键,C项错误.化学键是原子或离子之间的强相互作用,既有静电吸引,又有静电排斥,D项错误.
答案:A
1.下列物质中含有共价键的离子化合物是 ( )
A.Ba(OH)2 B.KCl
C.H2O D.H2
解析:H2O、H2中只含共价键,Ba(OH)2、KCl是离子化合物,在OH-中含有共价键.
答案:A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com