
7.1kg锂燃烧可放出42 998 kJ的热量,如将1 kg锂通过热核反应放出的能量相当于20 000t优质煤的燃烧。(锂的相对原子质量取7.0)
(1)写出锂燃烧的热化学方程式__________________________________。
(2)Li还可以组成Li电池,它是一种高能电池,在电池中Li作_______极,Li是IA族元素,在该电池中的电解质采用非水溶性有机电解质,原因是____________________。Li-I2电池常作心脏起搏器的电源,若电池中Li为14g,则理论上需I2为__________g,可产生________C电量(1个电子的电量为1.6×10-19C) 。
专题2 化学反应与能量变化
第4单元 太阳能、生物质能与氢能的利用
课时6:太阳能、生物质能与氢能的利用
6.如右图所示,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡。小心地从烧杯中央滴入CuSO4溶液。
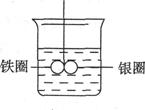 (1)片刻后可观察到的现象是(指悬吊的金属圈)______________。
(1)片刻后可观察到的现象是(指悬吊的金属圈)______________。
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
(2)产生上述现象的原因是_______________________________
5.(1)粗铜中含有少量锌、铁、银、金等金属,采用电解法提纯粗铜时,应以__________为阳极,_________为阴极,__________为电解质溶液,电解时,在阴极上还原出来的金属是_____,留在溶液中的离子是_________________。
(2)欲在铜片上镀银,请设计实验,画出装置图,注明电极和电解质溶液的名称,写出电极方程式________________________________________________。
4.下列关于铜电极的叙述正确的是
A.铜锌原电池中铜是正极
B.用电解法精炼铜时粗铜作阴极
C.在电镀时,镀件上镀铜可用铜作阳极
D.电解饱和食盐水时,用铜片作阳极
3.已知空气一锌电池的电极反应为:锌片Zn+2OH――2e-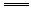 ZnO+H2O,石墨
ZnO+H2O,石墨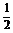 O2+H2O+2e-
O2+H2O+2e-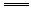 2OH-。据此判断锌片是
2OH-。据此判断锌片是
A.负极,并被氧化 B.负极,并被还原
C.正极,并被氧化 D.正极,并被还原
2.下列叙述不能达到电镀目的的是
A.铜作阳极,锌作阴极,硫酸铜作电解质溶液
B.锌作阳极,铜作阴极,硫酸锌作电解质溶液
C.铁接在直流电源的正极,银接在直流电源的负极,硝酸银溶液作电解质溶液
D.铁接在直流电源的负极,银接在支流电源的正极,硝酸银溶液作电解质溶液
1.在原电池和电解池的电极上所发生的反应,同属氧化反应或同属还原反应的是
A.原电池正极和电解池阳极所发生的反应
B.原电池正极和电解池阴极所发生的反应
C.原电池负极和电解池阳极所发生的反应
D.原电池负极和电解池阴极所发生的反应
10.铜片、锌片连接后浸入稀硫酸中构成原电池,当导线上通过3.01×1022个电子时,锌失去电子_________mol,锌片质量减少________g。铜片表面析出氢气_________L(标准状况)。
课时5:电能转化为化学能
9.在原电池中,较活泼的金属组成的电极是______极,电池工作时这一极不断有电子流____,同时发生_____________反应,常常伴随的现象是_________________________;较不活泼的金属组成的电极是________极,电池工作时,这一极不断有电子流_________,同时发生________反应,常常伴随的现象是________________________。
8.埋在地下的输油铸铁管道,在下列各种情况下,被腐蚀速率最慢的是
A.在含铁元素较多的酸性土壤中 B.在干燥致密不透气的土壤中
C.在潮湿疏松透气的土壤中 D.在含碳粒较多的潮湿透气的中性土壤中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com