
6.由H2SO4、Al2O3、NaOH、Mg、Cl2两两之间进行反应,可制得的正盐有
A.5种 B.6种 C.7种 D.8种
5.向含有amol AlCl3溶液中加入含有bmol KOH溶液,生成沉淀的物质的量可能是
①amol ②bmol ③a/3mol ④b/3mol ⑤0mol ⑥(4a-b)mol
A.①③④⑤⑥ B.①②③④⑤
C.①④⑤⑥ D.①④⑤
4.下列各组物质中的两种物质相互反应时,无论哪种物质过量,均可用一个离子方程式表示的是
A.硫酸与偏铝酸钠溶液 B.氯化铜溶液与氨水
C.苯酚钠溶液与二氧化碳 D.硝酸银溶液与烧碱
3.实现Al3++3A1O2-+6H2O=4Al(OH)3↓,正确的做法是
A.向铝盐溶液中不断加入纯碱溶液
B.向铝盐溶液中不断加入小苏打溶液
C.向烧碱溶液中不断滴入铝盐溶液
D.向铝盐溶液中不断滴入烧碱溶液
2.①氧化钠、②氢氧化钠、③过氧化钠、④亚硫酸钠。各1摩尔上述固体物质,长期放置于空气中,最后质量增加情况是(不考虑潮解因素)
A.①=②>③>④ B.①>③>④>②
C.②>①=③>④ D.④>②>③>①
1.试管中装有煤油和水的混合物,静置后放入一小块碱金属,可观察到金属块在煤油和水的界面附近上下往复运动。下列说法不正确的是
A.此碱金属可能为钾或钠
B.上下运动是由于该金属与水反应产生气体
C.反应一段时间煤油会燃烧
D.若是金属铷,则上下运动的幅度比钠大
7.将一块铜板浸泡在一定浓度的FeCl3溶液中一段时间后取出,得到一混合溶液,某校化学兴趣小组的同学为分析该混合溶液的组成,进行了如下实验:
Ⅰ、取50.0mL混合溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为86.1 g;
Ⅱ、另取50.0mL混合溶液,向其中加入1.40 g铁粉,结果铁粉全部溶解但未见固体析出;
Ⅲ、再取50.0mL混合溶液,向其中加入20.0 mL稀硝酸,到一种无色气体,其体积换算成标准状况时为0.448 L ;请根据以上实验中得到的数据分析计算:
⑴ 原FeCl3溶液物质的量浓度(反应过程中过程中溶液体积的变化忽略不计);
⑵ 所得混合溶液中c(Cu2+)的取值范围。
[课后巩固]
6.如下图所示:是用明矾[KAl(SO4)2·12H2O]制取硫酸铝和硫酸钾的操作步骤流程图(图中略去了沉淀物的洗涤操作),请在图中圆括号内填入适当的试剂名称,在方括号内填入适当的分离方法,并回答有关问题。
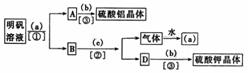
(1)试剂a是 ,b是 ,c是 。分离方法①是 ,②是 ,③是 。
(2)按上述操作,不考虑损耗,在理论上,158g明矾最多可以制得Al2(SO4)3·18H2O____g,至少可以制得K2SO4______g。
5.回答下列有关金属铜的问题:
(1)在使用电烙铁时,其头部是一铜制的烙铁头,长期使用,表面被氧化,但脱落下来的氧化膜却是红色的,试说明原因。
(2)许多金属导体在导电过程中易冒电火花;铜的导电性仅次于银,但价格较低。试分析在航空仪表中为什么不采用铜,而是用价格较为昂贵的Au、Pt、Pd的合金作为触点?
(3)CuS既可溶于稀HNO3,又可溶于KCN,这两种溶解过程明显不同,前一反应中CuS生成S单质,后一反应中CuS生成(Cu(CN)4)3-。写出化学方程式。
4.将amL 0.1mol/L硫酸铝溶液与bmL 0.5mol/L氢氧化钠溶液混合,得到cmol氢氧化铝沉淀,若已知a、b、c中任意两个值,求另一个值,所求的值不止一个解的是(各选项中,单位均已略去)
A.a=100 b=90 c=? B.a=100 c=0.015 b=?
C.b=90 c=0.015 a=? D.a=75 c=0.015 b=?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com