
1ЃЎвЛЕШбќШ§НЧаЮЕФжмГЄЪЧ20ЃЌЕзБпyЪЧЙигкбќГЄxЕФКЏЪ§ЃЌЫќЕФНтЮіЪНЮЊ(ЁЁ)
AЃЎyЃН20Ѓ2x(x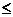 10)ЁЁЁЁЁЁЁЁ BЃЎyЃН20Ѓ2x(xЃМ10)
10)ЁЁЁЁЁЁЁЁ BЃЎyЃН20Ѓ2x(xЃМ10)
CЃЎyЃН20Ѓ2x(5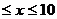 )ЁЁЁЁЁЁЁЁЁЁ
DЃЎyЃН20Ѓ2x(5ЃМxЃМ10)
)ЁЁЁЁЁЁЁЁЁЁ
DЃЎyЃН20Ѓ2x(5ЃМxЃМ10)
1ЃЎ(08дцзЏЕквЛДЮЕїба)ЯжгаAЁЂBЁЂCЁЂDЁЂFСљжжЖЬжмЦкдЊЫиЃЌдкЛЏбЇЗДгІжаОљФмаЮГЩМђЕЅЕФвѕРызгЛђбєРызгЃЌЧвAЁЂBЁЂCЁЂDРызгОпгаЯрЭЌЕФЕчзгВуНсЙЙЁЃ
вбжЊЃКЂйГЃЮТЯТЃЌFЕФЕЅжЪЪЧвЛжжгаЩЋЦјЬхЃЌГЃгУгкЩБОњЁЂЯћЖОЃЛ
ЂкAЕФЕЅжЪвдШмгкNaOHШмвКЃЌЯђЩњГЩЕФШмвКжаЭЈШыCO2ЦјЬхгаАзЩЋГСЕэЩњГЩЃЛ
ЂлCЕФЧтЛЏЮяЗжзгGЪЧОпга10ЕчзгЮЂСЃЃЌЧввдЗЂЩњЯТСазЊЛЏ
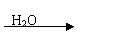


GЁЁЁЁЁЁЁЁЁЁЁЁЁЁ PЁЁЁЁЁЁЁЁЁЁЁЁ QЁЁЁЁЁЁЁЁЁЁЁЁ M+P
ЂмEКЭDЪЧЭЌвЛжїзхЕФдЊЫиЃЌЖўепФмаЮГЩЮЂСЃЕФИіЪ§БШЮЊ1ЃК2КЭ1ЃК3ЕФЛЏКЯЮяTКЭKЃЛ
ЂнBКЭDПЩаЮГЩЮЂСЃИіЪ§БШЮЊ1ЃК1КЭ2ЃК1ЕФРызгЛЏКЯЮяXКЭYЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
ЁЁ (1)BдЊЫиЕФУћГЦЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЃЛ
ЁЁ (2)EдЊЫиЕФдзгНсЙЙЪОвтЭМЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ
 ЁЁ
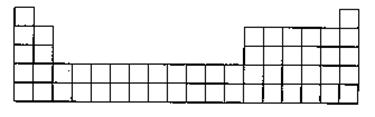
(3)ЧыНЋAЁЂCЕФдЊЫиЗћКХЬюдкШчЭМЫљЪОВПЗждЊЫижмЦкБэЕФЪЪЕБЮЛжУЩЯЁЃ
ЁЁ
(3)ЧыНЋAЁЂCЕФдЊЫиЗћКХЬюдкШчЭМЫљЪОВПЗждЊЫижмЦкБэЕФЪЪЕБЮЛжУЩЯЁЃ
ЁЁ (4)GЕФЕчзгЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃЛЏКЯЮяXЫљКЌЛЏбЇМќРраЭгаЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (5)TгыFЕЅжЪЕФЫЎШмвКЗДгІЕФРызгЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
GгыDЕФЕЅжЪЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
MгыЭЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
3ЃЎ(08ЩНЖЋЖўФЃ)ЯТСаЙигкЮяжЪНсЙЙЕФЫЕЗЈжае§ШЗЕФЪЧ
AЃЎРызгЛЏКЯЮяNaxNO4жаЃЌNO4XЃжаЕФИїдзгзюЭтВуЖМДя8ЕчзгЮШЖЈНсЙЙЃЌдђxЃН3
BЃЎФГдЊЫидзгзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФaБЖЃЌдђИУдзгКЫФкжЪзгЪ§ЮЊa+2
CЃЎD2OЗжзггыH2OЗжзгЪЧЫљКЌЕчзгзмЪ§ВЛЯрЕШЕФМЋадЗжзг
DЃЎдкШЮКЮЮяжЪЕФЗжзгжаЖМКЌгаЛЏбЇМќ
ЗЧбЁдёЬт
2ЃЎ(08ЩНЖЋЖўФЃ)2006Фъ10дТ9ШеЃЌГЏЯЪЧПТѕЁАКЫЁБУХМїНјааСЫКЫЪЕбщЃЌв§Ц№СЫЙњМЪЩчЛсЕФЙуЗКЙизЂЁЃФПЧАЃЌКЫЗДгІВњЩњЕФКЫФмжївЊРДдДгк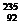 UЕФСбБфЃЌдђЯТСаЫЕЗЈжае§ШЗЕФЪЧ
UЕФСбБфЃЌдђЯТСаЫЕЗЈжае§ШЗЕФЪЧ
AЃЎ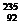 UдзгКЫжага92ИіжЪзгЁЂ143ИіКЫзг
UдзгКЫжага92ИіжЪзгЁЂ143ИіКЫзг
BЃЎ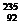 UЕФвЛжжПЩФмЕФСбБфЪЧБфГЩСНИіжаЕШжЪСПЕФдзгКЫЃЌКЫЗДгІЗНГЬЮЊ
UЕФвЛжжПЩФмЕФСбБфЪЧБфГЩСНИіжаЕШжЪСПЕФдзгКЫЃЌКЫЗДгІЗНГЬЮЊ
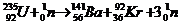 ЃЌЫЕУїUЪЧгЩBaКЭKrзщГЩЕФ
ЃЌЫЕУїUЪЧгЩBaКЭKrзщГЩЕФ
CЃЎ UЪЧЬьШЛЗХЩфаддЊЫиЃЌГЃЮТЯТЫќЕФАыЫЅЦкдМЮЊ45вкФъЃЌЩ§ИпЮТЖШАыЫЅЦкЫѕЖЬ
UЪЧЬьШЛЗХЩфаддЊЫиЃЌГЃЮТЯТЫќЕФАыЫЅЦкдМЮЊ45вкФъЃЌЩ§ИпЮТЖШАыЫЅЦкЫѕЖЬ
DЃЎШєвЛИігЫКЫдкСбБфЧАКѓЕФжЪСППїЫ№ЮЊ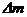 ЃЌдђЦфЪЭЗХЕФКЫФмЮЊ
ЃЌдђЦфЪЭЗХЕФКЫФмЮЊ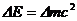
13ЁЂ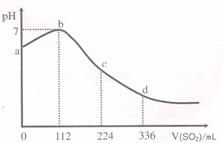 (НЫеЪЁБМХЃИпМЖжабЇ2008-2009бЇФъЖШИпШ§ЕкЖўДЮЕїба)ЃЎБъзМзДПіЯТЃЌФГЭЌбЇЯђ 100 mL H2S БЅКЭШмвКжаЭЈШыSO2ЃЌ ЫљЕУШмвК pH БфЛЏШчЭМЫљЪОЁЃЯТСаЗжЮіжаЃЌе§ШЗЕФЪЧ[A ]
(НЫеЪЁБМХЃИпМЖжабЇ2008-2009бЇФъЖШИпШ§ЕкЖўДЮЕїба)ЃЎБъзМзДПіЯТЃЌФГЭЌбЇЯђ 100 mL H2S БЅКЭШмвКжаЭЈШыSO2ЃЌ ЫљЕУШмвК pH БфЛЏШчЭМЫљЪОЁЃЯТСаЗжЮіжаЃЌе§ШЗЕФЪЧ[A ]
AЃЎab ЖЮЗДгІЪЧЃКSO2 + 2 H2S=3SЁ§+2 H2O
BЃЎбЧСђЫсЪЧБШЧтСђЫсИќШѕЕФЫс
CЃЎдH2SШмвКЕФЮяжЪЕФСПХЈЖШЮЊ0.05 mol•LЃ1
DЃЎb ЕуЖдгІЕФШмвКЕМЕчадзюЧП
12ЃЎ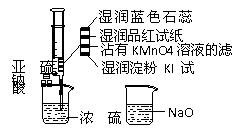 (НЫеЪЁБМХЃИпМЖжабЇ2008-2009бЇФъЖШИпШ§ЕкЖўДЮЕїба)ШчЭМЃЌдкзЂЩфЦїжаМгШыЩйСПNa2SO3ОЇЬхЃЌВЂЮќШыЩйСПХЈСђЫс(вдВЛНгДЅжНЬѕЮЊзМ)ЁЃдђЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ[CD ]
(НЫеЪЁБМХЃИпМЖжабЇ2008-2009бЇФъЖШИпШ§ЕкЖўДЮЕїба)ШчЭМЃЌдкзЂЩфЦїжаМгШыЩйСПNa2SO3ОЇЬхЃЌВЂЮќШыЩйСПХЈСђЫс(вдВЛНгДЅжНЬѕЮЊзМ)ЁЃдђЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ[CD ]
AЃЎРЖЩЋЪЏШяЪджНЯШБфКьКѓЭЪЩЋ
BЃЎЦЗКьЪджНЁЂеДгаKMnO4ШмвКТЫжНОљЭЪЩЋЖМФмжЄУї
SO2ЁЁ ЕФЦЏАзад
CЃЎЪЊШѓЕэЗлKIЪджНЮДБфРЖЫЕУїSO2ЕФбѕЛЏадШѕгкI2
DЃЎNaOHШмвКПЩгУгкГ§ШЅЪЕбщжаЖргрЕФSO2
11ЃЎ(НЫеЪЁоВш09ИпШ§ЛЏбЇВтЪдОэ11дТ)баОПадбЇЯАаЁзщзіЭгыХЈСђЫсЗДгІЪЕбщЪБЃЌЗЂЯжЪдЙмЕзВПгаАзЩЋЙЬЬхВЂМадггаЩйСПКкЩЋЮяжЪЁЃЕЙШЅЪдЙмжаЕФХЈСђЫсЃЌНЋЪЃгрЙЬЬх(КЌЩйСПХЈСђЫс)ЕЙШыЪЂгаЩйСПЫЎЕФЩеБжаЃЌЗЂЯжЫљЕУШмвКЮЊРЖЩЋЃЌКкЩЋЙЬЬхЮДШмНтЁЃЙ§ТЫЁЂЯДЕгКѓЃЌЯђКкЩЋЙЬЬхжаМгШыЙ§СПХЈЯѕЫсЃЌКкЩЋЙЬЬхШмНтЃЌШмвКГЪРЖЩЋЃЌЫљЕУШмвКМгBaCl2ШмвККѓгаАзЩЋГСЕэЩњГЩЁЃЯТСаЫљЕУНсТле§ШЗЕФЪЧ[AD]
AЃЎЭгыХЈСђЫсЗДгІЫљЕУАзЩЋЙЬЬхЪЧCuSO4
BЃЎМгBaCl2ШмвККѓЫљЕУАзЩЋГСЕэЪЧBaSO3
CЃЎАзЩЋЙЬЬхжаМадгЕФЩйСПКкЩЋЮяжЪПЩФмЪЧCuO
DЃЎАзЩЋЙЬЬхжаМадгЕФЩйСПКкЩЋЮяжЪжаКЌдЊЫиCuЁЂS
10ЃЎ(НЫеКЃжнИпМЖжабЇ2009НьИпШ§ЛЏбЇЕкШ§ДЮзлКЯВтЪд)АбвЛЖЈСПЕФаПгы100 mL 18.5 mol/LЕФХЈСђЫсГфЗжЗДгІКѓЃЌаПЭъШЋШмНтЃЌЭЌЪБЩњГЩЦјЬхY 33.6L(дкБъзМзДПіЯТ.)ЁЃНЋЗДгІКѓЕФШмвКЯЁЪЭЕН1 LЃЌВтЕУШмвКЕФpH=1ЃЌдђЯТСаа№Ъіе§ШЗЕФЪЧ( ADЁЁЁЁ )
AЃЎЦјЬхYЪЧSO2КЭH2ЕФЛьКЯЮяЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ BЃЎЦјЬхYжаSO2КЭH2ЕФЬхЛ§БШЮЊ4:1
CЃЎЗДгІжаЙВЯћКФаП87.5gЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЗДгІжаЙВзЊвЦЕчзг3 mol
9ЃЎ [НЫеЪЁПкАЖжабЇ2008-2009бЇФъЖШИпШ§ФъМЖЕквЛбЇЦкЕкЫФДЮЕїбаВтЪд] (11Зж)зЪСЯЯдЪОВЛЭЌХЈЖШЕФСђЫсгыаПЗДгІЪБЃЌСђЫсПЩвдБЛЛЙдЮЊSO2ЃЌвВПЩБЛЛЙдЮЊЧтЦјЁЃЮЊСЫбщжЄетвЛЪТЪЕЃЌФГЭЌбЇФтгУЯТЭМзАжУНјааЪЕбщ (ЪЕбщЪБбЙЧПЮЊ10lkPaЃЌЮТЖШЮЊ0Ёц)ЁЃЁЁЁЁЁЁ
[НЫеЪЁПкАЖжабЇ2008-2009бЇФъЖШИпШ§ФъМЖЕквЛбЇЦкЕкЫФДЮЕїбаВтЪд] (11Зж)зЪСЯЯдЪОВЛЭЌХЈЖШЕФСђЫсгыаПЗДгІЪБЃЌСђЫсПЩвдБЛЛЙдЮЊSO2ЃЌвВПЩБЛЛЙдЮЊЧтЦјЁЃЮЊСЫбщжЄетвЛЪТЪЕЃЌФГЭЌбЇФтгУЯТЭМзАжУНјааЪЕбщ (ЪЕбщЪБбЙЧПЮЊ10lkPaЃЌЮТЖШЮЊ0Ёц)ЁЃЁЁЁЁЁЁ
ЁЁ(1)ШєдкЩеЦПЗХШы1.30gаПСЃЃЌгыc molЃЏL H2SO4 ЗДгІЃЌЮЊБЃжЄЪЕбщНсТлЕФПЩППЃЌдкЯДЦјЦПжаМгШы1molЃЏL NaOHШмвКЕФЬхЛ§VЁн_______mLЃЌСПЦјЙмЕФЪЪвЫЙцИёЪЧ__________ЁЁЁЁ ___mLЁЃ
(бЁЬюЃК200,400,500)ЁЃ
ЁЁ(2)Шє1.30gаПСЃЭъШЋШмНтЃЌЧтбѕЛЏФЦЯДЦјЦПдіжиl.28g ЃЌдђЗЂЩњЗДСЂЕФЛЏбЇЗНГЬЪНЮЊЃК__________________ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ _____ЁЃ
ЁЁ (3)ШєЩеЦПжаЭЖШыagаПЧвЭъШЋЗДгІЃЌЧтбѕЛЏФЦЯДЦјЦПдіжиb gЃЎСПЦјЦПжаЪеМЏЕНVmLЦјЬхЃЌдђгаЃКagЃЏ65gЁЄmolЃ1ЃНbgЃЏ64gЁЄmolЃ1+V mL / 22400 mLЁЄmolЃ1ЃЌвРОнЕФдРэЪЧ ___________________________________ЁЁЁЁЁЁЁЁЁЁ ________________________ЁЃ
ЁЁ (4)ШєдкЩеЦПжаЭЖШыd gаПЃЌМгШывЛЖЈСПЕФc molЃЏL ХЈСђЫсV LЃЌГфЗжЗДгІКѓаПгаЪЃгрЃЌВтЕУЧтбѕЛЏФЦЯДЦјЦПдіжиmgЃЌдђећИіЪЕбщЙ§ГЬВњЩњЕФЦјЬхжаЃЌn(H2)/n(SO2)
ЃН_____________ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ __(гУКЌзжФИЕФДњЪ§ЪНБэЪО)ЁЃ
Д№АИ.(1)20,500 (2)Zn+2H2SO4=ZnSO4+SO2Ёќ+2H2O
(3)ЕУЪЇЕчзгЪиКу (4)(64CV-2m)/m(ЧАШ§ПеУПЬт2ЗжЃЌКѓвЛПеУПЬт3ЗжЁЃ) w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
8ЃЎ[НЫеЪЁПкАЖжабЇ2009НьИпШ§ФъМЖЕкЖўДЮдТПМЛЏбЇЪдЬт](10Зж)ПеЦјжаЕФSO2КЌСПКЭПЩЮќШыПХСЃЕФКЌСП(ПЩгУg/cm3БэЪО)ЖМЪЧживЊЕФПеЦјжЪСПжИБъЁЃдкЙЄвЕЩњВњЩЯЙцЖЈЃКПеЦјжаЖўбѕЛЏСђЕФзюДѓдЪаэХХЗХХЈЖШВЛЕУГЌЙ§0.02mg/LЁЃ
ЂХЮЊВтЖЈФГЕиЗНЕФПеЦјжаSO2КЭПЩЮќШыПХСЃЕФКЌСПЃЌМзЭЌбЇЩшМЦСЫШчЯТЭМЫљЪОЕФЪЕбщзАжУЃК
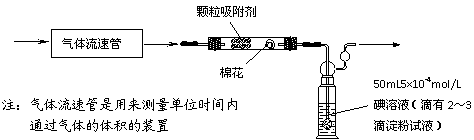
гІгУЩЯЪізАжУВтЖЈПеЦјжаЕФSO2КЌСПКЭПЩЮќШыПХСЃЕФКЌСПЃЌГ§ВтЖЈЦјЬхСїЫй(ЕЅЮЛЃКcm3/min)ЭтЃЌЛЙашвЊВтЖЈЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
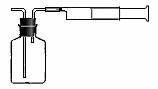 ЂЦввЭЌбЇФтгУЯТСаМђвззАжУВтЖЈПеЦјжаЕФSO2КЌСПЃКзМШЗЁЁЁЁЁЁ вЦШЁ50mL5ЁС10-4mol/LЕФБъзМЕтЫЎШмвКЃЌзЂШыгвЭМЫљЪОЙуПкЦПжаЃЌМг2-3ЕЮЕэЗлжИЪОМСЃЌДЫЪБШмвКГЪРЖЩЋЁЃдкжИЖЈЕФВтЖЈЕиЕуГщЦјЃЌУПДЮГщЦј100mLЃЌжБЕНШмвКЕФРЖЩЋШЋВПЭЪОЁЮЊжЙЃЌМЧТМГщЦјДЮЪ§(n)ЁЃ
ЂЦввЭЌбЇФтгУЯТСаМђвззАжУВтЖЈПеЦјжаЕФSO2КЌСПЃКзМШЗЁЁЁЁЁЁ вЦШЁ50mL5ЁС10-4mol/LЕФБъзМЕтЫЎШмвКЃЌзЂШыгвЭМЫљЪОЙуПкЦПжаЃЌМг2-3ЕЮЕэЗлжИЪОМСЃЌДЫЪБШмвКГЪРЖЩЋЁЃдкжИЖЈЕФВтЖЈЕиЕуГщЦјЃЌУПДЮГщЦј100mLЃЌжБЕНШмвКЕФРЖЩЋШЋВПЭЪОЁЮЊжЙЃЌМЧТМГщЦјДЮЪ§(n)ЁЃ w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
ЂйМйЩшввЭЌбЇЕФВтСПЪЧзМШЗЕФЃЌввЭЌбЇГщЦјЕФДЮЪ§жСЩйЮЊЁЁЁЁЁЁЁЁ ДЮЃЌЗНПЩЫЕУїИУЕиПеЦјжаЕФSO2КЌСПЗћКЯХХЗХБъзМЁЃ
ЂкШчЙћввЭЌбЇгУИУЗНЗЈВтСППеЦјжаSO2ЕФКЌСПЪБЃЌЫљВтЕУЕФЪ§жЕБШЪЕМЪКЌСПЕЭЃЌЧыФуЖдЦфПЩФмЕФдвђ(МйЩшШмвКХфжЦЁЂГЦСПЛђСПШЁМАИїжжЖСЪ§ОљЮоДэЮѓ)ЬсГіКЯРэМйЩшЃК_____________________________________________________ЁЁЁЁЁЁ __________ЁЃ
ЂлБћЭЌбЇШЯЮЊЃКввЭЌбЇЕФЪЕбщЗНАИашвЊГщЦјЕФДЮЪ§ЬЋЖрЃЌВйзїТщЗГЁЃгыввЬжТлКѓЃЌОіЖЈНЋГщЦјДЮЪ§НЕЕН100ДЮвдЯТЃЌЧыФуЩшМЦКЯРэЕФИФНјЗНАИЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЧИФБфКЯЪЪЕФЮќЪевКЃЌввЭЌбЇЪЙгУЕФзАжУЛЙПЩвдВтЖЈаТзАаоЕФОгЪвПеЦјжаМзШЉЕФХЈЖШЃЌЮќЪеМСзюКУбЁгУЁЁЁЁЁЁЁЁ (бЁЬюЃКЂйХЈСђЫсЁЂЂквјАБШмвКЁЂЂлаТжЦЕФЧтбѕЛЏЭЁЂЂмЫсЛЏЕФИпУЬЫсМиШмвК)ЁЃ
Д№АИЃЎЂХШмвКРЖЩЋЧЁКУЭЪШЅЫљашЕФЪБМфЃЌЮќЪеЧАКѓПХСЃЮќИНМСЁЂУоЛЈЁЂЪЂЗХШнЦїЕФзмжЪСП
ЂЦЂй800ЁЁ ЂкГщЦјЫйЖШЙ§ПьЃЌЛђзАжУЦјУмадНЯВю
ЂлНЋ50mL5ЁС10-4mol/LЕФЕтШмвКЕФЬхЛ§МѕаЁЮЊ5mLЃЌВЂНЋЙуПкЦПИФЮЊЪдЙм
ЂЧЂмЁЁЁЁ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com