
12. (09天津卷 10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:

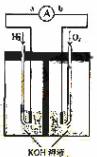 (1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
 (用a、b 表示)。
(用a、b 表示)。
 (2)负极反应式为 。
(2)负极反应式为 。
 (3)电极表面镀铂粉的原因为
。
(3)电极表面镀铂粉的原因为
。
 (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
 Ⅰ.2Li+H2
Ⅰ.2Li+H2
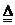 2LIH
2LIH
 Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
 ①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
 ②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
 ③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
答案:
(1)由化学能转变为电能 由a到b
(2)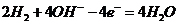 或
或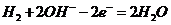
(3)增大电极单位面积吸附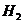 、
、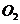 分子数,加快电极反应速率
分子数,加快电极反应速率
(4)①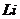
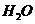
②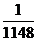 或
或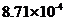
③32
解析:本题考查电化学知识
(1)原电池的实质为化学能转化成电能。总反应为2H2 + O2 =2H2O,其中H2从零价升至+1价,失去电子,即电子从a流向b。
 (2)负极为失去电子的一极,即H2失电子生成H+,由于溶液是碱性的,故电极反应式左右应各加上
(2)负极为失去电子的一极,即H2失电子生成H+,由于溶液是碱性的,故电极反应式左右应各加上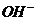 。
。
(3)铂粉的接触面积大,可以加快反应速率。
 (4)I.Li从零价升至+1价,作还原剂。
(4)I.Li从零价升至+1价,作还原剂。
II.H2O的H从+1降至H2中的零价,作氧化剂。由反应I,当吸收10molH2时,则生成20molLiH,V=m/ρ=20×7.9/0.82 ×10-3L=192.68×10-3L。V(LiH)/v(H2)= 192.68×10-3L/224L=8.71×10-4。20mol LiH可生成20mol H2,实际参加反应的H2为20×80%=1.6mol,1molH2转化成1molH2O,转移2mol电子,所以1.6molH2可转移3.2mol的电子
11. (09上海理综11)茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池。在这种电池中
(09上海理综11)茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池。在这种电池中
①铝合金是阳极 ②铝合金是负极
 ③海水是电解液
④铝合金电极发生还原反应
③海水是电解液
④铝合金电极发生还原反应
A.②③ B.②④
C.①② D.①④
答案:A
10.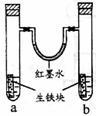 (09上海卷
(09上海卷 13)右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是
13)右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是
 A.生铁块中的碳是原电池的正极
A.生铁块中的碳是原电池的正极
 B.红墨水柱两边的液面变为左低右高
B.红墨水柱两边的液面变为左低右高
 C.两试管中相同的电极反应式是:
C.两试管中相同的电极反应式是: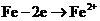
 D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
答案:B
9.(09北京卷6)下列叙述不正确的是
A.铁表面镀锌,铁作阳极
B.船底镶嵌锌块,锌作负极,以防船体被腐蚀
C.钢铁吸氧腐蚀的正极反应: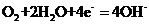
D.工业上电解饱和和食盐水的阳极反应: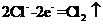
答案:A
8. (09广东化学
(09广东化学 14)可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
14)可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
 A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4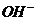
 B.以NaOH溶液为电解液时,负极反应为:Al+3
B.以NaOH溶液为电解液时,负极反应为:Al+3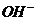 -3e-=Al(OH)3↓
-3e-=Al(OH)3↓
 C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
 D.电池工作时,电子通过外电路从正极流向负极
D.电池工作时,电子通过外电路从正极流向负极
 答案:A
答案:A
 解析: 电解质溶液显碱性或中性, 该燃料电极的正极发生反应为:O2+2H2O+4e-=4
解析: 电解质溶液显碱性或中性, 该燃料电极的正极发生反应为:O2+2H2O+4e-=4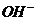 ,A对;铝作负极,负极反应应该是铝失去电子变为铝离子,在氢氧化钠的溶液中铝离子继续与过量的碱反应生成偏铝酸根,因此负极反应为:Al+4
,A对;铝作负极,负极反应应该是铝失去电子变为铝离子,在氢氧化钠的溶液中铝离子继续与过量的碱反应生成偏铝酸根,因此负极反应为:Al+4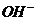 -3e=
-3e=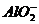 + 2H2O,B错; 该电池在碱性条件下消耗了碱,反应式为4Al+3O2+4
+ 2H2O,B错; 该电池在碱性条件下消耗了碱,反应式为4Al+3O2+4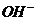 = 4
= 4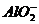 + 2H2O溶液PH降低,C错;电池工作时,电子从负极出来经过外电路流到正极,D错
+ 2H2O溶液PH降低,C错;电池工作时,电子从负极出来经过外电路流到正极,D错
7. (09广东化学 10)出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。下列说法正确的是
10)出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。下列说法正确的是
 A. 锡青铜的熔点比纯铜高
A. 锡青铜的熔点比纯铜高
 B.在自然环境中,锡青铜中的锡对铜起保护作用
B.在自然环境中,锡青铜中的锡对铜起保护作用

 C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快
C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快
 D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程
D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程
 答案:BC
答案:BC
 解析:锡青铜属于合金根据合金的特性,熔点比任何一种纯金属的低判断A错;
解析:锡青铜属于合金根据合金的特性,熔点比任何一种纯金属的低判断A错;
由于锡比铜活泼,故在发生电化学腐蚀时,锡失电子保护铜,B正确;
潮湿的环境将会加快金属的腐蚀速率,C正确;
电化学腐蚀过程实质是有电子的转移,属于化学反应过程,D错。
6. (09福建卷
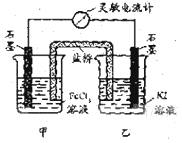
(09福建卷 11) 控制适合的条件,将反应
11) 控制适合的条件,将反应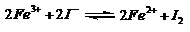 设计成如右图所示的原电池。下列判断不正确的是
设计成如右图所示的原电池。下列判断不正确的是

A. 反应开始时,乙中石墨电极上发生氧化反应
 B. 反应开始时,甲中石墨电极上Fe3+被还原
B. 反应开始时,甲中石墨电极上Fe3+被还原
 C. 电流计读数为零时,反应达到化学平衡状态
C. 电流计读数为零时,反应达到化学平衡状态
 D. 电流计读数为零后,在甲中溶入FeCl2固定,乙中石墨电极为负极
D. 电流计读数为零后,在甲中溶入FeCl2固定,乙中石墨电极为负极
答案:D
解析:乙中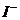 失去电子放电,故为氧化反应,A项正确;
失去电子放电,故为氧化反应,A项正确;
由总反应方程式知,Fe3+被还原成Fe2+,B项正确;
当电流计为零时,即说明没有电子发生转移,可证明反应达平衡,C项正确。
加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,而作为负极,D项错。
5.(09广东理科基础 34)下列有关电池的说法不正确的是
34)下列有关电池的说法不正确的是
 A.手机上用的锂离子电池属于二次电池
A.手机上用的锂离子电池属于二次电池
 B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极

 C.甲醇燃料电池可把化学能转化为电能
C.甲醇燃料电池可把化学能转化为电能
 D.锌锰干电池中,锌电极是负极
D.锌锰干电池中,锌电极是负极
 答案:B
答案:B
 解析:锂离子电池可以充用,再次使用,属于二次电池,A项正确;
解析:锂离子电池可以充用,再次使用,属于二次电池,A项正确;
铜锌原电池中铜为正极,故电流为铜流向锌,而电子是由锌流向铜,B项错;
电池的实质即是化学能转化成电能,C项正确;
Zn失去电子生成Zn2+,故作为负极,D项正确
4.(09浙江卷 12)市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li
12)市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li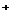 的高分子材料。这种锂离子电池的电池反应为:
的高分子材料。这种锂离子电池的电池反应为:
 Li+2Li
Li+2Li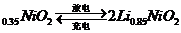
 下列说法不正确的是
下列说法不正确的是
 A.放电时,负极的电极反应式:Li-e
A.放电时,负极的电极反应式:Li-e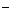 =Li
=Li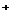
 B.充电时,Li
B.充电时,Li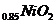 既发生氧化反应又发生还原反应
既发生氧化反应又发生还原反应
 C.该电池不能用水溶液作为电解质
C.该电池不能用水溶液作为电解质
 D.放电过程中Li
D.放电过程中Li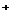 向负极移动
向负极移动

 答案:D
答案:D
3.(09江苏卷 12)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
12)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
 A.该电池能够在高温下工作
A.该电池能够在高温下工作
 B.电池的负极反应为:
B.电池的负极反应为:
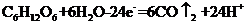
 C.放电过程中,
C.放电过程中,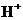 从正极区向负极区迁移
从正极区向负极区迁移
 D.在电池反应中,每消耗1mol氧气,理论上能生成标准状况下
D.在电池反应中,每消耗1mol氧气,理论上能生成标准状况下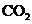 气体
气体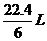
 答案:B
答案:B

 解析:
解析:
A项,高温条件下微生物会变性,所以A错;
B项,负极是葡萄糖失电子生成二氧化碳,所以B对;
C项,原电池内部阳离子应向正极移动,所以C错;
D项,消耗1mol氧气生成1mol二氧化碳,标准状况下体积是22.4L,D错
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com