
下图为北京城市空间扩张的GIS图像示意图。读图,回答6-7题。
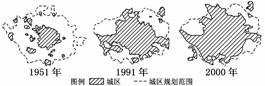
6.图中反映出北京地区城市化的标志为 ( )
A.城市人口数量增加 B.城市用地面积增加
C.城市人口比重增加 D.城市道路密度增加
解析:由图示可以直接看出,北京城区面积在不断地扩大。
答案:B
7.北京城市化过程中出现的主要问题是 ( )
A.城市绿化面积缩小 B.城市居民住房紧张
C.文物古迹普遍受到破坏 D.城市交通拥堵严重
解析:北京城市化出现的主要问题是城市车辆日益增多,导致城市交通拥堵严重。
答案:D
5.2010年上海世博会的主题是“城市,让生活更美好”。上海被看作近代中国城市化进程的缩影。有关近代上海城市化的说法,正确的是 ( )
A.明清时期的资本主义萌芽开启了上海城市化进程
B.以上海为代表的中国城市化进程体现了鲜明的半殖民地特征
C.民族工业的持续发展推动了城市化进程
D.洋务派“中体西用”思想阻碍了上海的城市化进程
解析:明清时期的资本主义萌芽主要出现在丝织业发达的苏州等地,上海城市化进程则开端于鸦片战争之后的被迫开放,由于西方列强的入侵,客观上使上海等地的城市 化开始起步;也因此而带有鲜明的半殖民地特征。
答案:B
读世界发达地区与欠发达地区的城市人口和城市化水平对比图,完成3-4题。
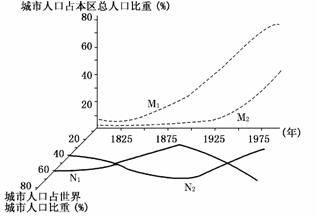
3.依图可知20世纪70年代中期,世界城市人口 ( )
A.总数量开始出现下降趋势
B.发达地区所占比重在增加
C.欠发达地区所占比重在减少
D.两地区所占比重基本持平
解析:由图中水平坐标可知,1975年发达地区城市人口占世界城市人口比重与欠发达地区城市人口占世界城市人口比重大致相等,各占约50%。故选D。
答案:D
4.世界欠发达地区的城市化水平开始快速提升的时期出现在 ( )
A.1825年前后 B.1875年前后
C.1925年前后 D.1950年前后
解析:城市化水平的高低主要看城市人口占本区总人口比重,即分析图中M1和M2曲线的变化。由于M1一直大于M2,故可确定M2代表欠发达地区。图中显示M2从1925年前后城市化水平开始快速提升。故选C。
答案:C
(2007·全国卷Ⅰ)读图,结合所学知识回答1-2题。
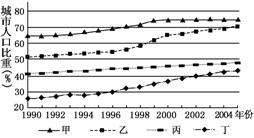
1.能正确反映我国城市化水平变化的曲线是 ( )
A.甲 B.乙 C.丙 D.丁
解析:我国的城市化水平较低,但改革开放后,随着经济的快速发展,我国城市化的发展十分迅速。甲、乙两曲线表示的城市化水平很高,丙曲线表示近十年来,城市化的增长速度十分缓慢,三条曲线都不符合我国的实际情况。
答案:D
2.在图示期间,与美国相比,我国 ( )
A.城市人口数较少 B.城市人口数增长率较低
C.城市人口比重较低 D.城市人口比重增长率较低
解析:与美国相比,我国的城市化水平低,发展快,故B、D两项不正确。我国的城市化水平虽然低,但由于我国的人口基数大,城市总人口居世界第一位,故A项也错误。
答案:C
20.将23.9 g表面已锈蚀成铜绿(Cu2(OH)2CO3)的铜片投入120 mL一定浓度的硝酸中,充分反应后,硝酸被还原成NO2和NO,反应后溶液中H+为0.160 mol。往反应后的溶液中加入过量的NaOH溶液,滤出沉淀,洗涤,干燥后得到29.4 g蓝色固体。求:(1)铜片中单质铜的质量分数;(2)铜片与硝酸充分反应后,溶液中NO3-的物质的量浓度(假设反应前后溶液的体积不变)。
19.某课外小组欲通过实验证明方铅矿分解所得白色粉末中含有氧元素,设计以下的实验装置:
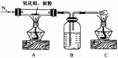
在实验或改进实验中,可能发生的化学反应如下:
PbO+C Pb+CO↑,2 PbO+C
Pb+CO↑,2 PbO+C 2Pb+CO2↑,
2Pb+CO2↑,
Ca(OH)2+CO2=CaCO3↓+H2O
[Cu(NH3)2]Ac+CO+2NH3 [Cu(NH3)4]Ac·CO △H<0。请回答以下问题:
[Cu(NH3)4]Ac·CO △H<0。请回答以下问题:
(1)在装置A中不断鼓入氮气的作用是 ,能否用空气代替氮气? ,其理由是 。
(2)在实验过程中,未见B装置中有白色沉淀生成,说明在装置A中发生反应的化学方程式是 ,证明氧化铅里含有氧元素的实验事实是 。
(3)若使实验更具有说服力,通过增添设备和药品,设计一个更加严密的改进实验方案是 。
(4)若没有木炭粉和氮气,改用氢气行吗? ,实验的装置和药品又将做怎样的调整?____________。
18.已知A、B、C、D、E为中学化学常见物质,A、B、C、D、E中均含有同一种元素,A、C均为气体,E为液体,下图中箭头上的反应物和反应条件均已略去。
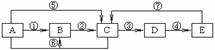
(1)当A与E反应生成B和C时,则A、E共同含有乙元素。生成的C气体易液化。常温常压下D是气体,冰水冷却D时变成无色晶体,此无色晶体的化学式是 。根据所学的氧化还原反应知识判断:在A~E各物质中,在一定条件下能与D发生氧化还原反应的物质有 (填字母)。D溶于纯净的E时,能按物质的量比1:1化合,生成物的化学式可表示为 (写成化合物、复合物或氧化物形式均可)。试描述气体C的物理性质________________________________。
2)当A与E发生化合反应时,能观察到空气中形成大量的白烟,则A、E共同含有甲元素。通过上述描述可知:A的化学式为 ,E的化学式为 。当小心加热A与E化合时的生成物F时,可得到一种无色无味的气体G(G和CO2具有相同的原子数目和电子数目)和一种无色无味的液体H,写出F分解生成的G+H的化学方程式 。
17.试依据下列事实,作出有关的结论。
(1)硅的非金属性特征大于金属特征,而锗的金属特征大于非金属特征,________________________________。(2)金刚石是电的绝缘体,石墨可以导电,而C60可作为制超导体材料,________________________________。
(3)在常温下硅的化学性质不活泼,但自然界中却没有单质硅存在,_____________________________________。
(4)硅酸钠溶液中通入CO2气体时,可生成难溶于水的酸-硅酸,_______________________________________。
(3)碳单质的三种同素异形体:骨架型的金刚石、层型的石墨及球形的球碳分子,试确定那一种物质易在火山喷发口附近发现,_________________________________。
16.氰(CN)2的结构式为N≡C-C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素。(CN)2和水反应可生成HCN和HCNO;(CN)2的氧化性比Br2弱,比I2强。
(1)下列有关反应的化学方程式不正确的是
(填选项标号)。
A.(CN)2和NaOH溶液反应:
(CN)2+2NaOH==NaCN+NaCNO+H2O
B.MnO2和HCN反应:
MnO2+4HCN Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C.向KCN溶液中加入碘水:I2+2KCN==2KI+(CN)2
D.在NaBr和KCN混合溶液中通入少量Cl2:
Cl2+2NaBr==2NaCl+Br2
(2)HCN的电子式为 ,按电子云重叠方式分类分子内化学键类型为_________________,碳原子的杂化类型为____________。
(3)处理含CN-(其中C为+2价)的工业废水常用ClO-氧化,生成的CNO-(其中C 为+4价)元素,反应的离子方程式如下:
aCN-+bClO-+cOH-=dCNO-+eN2↑+fCO32-+bCl-+cH2O
上述化学方程式可能的配平系数有多组,请回答:
①方程式中e : f的值为 (填选项标号)。
A.1 B.1/2 C.2 D.不能确定
②若d=e=1, 则b= 。
15.(1)少量的Mn2+可以催化分解H2O2,其反应的机理可简单解释为:
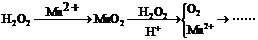
试写出上述2步反应的离子方程式_________________
_______________________________________________。
(2)对于CO中毒、心肌梗塞、冠心病或小儿肺炎等危重患者都要采用吸氧治疗。普通医务室中没有氧气瓶,但一般都有消毒用的30%的H2O2溶液。同时还有可选用的试剂为:KMnO4、HCl、H2SO4、MnO2、Mg、CuSO4、NaCl、葡萄糖。请写出一种使H2O2中氧完全释放出来的理想反应方程式______________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com