
5.在山东曲阜的游玩中,导游在一处名为“杏亭”的景点旁讲解道:“春秋年间,此人在这里大办教育,讲学授课,培养了大批人才。”旅客立刻想到此人的政治主张是( )
A.“天与人不相胜” B.“民贵君轻,社稷次之”
C.“为政以德,爱惜民力” D.“以法治国,中央集权”
4.孟子曾批判某家学说:“是无父也,无父无君,是禽兽也。”司马迁也说它:“使天下法若此,则尊卑无别也。”他们批判的是( )
A. 儒家的“仁政”思想 B.墨家的“兼爱”思想
C.法家的“刑不避大夫”思想 D.荀子的“性恶论”思想
3.下列言论有悖于民本思想的是( )
A.“因民之利而利之”
B.“兼相爱,交相利”
C.“威势之可以禁暴,而德厚之不足以止乱”
D.“君者,舟也,庶人者,水也。水则载舟,水亦覆舟”
2.孔子是我国著名的教育家,对右图《孔子讲学图》的评价不正确的是( )
 A.孔子讲学的教本是四书
A.孔子讲学的教本是四书
B.孔子讲学注意因材施教
C.孔子讲学主张“有教无类”
D.孔子教育学生“学而时习之”
1.战国时期,诸子百家学说最突出的共同点是( )
A.提出社会变革的主张 B.反对掠夺战争
C.主张实行“法治” D.主张放宽刑罚、减轻赋税
26.(10分)反应N2 +3H2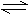 2NH3在固定容积的密闭容器中进行并达到平衡状态,此时,c(N2)=3.5mol/L,c(H2)=11mol/L,c(NH3)=5mol/L。
2NH3在固定容积的密闭容器中进行并达到平衡状态,此时,c(N2)=3.5mol/L,c(H2)=11mol/L,c(NH3)=5mol/L。
求:(1)该温度下,反应的平衡常数是多少?
(2)N2和H2的起始浓度是多少?
(3)N2的转化率是多少?
(4)平衡时的压强与开始时的压强比是多少?

25.(6分)已知下列两个热化学方程式:
H2(g)+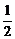 O2(g)===H2O(l) ΔH=-285 kJ/mol
O2(g)===H2O(l) ΔH=-285 kJ/mol
C3H8(g)+5O2(g)==3CO2(g)+4H2O(l) ΔH=-2220.0 kJ/mol
(1)实验测得H2和C3H8的混合气体共5 mol完全燃烧生成液态水时放热6262.5 kJ,则混合气体中H2和C3H8的体积比为 。
(2)已知:H2O(l)==H2O(g) ΔH=+44.0 kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式: 。
24.(9分)(1)盖斯定律的重要用途之一就是间接计算有些反应的反应热.
1 mol气态钠离子和1 mol气态氯离子结合生成1 mol氯化钠晶体所释放的热能为氯化钠晶体的晶格能。
①下列热化学方程式中,能直接表示氯化钠晶体的晶格能的是 。
A.Na+(g)+Cl-(g)=NaCl(s) △H B.Na(s)+1/2Cl2(g)=NaCl(s) △H1
C.Na(s)=Na(g) △H2 D.Na(g)-e-=Na+(g) △H3
E.1/2Cl2(g)=Cl(g) △H4 F.Cl(g)+e-=Cl-(g) △H5
②写出△H1 与 △H、△H2、△H3、△H4、△H5 之间的关系式:
。
(2)在一定条件发生反应:2KClO3+I2==2KIO3+Cl2↑,它属于 (从化合反应、分解反应、置换反应、复分解反应中选择)。有人据此认为碘的非金属性比氯强,你认为对吗?理由是
。
23.(4分)在101 kPa时,1 mol CH4 完全燃烧生成CO2和液态H2O, 放出890.3 kJ的热量,CH4的燃烧热为 。1000 L CH4(标准状况)燃烧后所产生的热量为 。
22.(13分)如图所示,25℃时,在烧杯A中装有50.00 ml蒸馏水,烧杯B 中盛有50.00 ml 0.5mol/L的盐酸,在烧瓶 C 和 D 中充满二氧化氮气体,并用导管将它们连通,把C烧瓶放入A烧杯中,D烧瓶放入B烧杯中。向 A烧杯中加入 50g 硝酸铵晶体,小心搅拌,使其迅速溶解;向B中加入 2g 苛性钠固体,小心搅拌也使其迅速溶解。
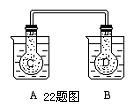
回答下列问题:
(1)烧杯A中温度(填“升高”、“降低”或“不变”,下同) ;烧杯B中温度 。
(2)已知在NO2生成N2O4的可逆反应中,正反应是放热反应,逆反应是吸热反应:
2 NO2(g) N2O4(g)。从上面实验可知C烧瓶中混合气体颜色(填“变浅”、“变深”或“不变”,下同) ;D烧瓶中混合气体颜色
。
N2O4(g)。从上面实验可知C烧瓶中混合气体颜色(填“变浅”、“变深”或“不变”,下同) ;D烧瓶中混合气体颜色
。
(3)若实验测得B烧杯中酸碱中和反应放热1.4325kJ,则NaOH溶液和HCl溶液发生中和反应的热化学方程式为 。
(4)若起始时在D烧瓶中充入mg N2O4,此时测得烧瓶中压强为101kPa,当可逆反应N2O4(g)  2 NO2(g)达到化学平衡状态时压强变为1.515×105Pa,则平衡混合气体的平均相对分子质量为
(精确到小数点后两位)。
2 NO2(g)达到化学平衡状态时压强变为1.515×105Pa,则平衡混合气体的平均相对分子质量为
(精确到小数点后两位)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com