
11.(6分)用金属钠制取Na2O,通常采用2NaNO2+6Na=4Na2O+X↑.
(1)上式中X的分子式为 。
(2)此反应中的氧化剂是____,还原剂是_________,转移电子数是____。
(3)试说明为什么不用钠在O2中燃烧而用此法制Na2O的原因:
知识点三.钠与盐溶液的反应.
10.金属钠着火时,可以灭火的物质是( )
A.水 B.砂子 C.煤油 D.二氧化碳
9.工业上制取钠常用的方法是( )
A.电解海水 B.电解熔融苛性钠 C.用碳还原氧化钠 D.电解熔融氯化钠
8.金属钠的用途有:① 还原某些金属;② 做高压钠灯;③ 制过氧化钠;④与钾混合作原子反应堆的导热剂。其中利用钠的物理性质的是( )
A.①② B.①③ C.②④ D.④
7.(6分)(1)在实验室里,有一钠块浸在煤油里,要取一小粒金属钠做实验,取用的操作方法:_____________________________________________________________
(2)把一小块金属钠暴露在空气中,观察到以下现象,试在横线上写出相应的化学反应方程式。
①金属钠表面逐渐变暗 ;
②过一段时间以后又逐渐变潮湿 ;
③再过些时候又变成白色固体 ;
④又过一段时间白色固体变成白色粉末_____________________________________。
知识点二.钠的用途. 钠的保存.
6.(4分)金属钠在700℃ -800℃时与四氯化钛(TiCl4)反应制取金属钛,该反应的化学方程式为 ____________________。该反应必须在隔绝空气的条件下进行,原因是_________________________________________
5.(6分) 将一小块钠投入一盛有水的烧杯中,发生下列现象,请说明原因:
①钠浮在水面上________________________;
②钠与水剧烈反应并熔成一个闪亮的小球_______________________;
③小球在水面上四处游动_______________________________;
④反应后在溶液中加几滴酚酞溶液,溶液变红__________________________;
⑤写出钠与水反应离子方程式______________________
4.取一小粒金属钠放在燃烧匙里加热,实验现象有下列叙述:
①金属钠先熔化 ②在空气中燃烧,产生紫色火焰 ③燃烧后生成白色固体④燃烧时火焰为黄色⑤燃烧后生成淡黄色固体。其中描述正确的是( )
A.①② B.①②③ C.①④⑤ D.④⑤
2.钠的下列化合物在自然界不存在的是( )
A.氯化物 B.氧化物 C.硫酸盐 D.碳酸盐
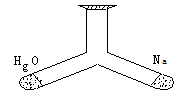 3.已知HgO不稳定,受热极易分解,生成单质汞和氧气。
3.已知HgO不稳定,受热极易分解,生成单质汞和氧气。
如图所示的装置中,一边装有2.3g金属钠,另一边装
有HgO,同时加热容器的两端,若加热后空气的成分不
变,那么装入容器中的HgO质量是( )
A.21.7g B.24g C.43.4g D.10.85g
1.关于钠原子和钠离子,下列叙述错误的是 ( )
A.它们相差一个电子层 B.它们的化学性质相似
C.钠原子半径比钠离子大 D.钠原子、钠离子均为同一元素
知识点一.钠的化学性质.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com