
10. (09上海卷
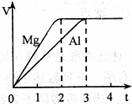
(09上海卷 15)镁和铝分别与等浓度、等体积的过量稀硫酸 反应,产生
15)镁和铝分别与等浓度、等体积的过量稀硫酸 反应,产生 气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
 A.物质的量之比为3:2
B.质量之比为3:2
A.物质的量之比为3:2
B.质量之比为3:2
 C.摩尔质量之比为2:3
D.反应速率之比为2:3
C.摩尔质量之比为2:3
D.反应速率之比为2:3
答案:A
9. (09四川卷11)向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
 A.
A.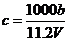 B.
B.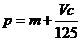 C.n=m+17Vc D.
C.n=m+17Vc D.
 <
< 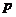 <
<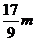
答案:C
8. (09江苏卷
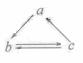 3)下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
3)下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
|
|
a |
b |
c |
|
A |
Al |
AlCl3 |
Al(OH)3 |
|
B |
HNO3 |
NO |
NO2 |
|
C |
Si |
SiO2 |
H2SiO3 |
|
D |
CH2=CH2 |
CH3CH2OH |
CH3CHO |
答案:B
7. (09全国卷Ⅰ8)下列表示溶液中发生反应的化学方程式错误的是
A.
B.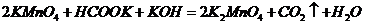
C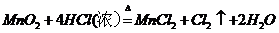
D.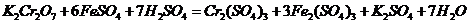
答案:B
解析:在碱性条件下,不可能产生CO2气体,而应是CO32 -,故B项错。
6. (08年江苏化学·13)研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
A.密闭容器中CuO和C高温反应的气体产物: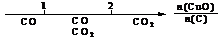
B.Fe在Cl2中的燃烧产物: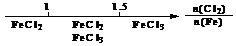
C.AlCl3溶液中滴加NaOH后铝的存在形式: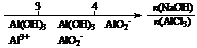
D.氨水与SO2反应后溶液中的铵盐: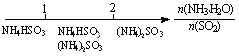
答案:B
5. (08年广东化学·6)相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是
A.Al B.Al(OH)3 C.Al Cl3 D.Al2O3
 答案:A
答案:A
4. (08年广东文基·64)铁和铁合金是生活中常用的材料,下列说法正确的是
A.不锈钢是铁合金,只含金属元素
B.一定条件下,铁粉可与水蒸气反应
C.铁与盐酸反应,铁合金不与盐酸反应
D.在空气中,铁板比镀锌铁板更耐腐蚀
答案:B
3. (2007年高考上海化学卷,铝)用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是 ( )
A.实验中发生的反应都是氧化还原反应
B.铝是一种较活泼的金属
C.铝与氧气反应放出大量的热量
D.铝片上生成的白毛是氧化铝和氧化汞的混合物
答案 :D
(1)抓价态:从铁元素三种价态的相互转化(铁三角关系)去认识铁及其化合物间的氧化-还原反应规律.
(2)想属类:如铁是一种比较活泼的过渡金属,氧化亚铁、氧化铁为碱性氧化物,氢氧化亚铁、氢氧化铁为不溶性弱碱,氯化铁为强酸弱碱盐,由此去分析理解它们各自所具有的性质.
Fe2+和Fe3+的检验
(1)Fe2+的检验:
方法一:滴加KSCN溶液,无明显现象,再滴加新制氯水,溶液立即变红色
方法二:滴加NaOH溶液,生成白色絮状沉淀,该沉淀迅速变为灰绿色,最后变为红褐色。
(2)Fe3+的检验:
方法一:滴加KSCN溶液或NH4SCN溶液,溶液立即变为血红色
方法二:滴加NaOH溶液,出现红褐色沉淀

击破考点一:金属的性质与结构
例1:金属的下列性质中与金属金属晶体结构无关的是 ( )
 A.导电性 B.化学反应中易失去电子
A.导电性 B.化学反应中易失去电子
C.延展性 D.硬度
答案:B
解析:金属的物理性质主要受金属结构的影响;金属的化学性质主要受金属原子的结构影响。
[变式训练1]有关合金的叙述不正确的是 ( )
A.合金的熔点比它的各成份金属的熔点低
B.合金的硬度和强度一般比纯金属高
C.合金一定是金属熔合而成的物质
D.硬铝、黄铜和钢均为合金
答案:C
击破考点二:镁、铝的性质及计算
例2:某化学兴趣小组用回收的镁铝合金制取氢气。现有l0.8 g镁铝合金,下列说法正确的是( )
A.常温下与足量18mol/LH2SO4溶液反应,最多可放出0.6 mol H2
B.常温下与足量2mol/LHNO3溶液反应,最少可放出0.45 mol H2
C.常温下与足量2 mol/L H2SO4溶液反应,放出H2的物质的量在0.45 mol-0.6 mol之间
D.常温下与足量2mol/LNaOH溶液反应,放出H2的物质的量在0-0.6 mol之间
答案:CD
解析:本题考查镁铝的性质。镁与浓硫酸反应生成SO2,铝与浓硫酸钝化,A项错误;镁铝与稀硝酸反应生成NO,B项错误;当10.8g合金完全是镁,产生氢气0.45mol,当10.8g合金完全是铝,产生氢气0.6mol,C项正确;当10.8g合金完全是镁,不产生氢气,当10.8g合金完全是铝,产生氢气0.6mol,D项正确。
[变式训练2]等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是( )
A.2mol.L-1H2SO4溶液 B.18 mol.L-1H2SO4溶液
C.6 mol.L-1KOH溶液 D.3 mol.L-1HNO3溶液
答案:A
解析:镁铝都可与稀硫酸反应放出氢气,但与浓硫酸,铝在常温下发生钝化,镁虽反应但不产生氢气。与氢氧化钾只有铝反应。与硝酸反应,硝酸为强氧化性酸,都不会产生氢气。
 [变式训练3]用铝箔包裹2.3 g金属钠,用针扎出一些小孔,放入水中,完全反应后,用排水集气法收集产生的气体,则收集到的气体为
( )
[变式训练3]用铝箔包裹2.3 g金属钠,用针扎出一些小孔,放入水中,完全反应后,用排水集气法收集产生的气体,则收集到的气体为
( )
A.O2和H2的混合气体 B.0.1g H2 C.大于0.1g H2 D.小于0.1g H2
答案:C
解析:本题涉及到根据化学反应方程式进行计算问题。根据反应方程式2Na+2H2O==2NaOH+H2↑可知,2.3g金属钠与水作用可产生0.1g
H2,而Al还会和反应生成的NaOH作用2Al+2NaOH+2H2O==2NaAlO2+3H2↑,进一步产生H2,故收集到的H2总量要大于0.1g
击破考点三:镁、铝化合物的考查
例3:下列有关金属铝及其化合物的叙述正确的是 ( )
A.铝在常温下不能与氧气反应
B.铝不能与氯气反应
C.铝既能溶于酸,又能溶于碱
D.氧化铝只能与酸反应,不能与碱反应
答案:C
解析:铝为活泼金属,常温下能与O2反应生成致密的氧化膜;加热条件下与Cl2激烈反应;铝、氧化铝既能与酸又能与碱反应。
[变式训练4]下列溶液能与镁反应生成氢气的是 ( )
A.氯化铵溶液 B.氢氧化钠溶液
C.碳酸钾溶液 D.饱和石灰水
答案:A
解析:氯化铵溶液水解呈酸性,所以答案为A.
[变式训练5]将100mL0.6mol/LAlCl3溶液跟0.4mol/LNaOH溶液混合后,得到3.9g氢氧化铝沉淀,此时消耗氢氧化钠的体积是 ( )
A.250mL B.375mL C.475mL D.500mL
答案:BC
解析:得到3.9g氢氧化铝沉淀可能有两种情况,①氢氧化钠量不足,只发生反应:Al3++3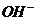 =Al(OH)3 ↓,则V(NaOH)=375mL; ②氢氧化钠过量,与生成的氢氧化铝继续反应,发生的反应为:Al3++3
=Al(OH)3 ↓,则V(NaOH)=375mL; ②氢氧化钠过量,与生成的氢氧化铝继续反应,发生的反应为:Al3++3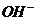 =Al(OH)3 ↓ , Al(OH)3+
=Al(OH)3 ↓ , Al(OH)3+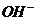 =
=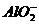 +2H2O,则V(NaOH)=475mL
+2H2O,则V(NaOH)=475mL
击破考点四:考查Fe2+与Fe3+的性质
例4:将过氧化钠投入到氯化亚铁溶液中,可以观察到的现象是 ( )
①生成白色沉淀②生成红裼色沉淀③有气泡产生④溶液变成棕黄色
A.①③ B.①④ C.②③ D.②④
 答案:C
答案:C
[变式训练6]浅绿色的硝酸亚铁溶液中存在如下平衡:Fe2++2H2O Fe(OH)2++2H+,若向该溶液中滴加足量的盐酸,则溶液的颜色
( )
Fe(OH)2++2H+,若向该溶液中滴加足量的盐酸,则溶液的颜色
( )
A.变黄色 B.绿色变深 C.绿色变浅 D.无变化
答案:A
[变式训练7]在氧化铁、氯化铜和盐酸混合溶液中加入铁粉,待反应结束,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是 ( )
A.Cu2+ B.Fe3+ C.Fe2+ D.H+
答案:C
击破考点五:氢氧化铝的两性及“铝三角”之间的转化
例5:某无色溶液里,只含有下列八种离子中的某几种:Mg2+、Na+、H+、Ag+、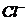 、
、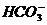 、
、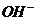 、
、 。已知该溶液能跟金属铝反应, 且放出的气体只有氢气试回答:
。已知该溶液能跟金属铝反应, 且放出的气体只有氢气试回答:
(1)若溶液跟Al反应后有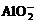 生成, 则原溶液一定含有大量的
离子, 还可能含有大量的
离子。
生成, 则原溶液一定含有大量的
离子, 还可能含有大量的
离子。
(2)若溶液跟Al反应后有Al3+生成, 则原溶液中一定不含有大量 离子
答案:(1)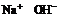
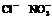 (2)
(2)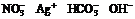
解析:(1)本题考查的基础知识
①单质Al既能与强碱反应又能与强酸(非氧化性酸)皆有H2生成 ②离子共存问题(离子能共存即离子间没有反应发生)
(2)溶液跟Al反应有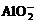 生成。
生成。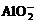 只存在于碱性溶液中, 上述八种离子组成强碱只能为NaOH
只存在于碱性溶液中, 上述八种离子组成强碱只能为NaOH 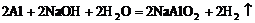 , ∴原溶液中一定含有大量
, ∴原溶液中一定含有大量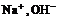 。有OH-存在,
。有OH-存在, 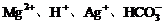 这些离子不能存在, 所以还可能存在离子。
这些离子不能存在, 所以还可能存在离子。
(3)若溶液跟Al反应有Al3+生成。Al3+只存在酸性溶液中, 上述八种离子组成强酸只能为Hcl, HNO3, 但Al与HNO3反应不出H2, 只能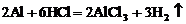 所以原溶液中肯定含有H+, Cl-与H+, Cl-不共存的为
所以原溶液中肯定含有H+, Cl-与H+, Cl-不共存的为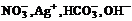 。
。
[变式训练8]粉末状试样A是一种含有少量某钾盐(白色或无色)和一种活泼金属组成的混合物。进行如下实验:
①将A和适量CuO粉末混合均匀,放在一置于三角架的石棉网上,用酒精灯加强热,可看到混合物迅猛燃烧,白光耀眼。完全反应后得到混合物B。
②向冷却的混合物B中加入稀盐酸至沉淀不再溶解,恰好用去HCl 0.6mol,得到溶液C。(设溶液体积为1000mL)和沉淀D,然后过滤。
③将溶液C加强热、蒸干、灼烧,得到固体E,且E的质量和A的质量恰好相等。
④如果向溶液C中逐滴加入NaOH溶液,则会出现白色沉淀且逐渐增多,继续滴加NaOH溶液白色沉淀又会逐渐减少,最后完全消失。请填空:
(1)写出①中可能的三个反应的化学方程式 ; ; 。
(2)A中金属的质量为 ;所含钾盐的物质的量为 。
(3)写出④中先后反应的离子方程式 , 。
答案:1)2KClO3
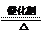 2KCl+3O2↑;2Al+3CuO
2KCl+3O2↑;2Al+3CuO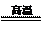 Al2O3+3Cu;4Al+3O2
Al2O3+3Cu;4Al+3O2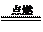 2Al2O3;
2Al2O3;
 (2)5.4g;0.1mol;
(2)5.4g;0.1mol;
(3)Al3++3OH- = Al(OH)3↓;Al(OH)3+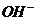 =
=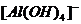
击破考点六:考查氢氧化亚铁的制备方法
例6:用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入 。
(2)除去蒸馏水中溶解的O2常采用 的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是 。
方法二:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备
(1)在试管Ⅰ里加入的试剂是 。
(2)在试管Ⅱ里加入的试剂是 。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂, 打开
止水夹,塞紧塞子后的实验步骤是 。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由
是 。
答案:方法一(1)稀H2SO4、铁屑
(2)煮沸
(3)避免生成的Fe(OH)2沉淀接触O2
方法二(1)稀H2SO4、铁屑
(2)NaOH溶液
(3)检验试管Ⅱ出口处排出的氢气的纯度。当排出的H2纯净时,再夹紧止水夹
(4)试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,且外界空气不容易进入
击破考点七:考查铁的化合物及其计算
例7.在由Fe、FeO和Fe2O3组成的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,并放出448mL气体(S.P.T),此时溶液中无Fe3+。则下列判断正确的是 ( )
 A.混合物中三种物质反应时消耗盐酸的物质的量之比为1:1:3
A.混合物中三种物质反应时消耗盐酸的物质的量之比为1:1:3
B.反应后所得溶液中的Fe2+和Cl-的物质的量之比为1:3
C.混合物中,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多
D.混合物中,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多
答案:C
[变式训练9]现有两种金属的混合物共4克,与足量氯气反应后,固体增重7.1克。另取4克该金属混合物,投入到足量盐酸中,产生2.24L(S.T.P)H2.则该混合物的组成不可能是 ( )
A.Cu,Al B.Mg,Fe C.Zn,Al D.Mg,Zn
答案:AB
击破考点八:铝铁及其化合物
例8:将a克Fe2O3、Al2O3样品溶解在过量的200mL Ph=1的硫酸溶液中,然后向其中加入NaOH 溶液使Fe3+、Al3+刚好完全沉淀,用去NaOH 溶液100 mL,则NaOH 溶液的浓度为( )
A.0.1 mol.L-1 B.0.2 mol.L-1
C.0.4 mol.L-1 D.0.8 mol.L-1
答案:B
解析:由题意及氧化物、氢氧化铝的两性可知,要使Fe3+、Al3+刚好完全沉淀,则须使溶液中的氢离子和氢氧根离子量相等
由题目中反应式可知,溶解1 mol Fe2O3所消耗的氢离子数与沉淀2 mol Fe3+所消耗的氢氧根离子数相等。同理,Al2O3也如此。故只要控制酸中的氢离子数与碱中所含氢氧根离子数相等即可使Fe3+、Al3+刚好完全沉淀。
[变式训练10]向a L物质的量浓度为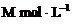 的明矾
的明矾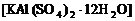 溶液中逐滴加入b L物质的量浓度为
溶液中逐滴加入b L物质的量浓度为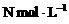 的
的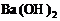 溶液时,①当b满足________时,沉淀的总物质的量为最大值;当b满足________时,沉淀的总质量为最大值。②当
溶液时,①当b满足________时,沉淀的总物质的量为最大值;当b满足________时,沉淀的总质量为最大值。②当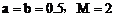 ,
,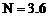 时,生成沉淀的质量为多少克?
时,生成沉淀的质量为多少克?
解析:①根据化学方程式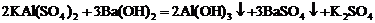 和
和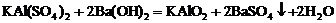 可知:向明矾中加
可知:向明矾中加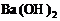 ,当
,当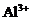 沉淀完全时,生成沉淀的物质的量最大,此时
沉淀完全时,生成沉淀的物质的量最大,此时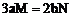 ,则
,则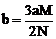 ;当
;当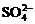 沉淀完全时,沉淀质量最大,此时
沉淀完全时,沉淀质量最大,此时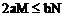 ,即
,即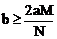 。
。
②根据IV中公式②可得:

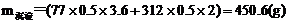
击破考点九:铁铜及其化合物
例9:把铜粉和过量的铁粉加入到热的浓硝酸中,充分反应后,溶液中大量存在的金属阳离子是 ( )
A.只有Fe2+ B.只有Fe3+
C.有Fe2+和Cu2+ D.有Fe3+和Cu2+
答案:A
解析:浓硝酸具有强氧化性,热的浓硝酸可将Fe和Cu分别氧化成Fe3+和Cu2+,过量的铁又与Fe3+和Cu2+反应生成Fe2+和Cu,所以充分后,溶液中大量存在的金属阳离子为Fe2+,故选A
[变式训练11]在铁与铜的混和物中,加入一定量的稀硝酸,充分反应后剩余金属m1g,再向其中加入一定量的稀硫酸,充分振荡后,剩余金属m2g,m1与m2的关系是
A. m1一定大于m2 B. m1可能等于m2
C. m1一定等于m2 D. m1可能大于m2
答案:A
[变式训练12]将6g纯铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中充分反应后得到200mL0.5mol/L的FeSO4溶液和5.2g固体,求:
(1)反应后生成铜多少克?
(2)加入铁粉前Fe2(SO4)3物质的量浓度
答案:发生反应的化学方程式为:
①Fe+Fe2(SO4)3=3FeSO4 ②Fe+CuSO4=Cu+FeSO4
两个反应共生成FeSO4为:0.2L×0.5mol/L=0.1mol
观察两个反应不难发现,若生成同样的FeSO4,②式消耗的铁更多。假设0.1molFeSO4全部为②式产生,则此时消耗的铁将达最大量为a。
Fe - FeSO4
1mol 1mol
a 0.1mol
a=0.1mol,即铁为5.6g,则5.2g固体中含Cu也含剩余的Fe,设原溶液的Fe2(SO4)3和CuSO4的物质的量分别为x和y。
Fe+Fe2(SO4)3=3FeSO4 Fe+CuSO4=Cu+FeSO4
X x 3x y y y y
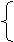 由题意得 3x+y=0.1mol
由题意得 3x+y=0.1mol
 6g-56g/mol×(x+y)+64g/mol×y=5.2g
6g-56g/mol×(x+y)+64g/mol×y=5.2g
解得:x=0.02mol y=0.04mol
则生成铜:0.04mol×64g/mol=2.56g
原Fe2(SO4)3和物质的量浓度为0.02mol/0.2L=0.1mol/L
击破考点十:有关图像问题的考查
例10:向MgSO4和Al2(SO4)3的混合溶液中, 逐滴加入NaOH溶液。下列图象中能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积, 纵坐标表示反应生成沉淀的质量)
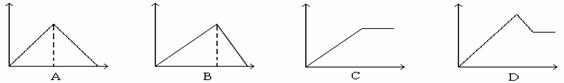
答案:D
解析: Al(OH)3能溶于过量的NaOH溶液,但是Mg(OH)2不溶,因此反应最终的沉淀不为“O”,据此断定A、B皆错。混合液在与NaOH溶液反应过程中,一定有沉淀减少过程[Al(OH)3溶于NaOH溶液中],最终只有Mg(OH)2,所以C错误D正确
[变式训练13]准确称取6克铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100ml某浓度的硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10ml的NaOH溶液,产生的沉淀的质量m与加入NaOH溶液的体积V的关系如图所示。请填空回答:


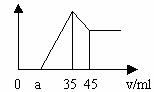
(1)H2SO4溶液的物质的量浓度为 ;
(2)a=2.3,用于沉淀铁离子,消耗氢氧化钠溶液的体积是
答案:(1)1.75mol/L (2)2.7ml.
解析:(1)由图像可知当加入35mlNaOH溶液时,滤液中过量的硫酸被中和,
且Fe3+、Al3+全部沉淀,用整体法分析反应的过程,消耗H+的物质的量等
于OH+的物质的量,得硫酸的物质的量浓度为:=1.75(mol/L)
(2)用隔离法考查:从溶解Al(OH)3消耗,推知用于Al3+沉淀所消耗的NaOH溶液30ml,则
沉淀Fe3+所消耗的NaOH溶液为:35-30-2.3=2.7ml


1.(2007年高考广东理基,铝)下列有关金属铝及其化合物的叙述正确的是 ( )
A.铝在常温下不能与氧气反应
B.铝不能与氯气反应
C.铝既能溶于酸,又能溶于碱
D.氧化铝只能与酸反应,不能与碱反应
答案: C
2. (2007年高考海南化学卷,镁)下列溶液能与镁反应生成氢气的是 ( )
A.氯化铵溶液 B.氢氧化钠溶液 C.碳酸钾溶液 D.饱和石灰水
答案 :A
I. 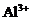 与NaOH反应生成沉淀的质量
与NaOH反应生成沉淀的质量
①当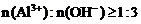 时,
时,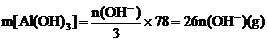 。
。
②当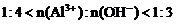 时,
时,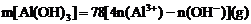 。
。
③当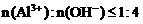 时,
时,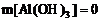 。
。
 II.
II. 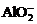 与强酸(
与强酸(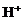 )反应生成沉淀的质量
)反应生成沉淀的质量
①当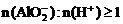 时,
时,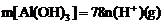 。
。
②当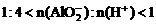 时,
时,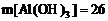
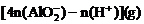 。
。
③当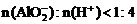 时,
时,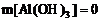 。
。
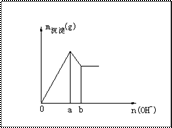 III.
III. 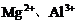 的混合溶液与
的混合溶液与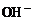 反应时,求
反应时,求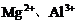 的物质的量。
的物质的量。
若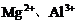 与
与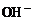 的反应关系如下图,则
的反应关系如下图,则
①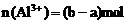
②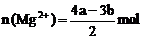
IV. 明矾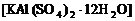 溶液与
溶液与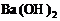 溶液反应生成沉淀的质量。
溶液反应生成沉淀的质量。
①当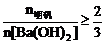 时,
时,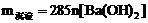 ;
;
②当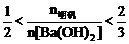 时,
时,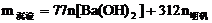 ;
;
③当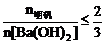 时,
时,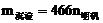 。
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com