
13.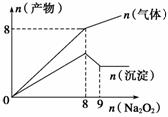 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+ 的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH4+的物质的量分别为
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+ 的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH4+的物质的量分别为
A. 2 mol、3 mol、4 mol
B.3 mol、2 mol、8 mol
C. 2 mol、3 mol、8 mol
D.3 mol、2 mol、4 mol
12.在反应KClO3+6HCl==3Cl2↑+KCl+3H2O中,被还原的氯原子和被氧化的氯原子的个数之比为
A.6∶1 B.1∶6 C.5∶1 D.1∶5
11. 能正确表示下列反应的离子方程式是
A.将铜屑加入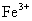 溶液中:
溶液中:
B.将磁性氧化铁溶于盐酸: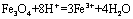
C.将氯化亚铁溶液和稀硝酸混合: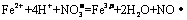
D.将铁粉加入稀硫酸中: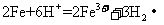
10. 0.1 mol/L Na2SO4溶液300 mL、0.1 mol/LMgSO4溶液200 mL和0.1 mol/L Al2(SO4)3溶液100 mL,这三种溶液中硫酸根离子浓度之比是
A.1∶1∶1 B.3∶2∶1 C.3∶2∶3 D.1∶1∶3
9.设NA为阿伏加德罗常数,下列叙述正确的是
A.24 g镁的原子最外层电子数为NA B.1 L 0.1 mol/L乙酸溶液中H+数为0.1NA
C.1 mol甲烷分子所含质子数为10NA D.标准状况下,22.4 L乙醇的分子数为NA
8. 用48 mL 0.1 mol/L的FeSO4溶液,恰好还原2.4×10-3mol [RO(OH)2]+,则R元素的最终价态为
A.+2 B.+3 C.+4 D.+5
7.在一定条件下,分别以过氧化氢、高锰酸钾、氯酸钾为原料制取氧气,当制得相同物质的量的氧气时,三个反应中转移电子数的物质的量之比为
A.1∶2∶3 B.2∶4∶3 C.1∶2∶2 D.1∶1∶1
6.已知在酸性条件下有以下反应:①KBrO3能将I-氧化为KIO3,本身被还原为Br2;②Br2能将I-氧化为I2;③KIO3能将I-氧化为I2,也能将Br-氧化为Br2,本身被还原为I2。向KBrO3溶液中滴加少量KI的硫酸溶液后,所得产物除水外还有
A.Br-、I2 B.Br2、Br-、I2 C.Br2、I2、IO3- D.Br2、IO3-
5.制备氰氨基化钙的化学方程式为CaCO3+2HCN == CaCN2+CO↑+H2↑+CO2↑,在反应中
A.氢元素被氧化,碳元素被还原 B.HCN是氧化剂,CaCO3是还原剂
2是氧化产物,H2是还原产物 D.CO为氧化产物,H2为还原产物
4.从海水中提取单质镁,下列正确的途径是
A.海水Mg(OH)2Mg B.海水MgCl2Mg
C.海水Mg(OH)2MgCl2Mg D.海水MgCl2Mg
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com