
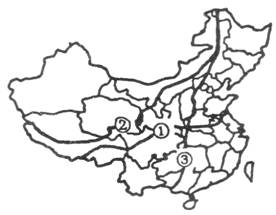
3.下图①、②、③为几条重要的地理界线,关于界线①、②、③的说法正确的是
 A.①为内外流域界线,③为森林与草场界线
A.①为内外流域界线,③为森林与草场界线
B.②为季风区与非季风区的界线,③为第二、三级阶梯(地形)界线
C.②为农区与牧区界线,③为东、中部经济带界线
D.②为400毫米年降水量界线,③为农牧业界线
2.下列省区中,分别位于西部、中部、东部经济地带的是
A.甘肃、山西、山东 B.西藏、陕西、江苏
C.青海、四川、广东 D.内蒙古、安徽、福建。
1.下列少数民族自治区中,既位于我国东部经济地带又属于西部大开发范围的是:
A.内蒙古自治区 B.广西自治区 C.新疆维吾尔自治区 D.宁夏回族自治区
14.(13分)(2009·福建高考)某研究性学习小组借助A-D的仪器装置完成有关实验.
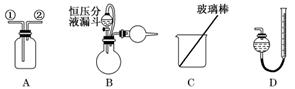
[实验一]收集NO气体
(1)用装置A收集NO气体,正确的操作是___________________________(填序号).
a.从①口进气,用排水法集气
b.从①口进气,用排气法集气
c.从②口进气,用排水法集气
d.从②口进气,用排气法集气
[实验二]为了探究镀锌薄铁板上锌的质量分数w(Zn)和镀层厚度,查询得知锌易溶于强
碱:Zn+2NaOH===Na2ZnO2+H2↑.据此,截取面积为S的双面镀锌薄铁板试样,剪
碎、称得质量为m1g.用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验.
方案甲:通过测量试样与碱反应生成的氢气体积来实现探究目标.
(2)选用B和________(填仪器标号)两个装置进行实验.
(3)测得充分反应后生成氢气的体积为V L(标准状况),w(Zn)=________.
(4)计算镀层厚度,还需知道的一个物理量是_______________________________.
(5)若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将__________(填“偏大”、
“偏小”、或“无影响”).
方案乙:通过称量试样与碱反应前后的质量实现探究目标.选用仪器C做实验,试样
经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2 g.
(6)w(Zn)=________.
方案丙:通过称量试样与碱反应前后仪器、试样和试剂的总质量(其差值即为H2的质量)
实现探究目标.实验同样使用仪器C.
(7)从实验误差角度分析,方案丙________方案乙(填“优于”、“劣于”或“等同于”).
解析:(1)NO与O2反应,不能用排气法集气;排水法集气则应遵循“短管进长管出”
的原则,故选c.
(2)题目所给量气装置只有D.
(3)由关系式:Zn-H2可知:m(Zn)= g,则:
w(Zn)=m(Zn)/m1=.
(4)m=ρV,V=Sh可推知答案.
(5)用恒压分液漏斗时,部分气体会扩散到橡胶管及分液漏斗上部,若改用普通分液漏
斗,则不存在此种情况,故改用普通分液漏斗后测得H2的体积偏大,则测量结果将偏
大.
(6)m(Zn)=m1-m2,则w(Zn)=.
(7)方案丙中产生H2的量较小,测量误差较大,故方案丙劣于方案乙.
答案:(1)c (2)D
(3)
(4)金属锌的密度(或其他合理答案)
(5)偏大
(6)(或其他合理答案)
(7)劣于
13.(17分)(1)有如下图所示A、B、C三种仪器:请选择下列仪器名称的序号,填入相应的空格内:
①烧杯 ②普通漏斗 ③圆底烧瓶 ④锥形瓶 ⑤分液漏斗
A________,B________,C________
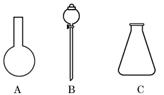
(2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,该
同学在操作时的一个错误是____________________________________,烧杯的实际质
量为________ g.
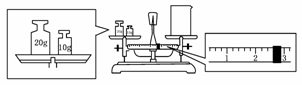
(3)指出下面三个实验中各存在的一个错误:
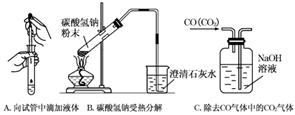
A________________________________________________________________________,
B________________________________________________________________________,
C________________________________________________________________________.
解析:(1)根据常见仪器的形状可判断三处仪器的名称.
(2)根据天平称量的要求“左物右码”,该同学将物品与砝码放反了,但仍然满足:左盘质量=右盘质量+游码质量,因此烧杯的实际质量为30-2.6=27.4(g).
(3)A中滴加液体时滴管不能伸入试管内;B项试管口应向下倾斜,否则很容易引起试管炸裂;C项应换为长进短出,否则CO会把NaOH溶液排到瓶外.
答案:(1)③ ⑤ ④
(2)砝码和物品的位置放反了 27.4
(3)A:胶头滴管伸入试管内了
B:试管口向上倾斜
 C:进气管和出气管反了(或混合气体从短管进入洗气瓶)
C:进气管和出气管反了(或混合气体从短管进入洗气瓶)
12.(11分)(1)玻璃棒是中学化学实验中常用的仪器.下列实验过程中,一般不需要用玻璃棒的是________(填写编号).
①用pH试纸测定Na2CO3溶液的pH
②配制一定物质的量浓度的氯化钠溶液
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
④探究Ba(OH)2·8H2O晶体和NH4Cl晶体反应过程中的能量变化
⑤实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
(2)用“大于”、“小于”或“等于”填空:
①读取量筒中液体的体积时,视线偏高,读取的体积数________实际体积数.
②用托盘天平称取10.4 g食盐,将砝码和食盐的位置颠倒,所称取食盐的质量________10.4 g.
③配制500 mL 0.1 mol/L NaOH溶液,定容时俯视刻度线,所得溶液的物质的量浓度__________0.1 mol/L.
④用中和滴定法测某NaOH溶液的浓度,量取待测液时未用该溶液润洗滴定管,测得的溶液浓度________实际浓度.
解析:(1)①中要用玻璃棒蘸取待测液,②中玻璃棒起到搅拌、引流作用,④中玻璃棒起到搅拌作用.
答案:(1)③⑤ (2)①大于 ②小于 ③大于 ④小于
11.(9分)现有下列仪器和药品:①铁架台(含铁圈、铁夹),②锥形瓶,③酸式与碱式滴定管,④烧杯,⑤玻璃棒,⑥胶头滴管,⑦天平(砝码),⑧滤纸,⑨量筒,⑩过滤漏斗,⑪NaOH固体,⑫标准NaOH溶液,⑬未知浓度HCl,⑭蒸馏水,⑮Na2CO3溶液.
(1)过滤时,应选用的上述仪器是__________.
(2)配制一定物质的量浓度的溶液时,还缺少的仪器是__________.
(3)做酸碱中和滴定时,还缺少的试剂是__________.
(4)进行中和滴定时,事先不应该用所盛溶液润洗的仪器是________.
A.酸式滴定管 B.碱式滴定管
C.50 mL量筒 D.锥形瓶
解析:本题考查实验基本操作.
(1)熟记过滤器的组成,要用到①④⑤⑧⑩.
(2)熟记配制溶液的步骤及所用的仪器,就可知道缺少的仪器是容量瓶.
(3)中和滴定没有指示剂不能判断终点.
(4)中和滴定时要润洗滴定管.
答案:(1)①④⑤⑧⑩ (2)容量瓶 (3)指示剂
(4)C、D
10.以下各种尾气吸收装置中,适合于吸收易溶性气体,而且能防止倒吸的是 ( )
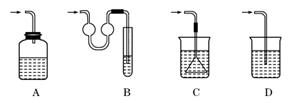
解析:防止倒吸的装置要求容器的容量较大,才能容纳可能吸入的液体.A中只有进气管没有出气管,且导气管没接近液面不利于气体的吸收;C中虽有倒置漏斗,但因其全部浸没在液体中未能发挥作用,应该将其边缘贴在液面上;D极易产生倒吸.
答案:B
9.下列实验操作完全正确的是 ( )
|
编号 |
实验 |
操作 |
|
A |
钠与水的反应 |
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
|
B |
配制一定浓度的氯化钾溶液1000 mL |
准确称取氯化钾固体,放入到1 000 mL的容量瓶中,加水溶解,振荡摇匀,定容 |
|
C |
排除碱式滴定管尖嘴部分的气泡 |
将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
|
D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
解析:A项钠与水反应的实验操作是将切下的绿豆大小的钠,吸去表面煤油小心放入装有一半水的小烧杯中;B项配制一定浓度的KCl溶液1000 mL时,溶解KCl应在烧杯中进行;D项取出分液漏斗中所需的上层液体应该是先将下层液体从分液漏斗下端管口放出,关闭活塞,然后换一个接收容器,将上层液体从分液漏斗上口倒出.
答案:C
8.下列装置或操作能达到实验目的的是 ( )
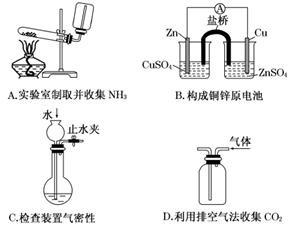
解析:实验室制取并收集NH3,收集装置中用塞子将瓶口塞住,NH3无法进入集气瓶,瓶内空气无法排出,A错误;Zn放入CuSO4溶液中,置换出的Cu附着在Zn表面,无法形成原电池,B错误;检查装置气密性,可以做成封闭体系,观察液面差能否稳定存在,推断装置气密性是否良好,C正确;因CO2密度大于空气,应长管进短管出,D错误.
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com