
1.某学校打算开辟一块食用菌栽培基地,以丰富学生的劳动技术课内容。首先对食用菌实验室进行清扫和消毒处理,准备食用菌栽培所需的各种原料和用具,然后从菌种站购来各种食用菌菌种。请回答下列问题:
(1)对买回来的菌种进行扩大培养,首先制备试管培养基,写出制备固体牛肉膏蛋白胨培养基所需的原料: 、
、 、 、 。其中提供氮源的是 ;提供能源的主要物质是 。
(2)微生物在生长过程中对各种成分所需量不同,配制培养基时各成分要有合适的 。在烧杯中加入琼脂后要不停地 ,防止 。
(3)将配制好的培养基分装到试管中,加棉塞后若干个试管一捆,包上牛皮纸并用皮筋勒紧放入 中灭菌,压力 kPa,温度 ,时间 。灭菌完毕后拔掉电源,待锅内压力自然降到0时,将试管取出。如果棉塞上沾有培养基,此试管应 。
(4)使用高压蒸汽灭菌锅时注意,先向锅内倒入 ,把锅内水加热煮沸并将其中原有冷空气彻底排出后将锅密闭。
(5)从一支试管向另一支试管接种时注意,接种环要用酒精灯 (“内”或“外”)焰灭菌,并且待接种环 后
蘸取菌种,试管口不能离开酒精灯火焰附近,将接种的试管放入 ℃冰箱中保藏。
答案 (1)牛肉膏 蛋白胨 水 无机盐 琼脂 蛋白胨、牛肉膏 牛肉膏 (2)比例 搅拌 琼脂糊底引起烧杯破裂
(3)高压蒸汽灭菌锅 100 121℃ 15-30 min 废弃 (4)适量水 (5)外 冷却 4
1.(08枣庄三诊)氮是地球上含量丰富的一种元素,氮及其化合拖把在工农业生产、生活中有着重要作用。请回答:
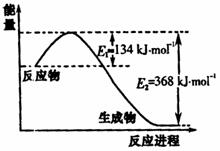 (1)右图是1molNO2和1molCO反应
(1)右图是1molNO2和1molCO反应
生成CO2和NO过程中能量变化
示意图,请写出NO2和CO反应
的热化学方程式
。
(2)在一定体积的密闭容器中,进行如
下化学反应:
 N2(g)+3H2(g) 2NH3(g),其化学
N2(g)+3H2(g) 2NH3(g),其化学
平衡常数K与温度t的关系如下表:
|
t/K |
298 |
398 |
498 |
… |
|
K/(mol·L-1)2 |
4.1×106 |
K1 |
K2 |
… |
完成下列问题:
①比较K1、K2的大小;K1 K2(填“>”、“=”或“<”)。
②判断该反应达到化学平衡状态的依据是 (填序号)。
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保护不变
(3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出墁酸肼第一步水解反应的离子方程式 。
②盐酸肼水溶液中离子浓度的排列顺序正确的是 (填序号)。
A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
C.2 c(N2H62+)+ c([N2H5·H2O+])+c(H+)= c(H+)+c(OH-)
D.c(N2H62+)> c(Cl-)>c(H+)>c(OH-)>
22.(08山东省滨州市三检)下列有关叙述正确的是 (B )
A.在AgCl悬浊液中,加入固体NaCl、KSP(AgCl)变小
B.用两铜棒做电极,电解稀H2SO4,电解初期主要化学方程式为

Cu+H2SO4 CuSO4+H2↑
C.钢柱在水下部分比在空气与水交界处更易腐蚀
D.10mL pH=12的NaOH溶液中加入pH=2的HA溶液至pH=7,所得溶液总体V≥20mL
21.(08山东省滨州市三检)下列表达正确的是 ( C )
A.常温下,pH=1的水溶液中Na+、NO-3、HCO3、Fe2+可以大量共存
B.乙烯、苯和乙醇都不能发生加成反应和加聚反应
C.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+=2Fe3++2H2O
D.醋酸与氢氧化钠溶液反应后,溶液显碱性,则溶液中各离子浓度一定存在如下关系
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
20..(08山东省滨州市二检)一定能在下列溶液中大量共存的离子组是 ( B )
A.水电离产生的c(H+)=1×10-12mol·L-1溶液:NH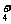 、Na+、Cl-、HCO
、Na+、Cl-、HCO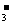
B.能使pH试纸变深蓝色的溶液中:Na+、[Al(OH)4]-、S2-、CO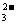
C.含有大量Fe3+的溶液:SCN-、I-、K+、Br-
D.澄清透明的无色溶液中:ClO-、MnO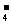 、Al3+、SO
、Al3+、SO
18.(08山东一模)对于体积相同的①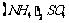 、②)NH4HSO4、③H2SO4溶液,下列说法正确的是( D )
、②)NH4HSO4、③H2SO4溶液,下列说法正确的是( D )
A.溶液的pH相同时,3种溶液物质的量浓度大小顺序是③>②>①
B.溶液的pH相同时,将3种溶液稀释相同倍数,pH变化最大的是①
C.溶液的pH相同时,由水电离出的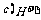 大小顺序是③>②>①
大小顺序是③>②>①
D.若3种溶液的物质的量浓度都相同,则溶液的pH大小顺序是①>②>③
16.(08山东二模)经测定某溶液中离子只有Na+、CH3COO-、H+、OH-四种,且离子浓度大小的排列顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),其可能的情况是
A.该溶液可能由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成
B.该溶液可以由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合而成
C.该溶液中离子浓度的关系符合c(CH3COO-)+c(OH-)>c(Na+)+c(H+)
D.在上述溶液中加入适量NaOH,离子浓度大小可改变为
|
17(08山东一模).下列说法正确的是( c )
①用25mL酸式滴定管可以准确放出8.00mL的稀盐酸;
②可用干燥的pH试纸测定氯水的pH;
③使用容量瓶配制溶液,定容时俯视,所得溶液的浓度偏大;
 ④加入盐酸有能使澄清石灰水变浑浊的无色气体生成,则原溶液中一定有大量CO
④加入盐酸有能使澄清石灰水变浑浊的无色气体生成,则原溶液中一定有大量CO 存在;
存在;
⑤在某温度下,一定量的醋酸与氢氧化钠溶液充分混合,若溶液 呈碱性时,溶液中离子浓度大小的关系一定为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
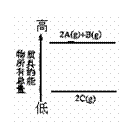
 ⑥右图是反应物和生成物的能量变化示意图,其可能发生反应的热化学方程式可表示为:2A(g)+B(g)
2C(g); △H=QkJ·mol-1(Q<0)。
⑥右图是反应物和生成物的能量变化示意图,其可能发生反应的热化学方程式可表示为:2A(g)+B(g)
2C(g); △H=QkJ·mol-1(Q<0)。
A.①③④ B.②④⑤ C.①③⑥ D.③⑤⑥
14.(08山东济宁4月模拟)已知某酸H2B在水溶液中存在下列关系:

 ①H2B H++HB-,②HB- H++B2-。关于该酸对应的酸式盐NaHB的溶液,下列说法中,一定正确的是( C
)
①H2B H++HB-,②HB- H++B2-。关于该酸对应的酸式盐NaHB的溶液,下列说法中,一定正确的是( C
)
A.NaHB属于弱电解质
B.溶液中的离子浓度c(Na+)>c(HB-)>c(H+)>c(OH-)
C.c(Na+)=c(HB-)+c(B2-)+c(H2B)
D.NaHB和NaOH溶液反应的离子方程式为H++OH- H2O
15(08山东海阳一中模拟)下列说法中正确的是( A )
A.25℃时,向CH3COONa溶液中加入适量CH3COOH使混合液pH=7,此时溶液中 [Na+]=[CH3COO-]
B.25℃时,0.1 mol·L-1氨水和0.05mol·L-氨水中[OH-]之比是2:1
C.体积相同、pH值相同的①盐酸 ②硫酸 ③醋酸,被NaOH溶液完全中和,消耗①、 ②、③溶液的体积由小到大的顺序是②<①<③
D.向含有HCO3-、CH3COO-、CO32-、SO32-离子的溶液中加入足量的Na2O2固体后,假设溶液体积不变,则以上四种离子浓度基本保持不变的是CO32-和CH3COO-。
13.(08青岛质量检测)在一定条件下,相同pH的硫酸和硫酸铁溶液中水电离出来的c(H+)分别是1.0×10-amol·L-1和是1.0×10-bmol·L-1,在此温度下,则下列说法正确的是 ( D )
A.a<b
B.a=b
C.水的离子积为1.0×10-(7+a)
D.水的离子积为1.0×10-(b+a)
12.(08山东实验中学一诊)下列各组离子,一定能大量共存的是 ( )
A.常温下,c(H+)/c(OH-)=1×10-12的溶液:I-、Cl-、HCO3-、Na+
B.含有大量Fe3+的溶液:Na+、HCO3-、NO3-、CO32-
C.加入铝粉能产生氢气的溶液:NH4+、Fe2+ 、SO42- 、Cl-
D.由水电离出的c(H+)=1×10-12 mol•L-1溶液中:K+、Cl- 、NO3- 、Na+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com