
12、3-4
10-3=c1α1 c1=10-3/α1,
c1=10-3/α1,
稀释后c(H+)2=c2α2=0.1c1·α2=0.1α2×10-3/α1=10-4·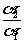 >10-4。
>10-4。
(下标1表示稀释前,下标2表示稀释后)
6、C 7、C 8、AD 9、D 10、C
17、在100mLCaCl2和盐酸的混合液中加入Na2CO3溶液时,测得生成沉淀和所加入Na2CO3溶液的体积曲线关系如图所示。若CaCl2的浓度为0.25mol/L,则原溶液的pH为多少?

[练习答案]
16、计算下列溶液的pH:
(1)pH=3和pH=5的两种盐酸溶液等体积混合。
(2)pH=8和pH=13的两种氢氧化钠溶液等体积混合。
15、某地酸雨经检验除H+和OH-外,还含有Na+、Cl-、NH4+和SO42-等离子,其浓度:C(Na+)=7.0×10-6mol/L,C(Cl-)=3.5×10-5mol/L,C(NH4+)=2.3×10-5mol/L,C(SO42-)=2.5×10-6mol/L,则该酸雨的pH值为 。
14、试回答如何分别利用(1)蒸馏水,(2)pH=10的NaOH溶液,(3)0.01mol/L的盐酸;使pH=12的NaOH溶液100mL的pH变为11?
(1) ;
(2) ;
(3) 。
13、在25℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH值与强碱的pH值之间应满足的关系是 。
12、将pH=3的某一元弱酸溶液冲稀10倍时,溶液的pH范围是 ,确定为该范围的理由是 。
11、HA、HB、HC三种一元弱酸溶液的浓度都是0.1mol/L。在室温时,HA溶液中A‑的浓度是1.32×10-3mol/L,HB的电离度是1.15%,HC溶液的pH值等于3,这三种酸的酸性由强到弱的顺序是 。
10、 已知D2O能发生类似于H2O的电离:D2O D++OD-。常温时,C(D+)·C(OD-)=2×10-15,则下列叙述正确的是( )
已知D2O能发生类似于H2O的电离:D2O D++OD-。常温时,C(D+)·C(OD-)=2×10-15,则下列叙述正确的是( )
A、当pD=7时,溶液呈中性 B、pD+pOD=14
C、0.1mol/L的DCl溶液中pD=1 D、0.1mol/L的NaOD溶液中pD=13
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com