
6.已知a,b,x,y均为正数,且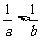 ,x>y,求证
,x>y,求证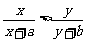 .
.
5.如果-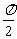 ≤a<β≤
≤a<β≤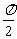 ,则
,则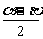 的范围是_________.
的范围是_________.
4.在“充分而不必要条件,必要而不充分条件,充要条件,非充分非必要条件”中选择适当的词填空:
(1)a>b,c>d是a+c>b+d的_________条件;
(2)a+b>2,ab>1是a>1且b>1的_________条件;
(3) >1是a>b的_________条件
>1是a>b的_________条件
3.设a∈R,且a2+a<0,那么a,a2,-a,-a2的大小顺序是
A.a2>a>-a2>-a B.-a>a2>-a2>a
C.-a>a2>a>-a2 D.a2>-a>a>-a2
2.已知a>b,则下列不等式①a2>b2,②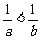 ,③
,③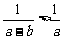 中不成立的个数是
中不成立的个数是
A.0 B.1 C.2 D.3个
1.若a>b>1,P= ,Q=
,Q=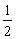 (lga+lgb),R=lg
(lga+lgb),R=lg ,则
,则
A.R<P<Q B.P<Q<R
C.Q<P<R D.P<R<Q
15. 某样品为Na2CO3和NaHCO3固体混合物,现将一定质量的样品与稀盐酸反应,用测定生
成CO2体积的方法计算出样品中各组分的质量分数。为较准确地测出生成CO2的体积,在反应结束后加热反应混合物,使溶于溶液中的CO2逸出,待冷却至室温后测CO2的体积(加热时蒸发的水的体积忽略不计)。右图是实验装置图,其中,B和C可供选择。请回答下列问题:
某样品为Na2CO3和NaHCO3固体混合物,现将一定质量的样品与稀盐酸反应,用测定生
成CO2体积的方法计算出样品中各组分的质量分数。为较准确地测出生成CO2的体积,在反应结束后加热反应混合物,使溶于溶液中的CO2逸出,待冷却至室温后测CO2的体积(加热时蒸发的水的体积忽略不计)。右图是实验装置图,其中,B和C可供选择。请回答下列问题:
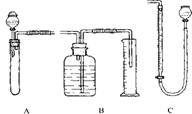
(1)测量CO2气体的体积时,可选用B或C中的一种与A连接,你将选择____(填B或C),不选另一种的理由是 ____________________________。
(2)在B或C中所盛的液体应为_________(选填编号)。
A.澄清石灰水 B.饱和Na2CO3溶液
C.水 D.NaOH溶液
(3)在正确选用了B或C中所盛液体后,则实验过程中造成收集到的CO2体积会_________(填“偏大”或“偏小”)。若要使收集到的CO2体积较准确,应对该实验作何改变?____________________________________________。
(4)若测得CO2体积换算成标准状况下是VL(样品为mg),则V的数值范围是_______________(用含m的代数式表示)。
(5)若气体最大量程为50mL,则固体样品的取样范围是______________(假设为标准状况下)。
(6)用此方法测定Na2CO3或NaHCO3质量分数其结果不够准确。现有人设计了下面几种实验方案,请你从中选择一种既简单可行又测定结果较准确的实验方案是___________(选填编号)。
A.称取一定量样品,配成溶液,加入澄清石灰水,将产生的沉淀过滤、洗涤、干燥、称量,则可计算出样品中各组分的质量分数
B.称取一定量样品,加热样品使之反应完全,恢复至室温,再称量剩余固体质量,则可计算出样品中各组分的质量分数
C.称取一定量样品,加热样品使之反应完全,将收集到的CO2称其质量,则可计算出样品中各组分的质量分数
D.称取一定量样品,加热样品使之反应完全,将用排水法收集到的CO2测出其体积,则可计算出样品中各组分的质量分数
答案 (1)C 因为B用量筒计量水的体积误差太大 (2) C (3)偏小 在C装置量气管处水面上加一层油,减少CO2溶解 (4)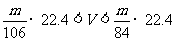 (5)
(5)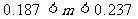 (6) B
(6) B

14. (江苏省扬州中学2008-2009学年第一学期第一次月考)硅酸盐在自然界中分布极广,几乎在所有的硅酸盐矿物中,Si原子都和4个O原子结合成四面体的[SiO4]单元(图1),图中○表示“O”,⊙表示“Si-O”),[SiO4]单元既可以是分立的,也可以和其它四面体共用顶点连接各种各样的链状结构(如图2)、环状结构(图3)

(1)形成硅氧四面体是硅与氧成键的一个重要特征,试再举两种含有[SiO4]单元的物质(要求不同种类) 。
(2)最简单的硅酸盐是硅酸钠,硅酸钠溶液中滴入酚酞显红色,用离子方程式解释其原因 ,通入CO2能使溶液的红色褪色,离子方程式 。
(3)将某些盐混进硅酸钠溶液时,盐会向上扩散长成很漂亮的树状,且树会保留金属离子的特征颜色,例如:CuSO4·5H2O和Na2SiO3溶液发生水解反应长成蓝色的树,NiSO4·7H2O则会长成绿色的树,写出加入CuSO4·5H2O长成蓝树的离子方程式: 。
(4)图1为 ,图2、图3所示硅酸盐离子的符号
、
,图2、图3所示硅酸盐离子的符号
、
(5)由13个正四面体结合成的环状结构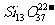 离子中,其中有
个正四面体和另外的四面体共享2个顶点
离子中,其中有
个正四面体和另外的四面体共享2个顶点
答案(1)SiO2或H4SiO4或其它合理答案
 (2)SiO32-+2H2O H2SiO3+2OH- 2CO2+2H2O+SiO32-=2HCO3-+H2SiO3↓
(2)SiO32-+2H2O H2SiO3+2OH- 2CO2+2H2O+SiO32-=2HCO3-+H2SiO3↓
(3)Cu2++SiO32-+2H2O=Cu(OH)2↓+H2SiO3↓
(4)Si3O108 Si3O96
(5)9个
13. X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。请回答:
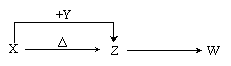
(1)W的电子式是 。
(2)X与Y在溶液中反应的离子方程式是 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置V中可收集到一种无色气体
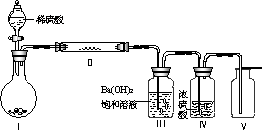
①装置Ⅰ中反应的化学方程式是 。
装置Ⅱ中物质的化学式是 。
②用Ⅹ含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 ,所需仪器装置是 (从上图选择必要的装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是 。
 答案:
答案:
(2)
(3)①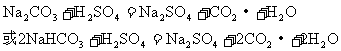 Na2O2
Na2O2
② H2O2 I、IV、V
(4)
12.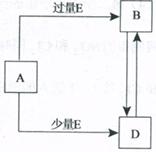 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的转化关系如图所示(部分产物略去)。
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的转化关系如图所示(部分产物略去)。
(1)若A和E为单质且B物质为由极性键形成的非极性分子。
B的电子式为: ,M的原子序数比A大76,则M位于元素周期表中第 周期 族。试写出M的最高价氧化物与浓盐酸反应得到单质气体C的化学反应方程式:
 (2)若A、B、D、E均为高熔点的物质且E、D为单质,写出A→B的化学方程式:
。D的原子结构示意图:
。
(2)若A、B、D、E均为高熔点的物质且E、D为单质,写出A→B的化学方程式:
。D的原子结构示意图:
。
(3)若A为可溶性强碱(MOH),E为同主族元素形成的常见非金属化合物,且该化合物中两元素的质量比为l:1,试写出A→B的化学方程式:
答案 (1)O∶∶C∶∶O 六,ⅣA
 PbO2+4HCl=PbCl2+Cl2↑+2H2O
PbO2+4HCl=PbCl2+Cl2↑+2H2O
(2)SiO2+3C SiC+2CO +14
(3)MOH+SO2=MHSO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com