
6£®ÈçÏÂͼËùʾ£ºÊÇÓĂĂ÷·¯[KAl(SO4)2¡¤12H2O]ÖÆÈ¡Ạ́ËáÂÁºÍẠ́Ëá¼ØµÄ²Ù×÷²½ÖèÁ÷³̀ͼ(ͼÖĐÂÔÈ¥Á˳ÁµíÎïµÄÏ´µÓ²Ù×÷)£¬ÇëÔÚͼÖĐÔ²À¨ºÅÄÚ̀îÈëÊʵ±µÄÊÔ¼ÁĂû³Æ£¬ÔÚ·½À¨ºÅÄÚ̀îÈëÊʵ±µÄ·ÖÀë·½·¨£¬²¢»Ø´đÓĐ¹ØÎỀâ¡£
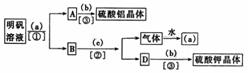
(1)ÊÔ¼ÁaÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ £¬bÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ £¬cÊÇ¡¡¡¡¡¡¡¡¡¡ ¡£·ÖÀë·½·¨¢ÙÊÇ¡¡¡¡¡¡¡¡ £¬¢ÚÊÇ¡¡¡¡¡¡¡¡¡¡ £¬¢ÛÊÇ¡¡¡¡¡¡¡¡¡¡ ¡£
(2)°´ÉÏÊö²Ù×÷£¬²»¿¼ÂÇËđºÄ£¬ÔÚÀíÂÛÉÏ£¬158gĂ÷·¯×î¶à¿É̉ÔÖƵĂAl2(SO4)3¡¤18H2O____g£¬ÖÁÉÙ¿É̉ÔÖƵĂK2SO4______g¡£
5£®»Ø´đÏÂÁĐÓĐ¹Ø½đÊô͵ÄÎỀ⣺
(1)ÔÚʹÓõçÀÓ̀úʱ£¬ÆäÍ·²¿ÊÇ̉»ÍÖƵÄÀÓ̀úÍ·£¬³¤ÆÚʹÓĂ£¬±íĂæ±»Ñơ»¯£¬µ«ÍÑÂäÏÂÀ´µÄÑơ»¯Ä¤È´ÊǺ́É«µÄ£¬ÊÔ˵Ă÷Ộ̉¡£
(2)Đí¶à½đÊôµ¼̀åÔÚµ¼µç¹ư³̀ÖĐ̉×Ă°µç»đ»¨£»ÍµÄµ¼µçĐÔ½ö´ÎÓÚ̉ø£¬µ«¼Û¸ñ½ÏµÍ¡£ÊÔ·ÖÎöÔÚº½¿ỞDZíÖĐÎªÊ²Ă´²»²ÉÓĂÍ£¬¶øÊÇÓĂ¼Û¸ñ½ÏΪ°º¹óµÄAu¡¢Pt¡¢PdµÄºÏ½đ×÷Ϊ´¥µă£¿
(3)CuS¼È¿ÉÈÜÓÚÏ¡HNO3,ÓÖ¿ÉÈÜÓÚKCN£¬ƠâÁ½ÖÖÈܽâ¹ư³̀Ă÷ÏÔ²»Í¬£¬Ç°̉»·´Ó¦ÖĐCuSÉú³ÉSµ¥ÖÊ£¬ºó̉»·´Ó¦ÖĐCuSÉú³É(Cu(CN)4)3£¡£Đ´³ö»¯Ñ§·½³̀ʽ¡£
4£®½«amL 0.1mol/LẠ́ËáÂÁÈÜ̉ºÓëbmL 0.5mol/LÇâÑơ»¯ÄÆÈÜ̉º»́ºÏ£¬µĂµ½cmolÇâÑơ»¯ÂÁ³Áµí£¬ÈổÑÖªa¡¢b¡¢cÖĐÈÎ̉âÁ½¸öÖµ£¬ÇóÁí̉»¸öÖµ£¬ËùÇóµÄÖµ²»Ö¹̉»¸ö½âµÄÊÇ(¸÷Ñ¡ÏîÖĐ£¬µ¥Î»¾ù̉ÑÂÔÈ¥)
A£®a£½100¡¡ b£½90¡¡ c£½?¡¡ B£®a£½100¡¡ c£½0.015¡¡ b£½?
C£®b£½90¡¡ c£½0.015¡¡ a£½?¡¡ D£®a£½75¡¡ c£½0.015¡¡ b£½?
3£®ÓĐ̉»ÄÆ¿é·ÅÖĂÓÚ³±Êª¿ƠÆøÖĐ£¬±íĂæÑơ»¯±äÖÊ£¬Ç̉ÈÔΪ°×É«¿é×´¹̀̀壬³ÆÆäÖÊÁ¿Îª25g£¬½«ÆäÈ«²¿Í¶Èë×ăÁ¿Ë®ÖĐ·´Ó¦£¬µĂµ½ÈÜ̉º1000mL £¬²¢ÊƠ¼¯µ½Æø̀å2.24L(±ê×¼×´¿öϵĴ¿¾»Îï)£¬ÔÙÈ¡´ËÈÜ̉º100mL£¬ÓĂ1mol/LµÄÑÎËáµÎ¶¨ÖÁÖĐĐÔ£¬ÓĂÈ¥70mL£¬²¢½«µÎ¶¨¹ư³̀ÖĐ²úÉúµÄÆø̀åͨÈëµ½×ăÁ¿µÄ³ÎÇåʯ»̉Ë®ÖĐ£¬µĂµ½¸ÉÔïµÄ³Áµí1g£¬Ộ½đÊôÄƵÄÑơ»¯ÂÊΪ
A£®71.4%¡¡¡¡ B£®81.6%¡¡¡¡ C£®18.4%¡¡¡¡ D£®28.6%
2£®Ị̈Ạ́ËáÍÈÜ̉ºÖĐ¼ÓÈ백ˮ£¬Ê×ÏÈĐγÉÄÑÈÜÎ¼̀Đø¼Ó°±Ë®£¬ÄÑÈÜÎïÈܽâµĂµ½ÉîÀ¶É«µÄ͸Ă÷ÈÜ̉º¡£ÏÂÁжԴËÏÖÏó˵·¨ÖĐƠưÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
A£®Cu(OH)2ÏÈÉú³ÉºóÓÖÈܽ⣬˵Ă÷Cu(OH)2ºÍAl(OH)3µÄĐÔÖÊÏàËÆ
B£®³ÁµíÈܽâºó£¬½«Éú³ÉÉîÀ¶É«µÄÅäÀë×Ó[Cu(NH3)4] 2+
C£®Ị̈·´Ó¦ºóµÄÈÜ̉ºÖĐ¼ÓÈë̉̉´¼ÓĐ¾§̀åÎö³ö£¬̣̉Ϊ[Cu(NH3)4] 2+Óë̉̉´¼·¢Éú·´Ó¦
D£®ÔÚ[Cu(NH3)4] 2+Àë×ÓÖĐ£¬Cu2+̀ṩ¿Ơ¹́µÀ£¬NH3̀ṩ¹Â¶Ôµç×Ó
1£®½ÚÈƠµÄÑæ»đÔڼž²µÄ̉¹¿Ơȼ·Å³öѤÀö¶à×˵ĻĂ棬ƠâÊÇÀûÓĂÁË̉»Đ©½đÊôÔªËØÔÚȼÉƠʱ²úÉú²»Í¬µÄÑƠÉ«µÄÔÀí£¬È纬ÓĐ¸Æ¡¢¼Ø¡¢ÍÔªËصĻ¯ºÏÎïÄܲúÉúשº́É«¡¢×ÏÉ«¡¢ẦÉ«µÄ»đÑæ¡£½áºÏÎ̉ĂÇѧ¹ưµÄ֪ʶ£¬ÏÂÁĐ¹ØÓڸơ¢¼Ø¡¢ÍµÄ̉±Á¶·½·¨ƠưÈ·ÊÇ
A£®µç½â·¨¡¡ Èȷֽⷨ¡¡ ÈÈ»¹Ô·¨ ¡¡¡¡¡¡¡¡
B£®µç½â·¨¡¡ µç½â·¨¡¡¡¡¡¡ ÈÈ»¹Ô·¨
C£®ÈÈ»¹Ô·¨¡¡ Èȷֽⷨ¡¡ µç½â·¨¡¡¡¡¡¡¡¡
D£®µç½â·¨¡¡ µç½â·¨¡¡¡¡¡¡ Èȷֽⷨ
5£®Îå²ÊçÍ·×µÄÍÊÀ½ç
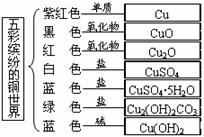
[µäĐÍÀưÎö]
Àư1£º°Ñ̉»Æ¿²»±¥ºÍµÄÉƠ¼îÈÜ̉º·Ö³É4µÈ·Ư¡£±£³ÖζȲ»±ä£¬Ị̈4·ƯÈÜ̉ºÖĐ·Ö±đ¼ÓÈë̉»¶¨Á¿µÄNaOH¡¢Na2O2¡¢Na2OºÍNa£¬Ê¹ÈÜ̉º¾ùÇ¡ºĂ±¥ºÍ£¬ÏÂÁĐ˵·¨ÖĐƠưÈ·µÄÊÇ
A£®¼ÓÈëµÄNaOHµÄÖÊÁ¿̉»¶¨×î´ó
B£®¼ÓÈëµÄNa2O2ºÍNa2OµÄÖÊÁ¿±ÈΪ1:1
C£®¼ÓÈëµÄNaOH¡¢Na2O2¡¢Na2O¡¢NaµÄÎïÖʵÄÁ¿Ö®±ÈΪ2:1:1:2
D£®ÖƳɱ¥ºÍÈÜ̉ººó£¬4·ƯÈÜ̉ºÖĐËùº¬NaOHÖÊÁ¿Ïàͬ
±äʽѵÁ·£º½«NaHCO3ºÍNa2O2¹̀̀å»́ºÏÎïÖĂÓÚĂܱƠÈƯÆ÷ÖĐ¼ÓÈÈÖÁ250¡æ£¬Ê¹Æä³ä·Ö·´Ó¦ºó£¬×îºóµĂµ½²ĐÓà¹̀̀åÓÉÁ½ÖÖÎïÖÊ×é³É£¬·Ö±đΪamol£¬bmol£¬Ç̉a>b¡£ÊÔͨ¹ư¼ÆËă£º
(1)ÇóÔ¹̀̀å»́ºÏÎïÖĐNaHCO3ºÍNa2O2µÄÎïÖʵÄÁ¿¡£
(2)Çó×îºóÆø̀¬Éú³ÉÎïÖи÷ÎïÖʵÄÁ¿¡£
Àư2£ºỊ̈XµÄÈÜ̉ºÖĐ£¬¼ÓÈëYÊÔ¼Á£¬²úÉúµÄ³Áµíʾ̉âͼÈçÏÂͼËùʾÇéĐεÄÊÇ(×¢̉âÏ߶εÄбÂÊ)
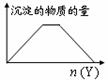
A£®Ị̈NaOHºÍCa(OH)2µÄ»́ºÏ̉ºÖĐͨÈëCO2¡¡¡¡¡¡¡¡ ¡¡¡¡
B£®Ị̈HClºÍAlCl3µÄ»́ºÏ̉ºÖĐµÎ¼ÓNaOH
C£®Ị̈NH4Al(SO4)2ÈÜ̉ºÖĐµÎ¼ÓNaOH¡¡¡¡¡¡¡¡
D£®Ị̈NH4ClºÍMgCl2µÄ»́ºÏ̉ºÖĐµÎ¼ÓNaOH
±äʽѵÁ·£º½«mg Al2O3ºÍFe2O3µÄ»́ºÏÎïÈÜÓÚ100mLÑÎËáÖĐ£¬È»ºóÖđµÎ¼ÓÈë1mol/LNaOHÈÜ̉º£¬Æä½á¹ûÈçͼËùʾ£º
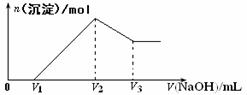
(1)×î³ơ¼ÓÈëV1mLNaOHÈÜ̉ºµÄ×÷ÓĂÊÇ____________£»
(2)ÑÎËáµÄÎïÖʵÄÁ¿Å¨¶ÈÊÇ___________________£»
(3)Èômg»́ºÏÎïÖĐAl2O3ºÍFe2O3°´²»Í¬±ÈÀư½øĐĐÉÏÊöʵÑé(ÆäËû̀ơ¼₫²»±ä)£¬ỘV2µÄÖµ»á²»»á¸Ä±ä__________(̀î¡°»á¡±»̣ ¡°²»»á¡±)£¬(V2-V1)µÄÈ¡Öµ·¶Î§ÊÇ____________¡£
Àư3£ºÏÖÓĐFe¡¢Cu×é³ÉµÄºÏ½đ£¬ÆäÖĐFe¡¢CuµÄ×ÜÎïÖʵÄÁ¿Îªamol¡¢CuµÄÎïÖʵÄÁ¿·ÖÊưΪx£»ÑĐ³É·ÛÄ©ºó£¬È«²¿Í¶È뺬bmolHNO3Ï¡ÈÜ̉ºÖĐ£¬Î¢ÈÈʹÆä³ä·Ö·´Ó¦£¬Ç̉ÏơËáµÄ»¹Ô²úÎïÖ»ÓĐNO£¬ÊԻشđÏÂÁĐÎỀ⣺
(1)ÓĂ΢Á£µÄ·ûºÅ̀îĐ´ÏÂÁĐ¿Ơ°×(ÁĐ¾ÙÈ«²¿¿ÉÄܳöÏÖµÄÇé¿ö)
|
¡¡ |
¢Ù |
¢Ú |
¢Û |
¢Ü |
¢Ư |
¢̃ |
|
²ĐÁô¹̀̀å³É·Ö |
¡¡ |
¡¡ |
¡¡ |
¡¡ |
¡¡ |
¡¡ |
|
ÈÜ̉ºÖĐµÄ½đÊôÀë×Ó |
¡¡ |
¡¡ |
¡¡ |
¡¡ |
¡¡ |
¡¡ |
(2)µ±ÈÜ̉ºÖĐ½đÊôÀë×ÓÖ»ÓĐFe2+¡¢Cu2+ʱ£¬ỘbµÄÈ¡Öµ·¶Î§ÊÇ(ÓĂa¡¢x±íʾ)_____________¡£
(3)µ±x=0.5ʱ£¬ÈÜ̉ºÖĐFe3+¡¢Fe2+µÄÎïÖʵÄÁ¿ÏàµÈʱ£¬ÔÚ±ê×¼×´¿öϹ²²úÉú672mLÆø̀壬Çóa¡¢bµÄÖµ¡£
±äʽѵÁ·£ºÈ¡̉»¶¨Á¿µÄFe¡¢CuµÄ»́ºÏÎï·ÛÄ©£¬Æ½¾ù·Ö³ÉÎåµÈ·Ư£¬·Ö±đỊ̈Ă¿̉»·ƯÖĐ¼ÓÈë̉»¶¨Á¿µÄÏ¡ÏơËᣬʵÑéÖĐÊƠ¼¯µ½µÄNOÆø̀å(Ω̉»»¹Ô²úÎï)µÄ̀å»ư¼°ËùµĂÊ£ÓàÎïµÄÖÊÁ¿¼Ç¼ÈçÏÂ(ËùÓĐ̀å»ư¾ùÔÚ±ê×¼×´¿öϲⶨ)£º
|
ʵÑéĐ̣ºÅ |
1 |
2 |
3 |
4 |
5 |
|
ÏơËáÈÜ̉º̀å»ư(mL) |
100 |
200 |
300 |
400 |
500 |
|
Ê£Óà¹̀̀åµÄÖÊÁ¿(g) |
17.2 |
8 |
0 |
0 |
0 |
|
Æø̀å̀å»ư(L) |
2.24 |
4.48 |
6.72 |
7.84 |
7.84 |
(1)¸ĂʵÑéÖĐËùÓĂÏơËáµÄÎïÖʵÄÁ¿Å¨¶ÈΪ___________¡£
(2)µÚ1´ÎʵÑéºóÊ£Óà¹̀̀åΪ___________£¬µÚ2´ÎʵÑéºóÊ£Óà¹̀̀åΪ___________¡£(¾ù̀îĐ´»¯Ñ§Ê½)¡£
(3)ÇóʵÑéÖĐĂ¿´ÎËùÈ¡»́ºÏÎïÖĐ͵ÄÖÊÁ¿
[µ±̀Ă·´À¡]
4£®Í¼°Æ仯ºÏÎï¼äµÄת»¯¹Øϵ
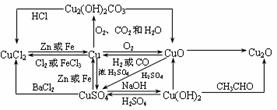
3£®̀ú¼°Æ仯ºÏÎï¼äµÄת»¯¹Øϵ

2£®ÂÁ¼°Æ仯ºÏÎï¼äµÄת»¯¹Øϵ

¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com