
1.D 2.B 3. C 4.D 5.B 6.C 7.A 8.B 9.C 10.C
2. C讲析:玻璃态的水和普通液态水的密度相同
新活题网站
1.(1)将导管的出口浸入水槽的水中,手握住试管,有气泡从导管口逸出,放开手后,有少量水进入导管,表明装置不漏气。
(2)②①③ (3)慢慢将量筒下降
(4)
讲析:第(2)小题,因排出的气体是需要用排出的水的体积衡量,而反应前后的量筒温度不同的,因此,停止加热、回到室温后,将量筒下移以调节量筒内的液面与水槽一致。
13.100.0g无水氢氧化钾溶于100.0g水。在T温度下电解该溶液,电流强度I=6.00A,电解时间10.00h。电解结束温度重新调至T,分离析出的KOH·2H2O固体后,测得剩余溶液的总质量为164.8g。已知不同温度下每100g氢氧化钾饱和溶液中氢氧化钾的质量为:
|
温度/℃ |
0 |
10 |
20 |
30 |
|
KOH/g |
49.2 |
50.8 |
52.8 |
55.8 |
(已知电子的电量为1.6×10-19c,最后结果要求三位有效数字。)
(1)被电解的水的物质的量为________mol。
(2)计算电解后剩余溶液的质量分数(写出计算过程)。
(3)温度T为________。
12.下图每一方框中的字母代表一种反应物或生成物:
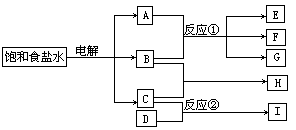

物质A跟B反应生成物质E、F和G;物质C跟D反应生成物质I,某温度下该反应起始和某时刻的反应混合物组成如右上表格所示。请填写下列空白:
(1)物质H的分子式是_____________。
(2)反应①的化学方程式是
________________________________________________。
(3)反应②的化学方程式(须注明反应条件)是_______________________________。
11. 关于“电解氯化铜溶液时的pH变化”问题。化学界有以下两种不同观点:
观点一是:“理论派”认为电解氯化铜溶液后溶液的pH升高。
观点二是:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时,pH随时间的变化如图曲线示。请回答下列问题:
(1)电解前氯化钠溶液的pH处于A点的原因是(用离子方程式说明):
(2)“理论派”所持观点的理论论据是
(3)“实验派”的实验结论是 ,该观点的理由是(从化学原理上加以简述):
10.某学生试图用电解法根据电极上析出的物质的量质量来验证阿佛加德罗常数值,其实验方案的要点为:①用直流电电解氯化铜溶液,所用仪器如右图:②在电流强度为I安培,通电时间为t秒钏后,精确测得某电极上析出的铜的质量为m克。试回答
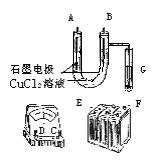
(1)连接这些仪器的正确顺序为(用图中标注仪器接线柱的英文字母表示。下同)E接 ,C接 , 接F。实验线路中的电流方向为 → → →C→ →
(2)写出B电极上发生反应的离子方程式 G试管中淀粉KI溶液变化的现象为 ;相应的离子方程式是 。
(3)为精确测定电极上析出铜的质量,所必需的实验步骤的先后顺序应是 。(选填下列操作步骤的编号)①称量电解前电极质量 ②刮下电解后电极上的铜并清洗 ③用蒸馏水清洗电解后电极 ④低温烘干电极后称量 ⑤低温烘干刮下的铜后称量 ⑥再次低温烘干后称量至恒重
(4)已知电子的电量为1.6×10-19库仑。试列出阿佛加德罗常数的计算表达式:
NA
9.有一硝酸盐晶体,其化学式表示为M(NO3)x·nH2O经测定其摩尔质量为242g·mol-1。取1.21g该晶体溶于水配成100mL溶液。将此溶液倒入右图所示装置中,用石墨作电极进行电解。当有0.01mol电子通过电极时,溶液中的金属阳离子全部析出,在A极得到金属0.32g。回答:
(1)金属M的原子量为 ,x = ,n = 。
(2)C极为 极。
(3)电解后溶液的pH为(设电解前后溶液的体积不变) 。
8. 已知SO2(H2SO3)能使溴水褪色,且相互定量反应。简答用惰性电极电解物质的量深度相等的BaI2和SO2的混合液(含少量的淀粉)时的现象和反应问题:
(1)电解时,在阳极附近的溶液中,将先后观察到什么现象?请写出先后相应发生的两步阳极反应式。
。
(2)写出第二步电解的化学方程式:
。
(3)如此分步电解的理论根据是什么?
7.现有500毫升食盐水,其中含有少量的NaOH,该溶液的PH值等于10,用石墨电极电解当,阴极产生的气体体积为5.60升(标况)时停止电解,此时溶液的PH值约为(忽略溶液的体积变化) ( ) A.13 B.12.3 C.12 D.14
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com