
13£Æ(1)““—ß…˙°° “ÚŒ™º◊—ß…˙…˺∆µƒ◊∞÷√£¨–° ‘πÐÃ◊‘⁄¥Û ‘πÐ÷–£¨–° ‘πÐ÷–µƒø’∆¯≤ª“◊≈≈≥ˆ£¨«“«‚∆¯“◊¥”¡Ω ‘πÐø’œ∂“ð≥ˆ(2)Ω´¥Û ‘πЬ˛¬˛œÚ…œ“∆∂Ø°°
(3)∑œ∏…µÁ≥ÿµƒ–ø∆§∫Õ∞◊¥◊ °£°°°°°°°°°°°°°°°°°°°°
12£Æ(1)10%-70% °° (2)’‚÷÷Àµ∑®÷ªƒÐ±Ì√˜ ’ºØµ¬H2ê˝∑÷ ˝¥Û”⁄70%£¨∂¯≤ª «¥øH2
Ω≤Œˆ£∫(1)”…±Ì÷–ø…÷™£∫H2µƒÃª˝∑÷ ˝Œ™90%°¢80% ±£¨ƒÐ∞≤æ≤µƒ»º…’£¨ H2µƒÃª˝∑÷ ˝–°”⁄10% ±£¨≤ª»º…’£¨∆‰À¸∫¨¡øæ˘±¨’®£¨“Ú¥ÀªÏ∫œ∆¯µƒ±¨’®ø…»∑∂®
11£ÆD
1£ÆB°° 2£ÆC°° 3£ÆD°° 4£ÆB 5£ÆC 6£ÆB 7£ÆD 8£ÆD 9£ÆA 10.C
2£Æ(1)C6H10O5+6O2°˙6CO2+5H2O
(2)BODŒ™0.0112 g°§L-1(3)”„¿ý≤ªƒÐ’˝≥£±£≥÷…˙√¸
Ω≤Œˆ£∫±æÂÀ˘ ˆµƒƒ⁄»ð‘⁄øŒƒ⁄≤¢Œ¥—ßπ˝£¨∂¯∆‰…ʺ∞ƒ⁄»ð‘Ú≤¢≤ª∏¥‘”°£
(1)≈‰∆Ω∑Ω≥Ã Ω£¨¥À∑Ω≥à Ωø…“‘ø¥◊ˆŒ™∫¨—ı”–ª˙ŒÔC6H10O5µƒ°∞»º…’°±∑Ω≥Ã Ω£¨“Ú∑÷◊”÷–H:O‘≠◊”±»∑˚∫œ2:1£¨‘ÚC°˙CO2À˘∫ƒ—ı¡øº¥Œ™ÕÍ»´—ıªØC6H10O5 ±µƒ∫ƒ—ı¡ø£∫
C6H10O5+6O2°˙6CO2+5H2O
(2)º∆À„BOD£¨Ω´∫”ÀƵƒ√Ð∂»Ω¸À∆ø¥◊˜1g°§cm£≠3£¨‘Ú1L∫”ÀƵƒC6H10O5µƒ÷ ¡øŒ™£∫
m(C6H10O5)=10°¡10-5g/cm3=1°¡10-2g
∏˘æðªØ—ß∑Ω≥à ΩΩ¯––º∆À„£∫
…Ë1°¡10-2g”–ª˙ŒÔ◊™ªØŒ™ŒÞª˙ŒÔ÷ –ËO2÷ ¡øŒ™m(O2)
m(O2)=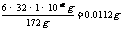
(3)”Î’˝≥£»Ð—ı¡ø±»Ωœ£∫0.0112g°§L-1>0.0092 g°§L-1£¨º¥BOD¥Û”⁄ÀÆ÷–µƒ’˝≥£—ı∆¯¡ø£¨π ”„¿ý≤ªƒÐ±£≥÷…˙√¸°£
°°ºÏ≤‚÷∏þ
1£Æ D°°Ω≤Œˆ£∫ æ–≈œ¢÷–”–“ª∏ˆπÿº¸µ„£¨º¥°∞»˝∏ˆ∑¥”¶µƒ¡™∫œ”Η≠ª∑°±°£∞—Â∏¯µƒ»˝∏ˆ∑¥”¶œýº”£¨ø…µ√◊Ð∑¥”¶ Ω «£∫2H2O=2H2°¸+O2°¸£¨¥”÷–æÕø…“‘µ√≥ˆ£¨’‚»˝∏ˆ∑¥”¶µƒƒøµƒ «Œ™¡Àµ√µΩH2°£
15£Æ(1)KMnO4 (2)K2MnO4+Cl2=2KCl+MnO2+O2°¸
(3)9
µ⁄19øŒ ±°°(BæÌ)
濥̗µ¡∑
14.¢Ÿ—ıªØÕ≠º”»»«∞“™œ»Õ®«‚∆¯£¨≈≈»• ‘πЃ⁄ø’∆¯£ª
¢⁄∑¥”¶∫Û»»Õ≠∑€ªπ–Ë‘⁄«‚∆¯÷–¿‰»¥£ª
¢€≤ø∑÷«‚∆¯Õ®π˝◊∞”–—ıªØÕ≠µƒ ‘πÐ ±£¨Œ¥”ΗıªØÕ≠∑¥”¶
13.¢≈bπÐ÷–µƒ“∫√Êæ˘∏þ”⁄aπУ¨∏þ∂»µƒœý≤ÓŒ™£∫C>B>D>A
¢∆»˝÷ß¿Ø÷Ú∞¥”…µÕµΩ∏þµƒÀ≥–Ú“¿¥Œœ®√°° ”…”⁄CO2µƒ√Ð∂»¥Û”⁄ø’∆¯
11.C°°12.CD
Ω≤Œˆ£∫10.‘⁄±∏—°µƒŒÔ÷ ÷–£¨COµƒœý∂‘∑÷◊”÷ ¡ø∫Õø’∆¯◊ÓœýΩ¸£¨∏˘æð∞¢∑¸º”µ¬¬Þ∂®¬…£¨ø…÷™√Ð∂»œýΩ¸£¨≈≈ø’∆¯ºØµ√∆¯ÃÂ¥ø∂»◊ÓµÕ°£°°11.∑¢…˙◊Ó«ø¡“±¨’®º¥º◊ÕÈ∫Õø’∆¯÷–µƒ—ı∆¯«°∫√ÕÍ»´∑¥”¶°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com