
12.1.92g铜和一定量的浓硝酸反应,随着铜的不断减少,反应生成的气体颜色也逐渐变浅。当铜反应完毕时,共收集到气体体积为1.12L(标况)。求反应中消耗的HNO3的物质的量。
11.在稀HNO3和稀H2SO4的混合溶液200mL中,滴入10mL 1mol/L的NaOH溶液恰好中和。向同量的这种混合溶液中加入过量BaCl2溶液,所生成的BaSO4沉淀,经洗涤干燥后,生成0.5825g,试求该混合溶液中HNO3和H2SO4的物质的量浓度。
10.硝酸工业尾气中的氮的氧化物(NO、NO2)是要大气污染物,其常用的治理方法有以下两种(已简化):
①NaOH吸收法。反应原理是:
2NO2+2NaOH NaNO3+NaNO2+H2O
NO+NO2+2NaOH 2NaNO2+H2O
②氨催化还原法。反应原理是NOx+NH3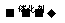 N2+H2O 现有一定量的含NO2和NO的硝酸工业尾气(不含其他气体)若用过量NaOH溶液吸收后,溶液中NaNO3与NaNO2的物质的量之比恰好与尾气中NO和NO2的物质的量之比相等。
N2+H2O 现有一定量的含NO2和NO的硝酸工业尾气(不含其他气体)若用过量NaOH溶液吸收后,溶液中NaNO3与NaNO2的物质的量之比恰好与尾气中NO和NO2的物质的量之比相等。
(1)若用NOx表示氮的氧化物的平均组成,试求x的值。
(2)将1体积该尾气用氨催化还原法处理,至少消耗多少体积相同状况下的氨气?
9. L、M、R、P、Q分别代表五种含不同化合价的氮元素的物质。A、B分别代表两别含不同化合价的氯元素的物质(每种物质中,氮或氯元素的化合价只有一种),又知物质M中的氮元素的化合价要比物质Q中氮元素的化合价低。在一定条件下,它们会发生如下的转化(关系式未配平):
①P+A→Q+B ②L+O2→M+H2O
③L+M→R+H2O ④B+H2O→A+O2
(1)若五种含氮元素的物质中,有一种是硝酸,则硝酸是 ,理由是 。
(2)反应②必须在催化剂(铂、氧化铁等)作用下,加热到一定温度时方能发生,此反应在化工生产上有重要用途。据此推断在同温、同压下,若物质R的密度比二氧化碳的密度小,则R的化学式为 .
(3)某学生写出下面三个含氮的物质的相互转化的关系式:
(a)M+P→N2O3+H2O
(b)N2O4+H2O→P+Q
(c)M+L→Q+H2O
其中一定不可能实现的是 ,理由是 。
8.0.96g Mg跟含6.3g HNO3的稀溶液恰好反应完全,则HNO3的还原产物的相对分子质量可能是 ( )
A.30 B.44 C.46 D.80
7.下列对氧化还原反应的叙述不正确的是
A.氧化剂所含元素得电子,化合价降低,所以氧化剂发生还原反应
B.还原剂所含元素失电子,化合价升高,所以还原剂被氧化
C.凡是有单质参加或生成的反应一定是氧化还原反应
D.氧化还原反应中被氧化和被还原的原子个数必相等
6.硝酸铵分解反应为NH4NO3-HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为
A.5:3 B 3:5
C.1:1 D.1:2
5.下列关于硝酸的叙述中,正确的是 [ ]
A.在相同条件下,硝酸的浓度越大,密度越大,挥发性越强
B.所有的金属与稀硝酸反应都放出NO气体
C.稀硝酸与铜反应生成NO,而浓硝酸与铜反应则生成NO2,说明稀硝酸的氧化性更强
D.稀硝酸具有酸性,可与较活泼金属反应生成氢气
4.氮和钠可形成化合物Na3N,它能与水剧烈反应产生NH3,下列叙述正确的是
A.Na3N与水的反应是非氧化还原反应
B.Na3N 是共价化合物
C.Na3N若与足量盐酸作用可生成两种盐
D.Na3N中钠离子与氮离子半径相等
3.1.92g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL气体(标况)。将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积是
A.504mL B。168mL
C。336mL D。224mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com