
10.(1)滴加氨水至过量Al3++3NH3·H2O= Al(OH)3↓+NH4+
(2)通人CO2至过量 AlO2-+CO2+2H2O= Al(OH)3↓+HCO3-
8. Al(OH)3在溶解的过程中质量的减少小于BaSO4沉淀
质量的增大。 9. n(Al3+)=n[Al(OH)3]或n(AlO2-)= n[Al(OH)3]
1.A 2.C 3.C 4.C 5.D 6.C 7.AD 8. C 9. BD
讲析:2.镁能在CO2中燃烧,铝能发生铝热反应,铝在常温时遇浓硝酸钝化。3.除溶液为无色外,本题应按在酸性或碱性条件下两种情况讨论。5.溶质均为MgSO4且量相等,主要运用守恒法比较溶液的质量大小。 6. n(NaOH)=n(Cl-)+n(Al3+) 7.反应后形成NaCl和NaAlO2的混合溶液。
4.⑴中和过量H2SO4 ⑵3.25mol/L ⑶ Al2O3和Fe2O30.05mol
讲析:计算时注意运用电荷守恒。
检测提高
3.⑴Al2O3 ⑵(NH4)2SO4、K2SO4
⑶AlO2- + CO2 + 2H2O = Al(OH)3 ↓+ HCO3-
讲析:突破口是Al2O3是两性氧化物。
1.B 2.AD
讲析:1.据电子得失守恒,若酸碱均过量时,等量的铝应产生等量的氢气,由此推知选项B符合题意。 2.选项B项中,AlCl3滴入NaOH溶液无白色沉淀,后产生沉淀;NaOH滴入AlCl3溶液先产生沉淀后沉淀溶解。选项C项 NaAlO2溶液滴入H2SO4先无沉淀、后出现白色沉淀, H2SO4溶液滴入NaAlO2溶液先有沉淀后溶解。
20. V(CO2)=10mL
V(CO) =10mL
V(O2)=10mL
19. 22.4mL 44.8mL. CO2+2NaOH=Na2CO3+H2O
CO2+NaOH=NaHCO3 n(NaCl)=n(NaOH)=0.002mol
m(NaCl)=0.117g.
18. (1)2Cl--2e→Cl2 升高
(2)Ca2++CO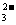 →CaCO3↓ Mg2++2OH-→Mg(OH)2↓
→CaCO3↓ Mg2++2OH-→Mg(OH)2↓
(3) a c
(4)b c
(5) 蒸发 过滤
(6) 2NaCl+2H2O H2↑+Cl2↑+2NaOH
H2↑+Cl2↑+2NaOH
17.
|
|
试剂及操作步骤 |
化学方程式 |
|
NaCl(Na2CO3) |
加足量稀盐酸 |
Na2CO3+2HCl=2NaCl+ CO2↑+H2O |
|
NaOH(Na2CO3) |
加适量Ca(OH)2 过滤 |
Na2CO3+Ca(OH)2 = CaCO3↓+2NaOH |
|
NaCl(Na2SO4) |
加适量BaCl2 过滤 |
Na2SO4+BaCl2= BaSO4↓+NaCl |
|
FeSO4(CuSO4) |
加Fe粉 过滤 |
Fe+CuSO4= FeSO4+Cu |
|
KCl(KBr) |
通入Cl2,加CCl4萃取分液 |
Cl2+2KBr= 2KCl+Br2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com