
8. (1)CH3CH2OH CH2=CH2↑+H2O
(1)CH3CH2OH CH2=CH2↑+H2O
CH2=CH2 +Br2→CH2 Br CH2 Br
(2)b中水面会下降,玻璃管中的水面会上升,甚至溢出。
(3)除去乙烯中带出的酸性气体或答二氧化碳、二氧化硫。
(4)①乙烯发生(或通过液溴)速度过快 ②实验过程中,乙烯和浓硫酸的混合液没有迅速达到170℃(或写“控温不当”也可以)
7.(1)A、E(或F)、C
(2)2Na2O2+2H2O=4NaOH+O2↑或2H2O2 = 2H2O+O2↑
(3)取带火星的木条置于集气瓶口,木条复燃,证明已收集满
(4)①C2H2 CaC2和水(或饱和食盐水)
②NH3 浓氨水和CaO
③SO2 Na2SO3和硫酸
④HCl 浓硫酸和浓盐酸
1.C 2.B 3.B 4.D 5.D
讲析:3.观察双球洗气管中的液面,再分析表格中四种气体的溶解度数据,可知是极易溶于水的气体表现的性质。4.制备乙烯用浓硫酸和乙醇;稀硝酸具有强氧化性,与锌反应不可能制得H2;大理石与稀硫酸反应生成的CaSO4微溶,覆盖在大理石的表面,阻止反应继续进行;浓硝酸具有强氧化性,将Na2SO3氧化,不能制得SO2。5.全面分析气体的干燥、收集和尾气处理装置,只有NH3符合。
3.(1)CaC2+2H2O→C2H2↑+ Ca(OH)2
HC≡CH+Br2→
(或HC≡CH+2Br2→ )
)
(2)不能 a、c
(3)H2S Br2+H2S = S↓+2HBr
(4) c b
(CuSO4溶液) (CuSO4溶液)
(5)如若发生取代反应,必定生成HBr,溶液酸性将会明显增强,故可用pH试纸验证。
检测提高
2.C 讲析:由铜元素守恒,可知C正确。H2还原CuO的实验操作要求是:先通入H2排空气,加热反应后得到的Cu要在H2流中冷却,所需H2比反应消耗的H2要多,则A、B、D不正确。
1.(1)①③⑤;②④⑦⑧ (2)①③⑥,A
(3)①②③④⑥⑧,B (4)⑥
讲析:气体的收集方法有:①向上排空气法(收集密度比空气大的气体);②向下排空气法(收集密度比空气小的气体);③排水集气法(收集难溶于水的气体)。
利用两导气管的长短可判断采用何种收集方法。
7.(2)g接a,b接c,d接e,f接h。或g接c,d接a,b接e,f接h。
(3)上;用燃着的木条放在瓶口,若火焰熄灭,则证明CO2已经充满。
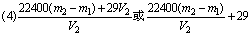 (5)偏低:因为含有H2S、HCl、H2O等杂质气体的式量均小于CO2的式量。
(5)偏低:因为含有H2S、HCl、H2O等杂质气体的式量均小于CO2的式量。
第46课时 (B卷)
纠错训练
6. (1)出现浑浊
(1)出现浑浊
 ONa+CO2+H2O→
OH+NaHCO3
ONa+CO2+H2O→
OH+NaHCO3
(2)紫红色褪去 CaC2+2H2O→Ca(OH)2+C2H2↑
(3)出现浑浊,最后消失
Ag++NH3·H2O→AgOH+NH4+
AgOH+2NH3·H2O=Ag(NH3)2++OH-+2H2O
(4)防止液体倒吸
1.C 2.B 3.D 4.C 5.C
讲析:1.实验室制备气体要操作简单,容易分离,经济实惠,切实可行。甲烷在高温下才能分解成H2和C,实验室难以办到。赤热的炭与水蒸气反应生成CO和H2,难以分离。4.加热固体,试管口应略向下倾斜(A、B错),NH3、NO2溶于水或与水反应(B、D错)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com