
6.在25℃,101kPa条件下,将15 L O2通入10 L CO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气中V(CO)= L, V(H2)= L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气中V(CO)︰V(H2)= 。
(3)若剩余气体的体积为aL,则a的取值范围是 。
(此题旨在考查有关混合物计算、过量计算和运用假设法等的综合计算问题。答题时要认真审题,正确书写相关的化学方程式,以不足量的反应物来进行计算。)
5.在100mL含等物质的量的HBr和H2SO3的溶液里通入0.01molCl2,有一半Br- 变为Br2(已知Br2能氧化H2SO3)。原溶液中HBr和H2SO3的浓度都等于( )
A.0.4mol•L-1 B.0.008mol•L-1
C.0.075mol•L-1 D.0.08mol•L-1
(此题旨在考查学生运用电子守恒法进行计算。答题时要考虑HBr和H2SO3两种还原剂被氧化的先后顺序。)
4.Mg、Al、Fe三种金属的混合物与足量的稀硫酸反应,生成2.80LH2(标准状况),则三种金属的物质的量之和不可能是( )
A.0.120mol B.0.15mol
C.0.0800mol D.0.100mol
(本题考查学生运用假设法进行计算。答题时要根据反应方程式所体现的量之间的关系,通过假设确定取值范围,进而作出判断。)
3.将15 L NO2通过水后(未完全反应)可收集到7 L气体(体积均在同温、同压下测定),被氧化的NO2有
A.4 L B.6 L C.8 L D.12 L
(该题旨在考查学生运用差量法进行计算。答题时由反应前后气体体积的差量关系列式计算。)
2.碳酸铜和碱式碳酸铜均可溶于盐酸,转化为氯化铜。在高温下这两种化合物均能分解成氧化铜。溶解28.4g上述混合物,消耗1mol/L盐酸500mL。灼烧等质量的上述混合物,得到氧化铜的质量是
A.35g B.30 g C.20 g D.15 g
(本题考查的是依据反应方程式进行有关计算的问题。答题的关键是利用元素守恒,找出反应物间量的关系。)
1.


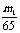 将m1g锌加到m2g20%HCl溶液中去,反应结果共放出nL氢气(在标准状况下),则被还原去的HCl的物质的量是( )
将m1g锌加到m2g20%HCl溶液中去,反应结果共放出nL氢气(在标准状况下),则被还原去的HCl的物质的量是( )
A. mol B. mol C. mol D. mol
(此题考查有关过量计算问题。答题时要认真审题,确定计算依据。)
3.某化工设计院承担新科硫酸厂的设计任务,该厂要求:①为了控制污染和提高生产效率,不再使用黄铁矿,改用固体硫为原料。
②改二次送风(鼓入空气)为一次送风,即送风后使硫充分燃烧,并在下一步催化氧化时不再补充空气。
③每天生产98%H2SO4 a t。
④送风机每天输送空气的体积为b m3/台(标准状况)。
求:(1)每天消耗纯度为95%的固体硫多少吨?
(2)理论上至少应安装多少台送风机?
(3)固体硫充分燃烧后的混合气体中氧气的体积分数ψ(O2)的下限为多少(转化过程不考虑损耗;固体硫中杂质与空气不反应;空气中氧气的体积分数为21%)?
(试题考查的内容涉及硫酸工业生产的基本知识和有关气体摩尔体积、利用反应方程式等的计算。解答此题时要对燃烧反应前后气体体积之间的关系以及对题干中ψ(O2)的下限的含义有清楚的理解,方可列式求算。)
新活题网站
2.( 2002年高考科研试测题)现有等物质的量的NaHCO3、KHCO3的混合物a g与100mL盐酸反应。题中涉及的气体体积均以标准状况计,填空时可以用带字母的公式表示。
(1)该混合物中NaHCO3与KHCO3的质量比为 。
(2)如碳酸氢盐与盐酸恰好完全反应,则盐酸的物质的量浓度为 mol·L-1。
(3)如果盐酸过量,生成CO2的体积为 L。
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道 。
(5)若NaHCO3和KHCO3不是以等物质的量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积范围是 。
(本题意在考查学生利用化学方程式,进行有关混合物计算及过量计算。解答此题的关键在于审清题意,正确书写发生反应化学方程式,确定所需反应物之间量的关系,从而求得结果。)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com