
17.由氧元素的两种同位素16O和18O所形成的两种气体单质
18Om和16On,在同温同压同体积时,中子数之比为5:6。求:
⑴m:n值为多少? ⑵18Om对16On的质量比是多少?
(本题综合考查构成原子的微粒之间的关系,答题时抓住
质量数=质子数+中子数)
第8课时 原子结构(B卷)
易错现象
16.某元素同位素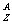 X的氯化物XCl21.11g配成溶液后,需用1mol/L的AgNO3溶液20mL,才能把氯离子完全沉淀下来。已知同位素中有20个中子,求:⑴计算X的质量数是多少?⑵指出X在周期表中的位置(周期、族)。⑶把X单质放在水中,有何反应现象?滴入的酚酞呈现什么颜色?写出有关的化学方程式。
X的氯化物XCl21.11g配成溶液后,需用1mol/L的AgNO3溶液20mL,才能把氯离子完全沉淀下来。已知同位素中有20个中子,求:⑴计算X的质量数是多少?⑵指出X在周期表中的位置(周期、族)。⑶把X单质放在水中,有何反应现象?滴入的酚酞呈现什么颜色?写出有关的化学方程式。
(本题综合考查原子结构的相关知识,答题时抓住质量数为
同位素的相对原子质量的近似整数值)
15.6C元素与某非金属元素R形成化合物CRn,已知CRn的分
子中各原子核外最外层电子数之和为32,核外电子总数为
42,则R为什么元素?n值等于多少?写出化合物CRn的化
学式。
(本题综合考查核外电子及其相关知识,答题时注意列数学
表达式讨论分析)
14.今有A、B、C、D四种元素,其中A元素是1826年一位
法国青年科学家发现的。他在研究海水制盐时,往剩余的副
产物苦卤中通入氯气后发现溶液颜色变深,若经进一步提
取,可得一种红棕色液体,有刺鼻的臭味。B、C、D的原子
电子层排布均不超过3个电子层。D原子核内的质子数正好
等于C原子核内质子数的2倍,而它们最外电子层上的电子
数恰好相等。D原子的最内电子层上电子数则是B原子核外
电子数的2倍。四种元素分别为:
A_____,B______,C______,D______。
由上述某元素的单质与另两种元素的化合物反应生成两种
酸的化学方程是 。
(本题主要考查据原子结构特征推断元素,答题时注意运用
讨论分析,并能正确表达化学用语)
13.原子核外N层最多可容纳______个电子;当N层为最外
层时最多可容纳______个电子;当N层为次外层时最多可容
纳______个电子。
(本题考查核外电子排布规律)
12.画出下列各微粒的结构示意图:
⑴与Ne原子电子层结构相同的-2价阴离子__________;
⑵最外层电子数为次外层电子数两倍的原__________;
⑶L层电子数为K层、M层电子数之和的原子__________;(本题考查微粒结构示意图的书写,答题时注意规范)
11.某元素最外层电子数是次外层电子数的a(a>1)倍,则该原子核内的质子数是 ( ) ( )
A. 2a B. a +2 C. 2a +10 D. 2a +2
(本题考查核外电子排布规律,答题时按电子层数分析讨论)
10.X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,下列叙述中,正确的是 ( )
A.X的质子数比Y的小
B.X原子的最外层电子数比Y的大
C.X元素的最高正价比Y的小
D.X是金属元素,而Y是非金属元素
(本题考查微粒结构与元素性质间的关系)
9.某金属元素R的某种原子的质量数为52,已知该原子
的离子中含有28个中子,21个电子,则由这种离子组成的
化合物的化学式正确的是 ( ) ( )
A. RCl2 B. R(OH)3
C. R2(SO4)3 D. K2R2O7
(本题考查离子所带电荷数多少,答题时主要考虑该离子的化合价)
8.下列叙述中,正确的是 ( ) ( )
A. 两种粒子,若核外电子排布完全相同,则其化学性质一定相同
B. 凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C. 两原子,如果核外电子排布相同,则一定属于同种元素
D. 阴离子的核外电子排布一定与比它原子序数小的稀有
气体元素原子的核外电子排布相同
(本题考查粒子结构特征,答题时注意一般情况和特例)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com