
6.氢化钠(NaH)是一种离子晶体,它与水反应生成碱和H?2,现有NaH和Al粉混合物m(g),与 足量的水充分反应放出n(g)气体.
求下列条件下混合物中Al的质量
(1)x≥y(设NaH x mol,Al y mol)
(2)x<y
知识点:Al粉与其他混合物的反应
能力点:信息迁移能力
5.有一不纯的Mg条0.8g(杂质不能燃烧,且不溶于盐酸),在空气中充分燃烧,然后将生成物溶于50ml、1.8mol/L盐酸中,当往此溶液中加入0.2 mol/L的NaOH溶液90ml时,正好中和多余的盐酸,如再加入碱液360ml并加热,不但Mg2+完全沉淀,且放出134.4mlNH3(标准状况)
求:(1)写出有关反应式或离子反应式(7个)
(2)NH3多少摩?
(3)Mg3N2多少摩?
(4)MgO多少摩?
(5)Mg条中Mg的质量分数
知识点:镁及其化合物的一系列反应
能力点:阶梯发散思维.
4.不另加固体或液体物质,如何使含有a mol Al3+的A溶液中的铝元素和含有b mol AlO2-的B溶液中的铝元素全部转化为Al(OH)3沉淀?
知识点:NH3与Al3+,CO2与AlO2-的反应。
能力点:分解发散能力。
3.向一个铝制易拉罐充满CO2气,然后往罐内注入足量的NaOH溶液,立即用胶布严封罐口,不多会儿听到罐内“卡卡”作响,发现易拉罐变瘪,再过一会易拉罐又鼓起来.
①易拉罐变瘪的原因 ,反应的离子反应式 ;
②易拉罐又鼓起来的原因 ,离子反应式
知识点:铝与碱液的反应
能力点:将理论知识运用于实际生活的能力.
2.已发现的一百多种元素里,大约有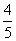 是金属元素,其中:
是金属元素,其中:
(1)自然界中,最活泼的金属元素是 ;
(2)熔沸点最低的金属元素是 ;
(3)质量相同时,与足量的酸反应,放出H2的量最多的金属是 ;
(4)第三周期氧化性最强的离子是
知识点:从不同角度分析金属有关性质.
能力点:综合能力
1.今有四种处于固态的物质:钠、硅、氖、氯化钠.问下列四项性质的叙述各属于哪种物质 ?(1)由分子间力结合而成,熔点很低.
(2)电的良导体,熔点在1000℃左右.
(3)由共价键组成的网状原子晶体.
(4)非导体、但熔融后可以导电.
知识点:晶体类型与物理性质间的关系.
能力点:概括能力、判断能力.
3.铝盐溶液与强碱溶液的反应.
(1)向AlCl3溶液中滴加NaOH溶液
①现象:白色沉淀 沉淀增加
沉淀增加 减少
减少 消失
消失
②有关反应:
Al3++3OH- Al(OH)3↓
Al(OH)3↓
Al(OH)3+OH-  AlO-2+2H2O
AlO-2+2H2O
(2)向NaOH溶液中滴加AlCl3溶液
①现象:沉淀 立刻消失,沉淀
立刻消失,沉淀 沉淀增加
沉淀增加 沉淀量不变
沉淀量不变
②有关反应:
Al3++3OH-
 Al(OH)3↓
Al(OH)3↓
Al(OH)3+OH- AlO-2+2H2O
AlO-2+2H2O
Al3++3AlO-2+6H2O
 4Al(OH)3↓
4Al(OH)3↓
2.Al(OH)3的两性
在溶液中同时发生酸式电离和碱式电离.
Al(OH)3
 H3AlO3
H3AlO3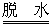 HAlO2+H2O
HAlO2+H2O

碱式电离
Al3++3OH- AlO-2+H+
若向此溶液中加入酸,因H+与OH-结合生成水,反应向碱式电离方向进行,此时Al(OH)3是碱性,若加入碱,因OH-与H+结合生成水,故向酸式电离方向进行,这时Al(OH)3显酸性.
Al(OH)3溶解度很小,无论酸式或碱式电离的程度都很小,其碱性略强于酸性,故仍属于弱碱.
1.铝与强碱溶液反应的实质
反应过程:
2×3e

2Al+6H2O 2Al(OH)3↓+3H 2↑
2Al(OH)3↓+3H 2↑
2Al(OH)3+2NaOH 2NaAlO2+4H2O
2NaAlO2+4H2O
2×3e

总反应式:
2Al+2H2O+2NaOH  2NaAlO2+3H2↑
2NaAlO2+3H2↑
Al与水很难反应,且生成的Al(OH)3附在Al的表面,阻止了Al继续反应,但强碱NaOH能溶 解Al(OH)3,故可促使Al与强碱液反应,而弱碱如氨水,不溶解Al(OH)3,故Al在弱碱溶 液中不反应.
3.受热分解
Mg(OH)2  MgO+H2O
MgO+H2O
2Al(OH)3 Al2O3+3H2O
Al2O3+3H2O
实验室制法
可溶性镁盐加NaOH溶液 Mg2++2OH-
 Mg(OH)2↓
Mg(OH)2↓
可溶性铝盐加氨水 Al3++3NH3·H2O Al(OH)3↓+3NH+4
Al(OH)3↓+3NH+4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com