
1.使君从南来,王马立踟蹰。( )
A.青丝为笼系,桂枝为笼钩
B.行者见罗敷,下担捋髭须
C.少年见罗敷,脱帽著头
D.头上倭堕髻,耳中明月珠;缃绮为下裙,紫绮为上襦
4.皆言夫婿殊:( )
A.出色,与众不同B.矮小C.除外D.小妹
3.使君谢罗敷:( )
A.感谢B.辞别C.致谢D.请问
2.五马立踟蹰:( )
A.象蜘蛛一样 B.如立柜形状
C.徘徊,停滞不进的样子D.一只足
1.组坐观罗敷:( )
A.座位B.因为,由于C.蹲下D.等待
20、已知氢化锂(LiH)属于离子晶体,LiH跟水反应可以放出氢气,下列叙述正确的是( )
A、LiH的水溶液显中性 B、LiH是一种强氧化剂
C、LiH中的氢离子可以被还原成氢气 D、LiH中氢离子与锂离子的核外电子排布相同
(1)X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的化学式可表示为
A、XY B、XY2 C、XY3 D、X2Y3
(2)氢化钠(NaH)是一种白色的离子晶体,其中钠是+1价,NaH与水反应放出氢气,下列叙述中正确的是
A、NaH在水中显酸性 B、NaH中氢离子的电子层排布与氦原子相同
C、NaH中氢离子半径比锂离子半径大 D、NaH中氢离子可被还原成氢气
(3)氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有氢气生成,下列叙述不正确的是( )
A、NH4H是离子化合物 B、NH4H溶于水所形成的溶液显酸性
C、NH4H与水反应时,NH4H是氧化剂
D、NH4H固体投入足量水中,有两种气体生成
(4)下列叙述正确的是
A. 金属阳离子被还原后,一定得到该元素的单质
B. 失电子难的原子获得电子的能力一定强
C. 含有最高价元素的化合物不一定具有强的氧化性
D. 阳离子只有氧化性,阴离子只有还原性
19.(2008·海南高考题)A、B、C、D、E均 为有机化合物,它们之间的关系如下图所示(提示:RCH===CHR′在酸性高锰酸钾溶液中反应生成RCOOH和R′COOH,其中R和R′为烷基)。
为有机化合物,它们之间的关系如下图所示(提示:RCH===CHR′在酸性高锰酸钾溶液中反应生成RCOOH和R′COOH,其中R和R′为烷基)。
→\x(B――→,\s\up7(NaHCO3
回答下列问题:
(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其余为氧元素,则A的分子式为 __________;
__________;
(2)已知B与NaHCO3溶液完全反应,其物质的量之比为1?2,则在浓硫酸的催化下,B与足量的C2 H5OH发生反应的化学方程式是__________,反应类型为:__________;
H5OH发生反应的化学方程式是__________,反应类型为:__________;
(3)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是__________;
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有__________种,其相应的结构简式是__________。
解析:A的式量小于90,其中ω(O)=0.186,则A中氧的式量少于90×0.186=16.56,所以A中只含一个O原子,可求出A的式量为16/0.186=86。利用式量求分子式的方法可求得A的分子式为C5H10O。由于C与C2H5OH发生酯反应生成C4H8O2,求得C是CH3COOH,所以B分子中含3个C原子。但B中与NaHCO3反应之比为1?2,可求得B中含2个-COOH,确定B的结构简式为HOOCCH2COOH。A与Na反应产生H2,说明A中含-OH,能使溴的CCl4溶液褪色,说明A含 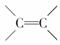 ,结合(1)(2)问可确定A的结构简式为CH3CH===CHCH2CH2OH,其中-OH也可被酸性KMnO4溶液氧化成-COOH。
,结合(1)(2)问可确定A的结构简式为CH3CH===CHCH2CH2OH,其中-OH也可被酸性KMnO4溶液氧化成-COOH。
答案:(1)C5H10O
(2)HOOC-CH2-COOH+2C2H5OH浓硫酸△C2H5OOC-CH2-COOC2H5+2H2O
酯化反应(或取代反应)
(3)HO-CH2-CH2-CH===CH-CH3
(4)2 CH3CH2CH2COOH、CH3CH(CH3)COOH
18.A、B、C都是含C、H、O、N四种元素的有机化合物。1 mol A隔绝空气经加热分解后得到1 mol B和1 mol CO2,且有机物的质量减少了29.53%,B是天然蛋白质水解的最终产物,经红外线光谱分析得到,B分子结构中不含甲基,除-COOH外,还含有一个-OH。C属于硝酸酯类化合物,又是B的同分异构体。
完成下列问题:
(1)A的相对分子质量是__________。
(2)B的结构简式是__________________。
(3)C可能的几种结构简式是__________________。
解析:根据题意知1 mol A隔绝空气经加热分解后得到1 mol B和1 mol CO2,且有机物的质量减少了29.53%,则可求出A和B的相对分子质量。
设A的相对分子质量为M。
A―→ B + CO2
M M-44
1 0.7047
=
解得M=149,则B的相对分子质量为105,因为B是天然蛋白质水解的最终产物,故B中含有-CH(NH2)COOH的结构,B中不含有甲基,含有一个羟基,所以B的结构简式为HOCH2CH(NH2)COOH。由于C是硝酸酯,又是B的同分异构体,所以C中含有-ONO2的结构,且含有3个碳,含有3个碳原子的烃基的结构简式有2种:正丙基和异丙基,因此C有两种同分异构体,分别为CH3CH2CH2ONO2,(CH3)2CHONO2。
答案:(1)149 (2)HOCH2CH(NH2)COOH
(3)CH3CH2C H2ONO2、(CH3)2CHONO2
H2ONO2、(CH3)2CHONO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com