
20.将23.9 g表面已锈蚀成铜绿(Cu2(OH)2CO3)的铜片投入120 mL一定浓度的硝酸中,充分反应后,硝酸被还原成NO2和NO,反应后溶液中H+为0.160 mol。往反应后的溶液中加入过量的NaOH溶液,滤出沉淀,洗涤,干燥后得到29.4 g蓝色固体。求:(1)铜片中单质铜的质量分数;(2)铜片与硝酸充分反应后,溶液中NO3-的物质的量浓度(假设反应前后溶液的体积不变)。
19.某课外小组欲通过实验证明方铅矿分解所得白色粉末中含有氧元素,设计以下的实验装置:
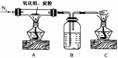
在实验或改进实验中,可能发生的化学反应如下:
PbO+C Pb+CO↑,2 PbO+C
Pb+CO↑,2 PbO+C 2Pb+CO2↑,
2Pb+CO2↑,
Ca(OH)2+CO2=CaCO3↓+H2O
[Cu(NH3)2]Ac+CO+2NH3 [Cu(NH3)4]Ac·CO △H<0。请回答以下问题:
[Cu(NH3)4]Ac·CO △H<0。请回答以下问题:
(1)在装置A中不断鼓入氮气的作用是 ,能否用空气代替氮气? ,其理由是 。
(2)在实验过程中,未见B装置中有白色沉淀生成,说明在装置A中发生反应的化学方程式是 ,证明氧化铅里含有氧元素的实验事实是 。
(3)若使实验更具有说服力,通过增添设备和药品,设计一个更加严密的改进实验方案是 。
(4)若没有木炭粉和氮气,改用氢气行吗? ,实验的装置和药品又将做怎样的调整?____________。
18.已知A、B、C、D、E为中学化学常见物质,A、B、C、D、E中均含有同一种元素,A、C均为气体,E为液体,下图中箭头上的反应物和反应条件均已略去。

(1)当A与E反应生成B和C时,则A、E共同含有乙元素。生成的C气体易液化。常温常压下D是气体,冰水冷却D时变成无色晶体,此无色晶体的化学式是 。根据所学的氧化还原反应知识判断:在A~E各物质中,在一定条件下能与D发生氧化还原反应的物质有 (填字母)。D溶于纯净的E时,能按物质的量比1:1化合,生成物的化学式可表示为 (写成化合物、复合物或氧化物形式均可)。试描述气体C的物理性质________________________________。
2)当A与E发生化合反应时,能观察到空气中形成大量的白烟,则A、E共同含有甲元素。通过上述描述可知:A的化学式为 ,E的化学式为 。当小心加热A与E化合时的生成物F时,可得到一种无色无味的气体G(G和CO2具有相同的原子数目和电子数目)和一种无色无味的液体H,写出F分解生成的G+H的化学方程式 。
17.试依据下列事实,作出有关的结论。
(1)硅的非金属性特征大于金属特征,而锗的金属特征大于非金属特征,________________________________。(2)金刚石是电的绝缘体,石墨可以导电,而C60可作为制超导体材料,________________________________。
(3)在常温下硅的化学性质不活泼,但自然界中却没有单质硅存在,_____________________________________。
(4)硅酸钠溶液中通入CO2气体时,可生成难溶于水的酸-硅酸,_______________________________________。
(3)碳单质的三种同素异形体:骨架型的金刚石、层型的石墨及球形的球碳分子,试确定那一种物质易在火山喷发口附近发现,_________________________________。
16.氰(CN)2的结构式为N≡C-C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素。(CN)2和水反应可生成HCN和HCNO;(CN)2的氧化性比Br2弱,比I2强。
(1)下列有关反应的化学方程式不正确的是
(填选项标号)。
A.(CN)2和NaOH溶液反应:
(CN)2+2NaOH==NaCN+NaCNO+H2O
B.MnO2和HCN反应:
MnO2+4HCN Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C.向KCN溶液中加入碘水:I2+2KCN==2KI+(CN)2
D.在NaBr和KCN混合溶液中通入少量Cl2:
Cl2+2NaBr==2NaCl+Br2
(2)HCN的电子式为 ,按电子云重叠方式分类分子内化学键类型为_________________,碳原子的杂化类型为____________。
(3)处理含CN-(其中C为+2价)的工业废水常用ClO-氧化,生成的CNO-(其中C 为+4价)元素,反应的离子方程式如下:
aCN-+bClO-+cOH-=dCNO-+eN2↑+fCO32-+bCl-+cH2O
上述化学方程式可能的配平系数有多组,请回答:
①方程式中e : f的值为 (填选项标号)。
A.1 B.1/2 C.2 D.不能确定
②若d=e=1, 则b= 。
15.(1)少量的Mn2+可以催化分解H2O2,其反应的机理可简单解释为:
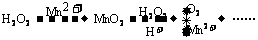
试写出上述2步反应的离子方程式_________________
_______________________________________________。
(2)对于CO中毒、心肌梗塞、冠心病或小儿肺炎等危重患者都要采用吸氧治疗。普通医务室中没有氧气瓶,但一般都有消毒用的30%的H2O2溶液。同时还有可选用的试剂为:KMnO4、HCl、H2SO4、MnO2、Mg、CuSO4、NaCl、葡萄糖。请写出一种使H2O2中氧完全释放出来的理想反应方程式______________________________。
14.NH3和O2混合气体100mL通过红热的铂丝,充分反应后的混合气体再通过足量水最终收集到10mL残留气体,则原混合气体中O2体积不可能是(气体体积在相同条件下测定)
A.12.5mL B.21.5mL C.64.2mL D.70.0mL
13.下列离子方程式不正确的是
A.银氨溶液中加入足量盐酸产生沉淀:
[Ag(NH3)2]++OH-+3H++Cl-=AgCl↓+2NH4++H2O
B.在亚硫酸钡沉淀中加入稀硝酸后,沉淀不溶解:
3BaSO3+2H++2NO3-=3BaSO4↓+2NO↑+H2O
C.碳酸钠溶液中通入少量SO2:
2CO32-+SO2+H2O=2HCO3-+SO32-
D.氧化铁可溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O
12.用浓硫酸吸收SO3可以得到H2SO4•SO3。用mg98%的H2SO4充分吸收SO3后再进行稀释,可得到98%的硫酸的质量为
A.2.42mg B.2.22mg C.2.02mg D.1.98mg
11.次氯酸盐最大的用途是漂白和消毒。这类漂白剂氧化能力是以“有效氯”的含量来标志。“有效氯”的含量定义为:从HI中氧化出相同量的I2所需Cl2的质量与指定化合物的质量之比,常以百分数表示。请问纯LiClO的“有效氯”为
A.121% B.100% C.89% D.21%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com