
2.废水中的氮常以含氮有机物、氨、硝酸盐及亚硝酸盐等形式存在。生物处理的方法是先将大多数有机态氮转化为氨态氮,然后通过进一步转化成N2而消除污染。生物除氮工艺有以下几种方法:
[方法一]在好氧条件下,通过好氧硝化菌的作用,将废水中氨态氮转化为中间过渡形态的硝酸态氮和亚硝酸态氮,然后在缺氧条件下,利用反硝化菌,硝酸态氮和亚硝酸态氮被水中的有机物还原为氮气。见图中之①。反应过程为如下(注:有机物以甲醇表示;当废水中有机物不足时,需另外投加有机碳源)。
2NH4++3O2=2HNO2+2H2O+2H+ 2HNO2+O2=2HNO3
6NO3-+2CH3OH→6NO2-+2CO2+4H2O
6NO2-+3CH3OH→3N2+3CO2+3H2O+6OH-
[方法二]与方法一相比,差异仅为硝化过程的中间过渡形态只有亚硝酸态氮。见图中之②。
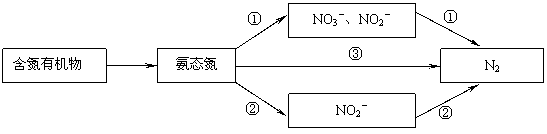 请回答以下问题:
请回答以下问题:
⑴ NH4+的空间构型为 。大气中的氮氧化物的危害有 和 等。
⑵ 方法一中氨态氮元素1g转化为硝酸态氮时需氧的质量为 g。
⑶ 从原料消耗的角度说明方法二比方法一有优势的原因: 。
⑷ 自然界中也存在反硝化作用,使硝酸盐还原成氮气,从而降低了土壤中氮素营养的含量,对农业生产不利,农业上可通过松土作业,以防止反硝化作用。其原因是 。
⑸ 荷兰Delft大学Kluyver生物技术实验室试验确认了一种新途径。在厌氧条件下,以亚硝酸盐作为氧化剂,在自养菌作用下将氨态氮(氨态氮以NH4+表示)氧化为氮气(见图中过程③)。其反应离子方程式为 。
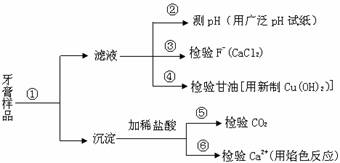
1.牙膏是生活必需品。下面是牙膏中某些主要成分的检验流程图,。
 请回答下列问题:
请回答下列问题:
(1)在①中加水、搅拌、静置后,接下来的实验操作名称是 ,所需要的主要玻璃仪器有 。
(2)在②中用pH试纸测溶液的pH的操作方法是 。
(3)写出④中发生反应的化学方程式: 。
(4)将⑤中放出的气体通入澄清的石灰水中时,未见沉淀出现,则可能的原因是 、 (任答两条)。
(5)在⑥中检验Ca2+的存在,除可用焰色反应外,还可利用Ca2+和 溶液的反应来进行。
17.(15分) 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。
应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
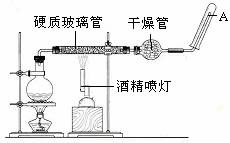
请回答该实验中的问题。
(1)写出该反应的反应方程式: ;并指明该氧化还原反应的还原剂是 ,氧化剂是 。
(2)实验前必须对整套装置进行气密性检查,操作方法是 。
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是 ;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 。
(4)酒精灯和酒精喷灯点燃的顺序是 ,为什么? 。
(5)干燥管中盛装是的物质是 ,作用是 。
(6)试管中收集气体是 ,如果要在A处玻璃管处点燃该气体,则必须对该气体进行 ,方法是 。这一操作的目的是 。
16.在铝质易拉罐中收集满CO2气体,然后在其中倒入10mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,能够观察到的实验现象是易拉罐突然变瘪了,可经过一段时间之后,又可以观察到的现象是 。试解释易拉罐变瘪的原因 ;并解释后一现象的原因 。写出反应过程中的两个离子方程式 ; 。
15.取黄豆粒大小的一块金属钠,用滤纸擦干其表面的煤油,然后加入到硫酸铜溶液中,观察实验现象并写出化学方程式:①钠在溶液中反应的实验现象 ,反应的化学方程式是 。②溶液中的实验现象 ;反应的化学方程式是 。
14.取两份等量的铝粉,分别与足量的盐酸、浓氢氧化钠溶液反应,在相同状态下产生的气体体积之比是 ( )
A.1:1 B.1:2 C. 1:3 D. 3:2
13.一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H2 0.2g,则被氧化的钠是 ( )
A.9.2g B.10.6g C.6.2g D.4.6g
12.下列反应的离子方程式书写正确的是 ( )
A.钠和冷水反应 Na+2H2O=Na++2OH-+H2↑
B.金属铝溶于氢氧化钠溶液 Al+2OH-=AlO2-+H2
C.金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑
D.铁跟稀硫酸反应:Fe+2H+=Fe2++H2
11.若在加入铝粉能放出H2的溶液中,分别加入下列各组离子,肯定不能共存的是
A. Fe3+、NO3-、Cl-、Na+ B.Ba2+、Mg2+、HCO3-、AlO2-(95上海)
C.NO3-、Na+、K+、CO32- D.NO3-、K+、AlO2-、OH-
10.钾(K)与Na在性质上具有很大的相似性,但K比Na的活泼性强,下面是根据Na的性质对K的性质的预测,其中正确的是 ( )
A.因为K的活泼性强,所以钾应该保存在煤油
B.K在空气可以被空气中的氧气所氧化,且在任何条件下产物都是K2O
C.K 与水能够反应,但不如Na与水的反应剧烈,但产物都有氢气
D.K可以与水剧烈反应,生成氢气
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com