
2. 2006年3月,温家宝指出“抓好资源节约,建设环境友好型社会”,这是我国社会和经济长期发展的重要保证。2008年4月22日是第39个“世界地球日”,中国邮政已发行的世界地球邮票(如右图)号召人们关爱地球。下列行为中不利于地球保护的是
2006年3月,温家宝指出“抓好资源节约,建设环境友好型社会”,这是我国社会和经济长期发展的重要保证。2008年4月22日是第39个“世界地球日”,中国邮政已发行的世界地球邮票(如右图)号召人们关爱地球。下列行为中不利于地球保护的是
A.大量开采煤、石油及天然气以满足工业发展的需要
B.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
C.研制开发以水代替有机溶剂的化工涂料
D.研发可降解塑料或替代用品,控制白色污染
1.下列有关说法不正确的是
A.可以利用电解的方法,从海水中获取淡水资源
B.以海水为原料,制备金属镁的过程中,一定发生了氧化还原反应
C.由铝土矿提取铝的过程中,不涉及置换反应
D.人类探月工程的目的之一是获取月球上的He-3资源
3.摄影工艺中废定影液的pH<7,其中含有银的化合物,为了回收银进行如下操作:向盛有废定影液的烧杯中,加入少量稀NaOH溶液,再加入硫化钠溶液生成黑色沉淀,过滤,将固体移入坩埚中,加碳酸钠和硼砂(催化剂)混合加热,放出二氧化碳和氧气。将残留的固体用水洗涤,即得到固体银,而洗涤液中主要含有硫化钠,试回答下列问题:
(1)开始时为何要向废液中加入少量NaOH溶液?
(2)操作中产生的黑色沉淀物质是什么?
(3)写出加热时坩埚内发生反应的化学方程式。
[课后巩固]
2.在NH3、HNO3、H2SO4的工业生产中,具有的共同点是
A.使用吸收塔设备 B.使用尾气吸收装置
C.使用H2作原料 D.使用催化剂
1.下列说法摘自一些科普杂志或广告用语,你认为没有科学性错误的是
A.化学家采用玛瑙研砵磨擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐
B.夏天到了,游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛
C.“白雪牌”漂粉精,令所有化学物质黯然失“色”,没有最白,只有更白
D.硅的提纯与应用,促进了半导体元件与集成芯片业的发展,可以说“硅是信息技术革命的催化剂”
3.自然资源的综合利用
(1)工业上从海水中提取溴的过程如下:
2Br-+Cl2=Br2+2Cl-,Br2+3Na2CO3= 5NaBr+NaBrO3+2CO2
5NaBr+NaBrO3+3H2SO4=3Na2SO4+3Br2+3H2O
(2)以海水为原料制备金属镁:
MgCl2+Ca(OH)2=Mg(OH)2+CaCl2,
Mg(OH)2+2HCl=MgCl2+2H2O,MgCl2 Mg+Cl2↑
Mg+Cl2↑
(3)从铝土矿中提炼金属铝:2Al2O3 4Al+3O2↑
4Al+3O2↑
(4)工业制氯气及烧碱:原理:2NaCl+2H2O 2NaOH+Cl2↑+H2↑原料:纯净的饱和食盐水;设备:离子交换膜电解槽;其他:食盐水的精制;离子交换膜的作用及特点。
2NaOH+Cl2↑+H2↑原料:纯净的饱和食盐水;设备:离子交换膜电解槽;其他:食盐水的精制;离子交换膜的作用及特点。
(5)硫酸的工业制法
4FeS2+11O2 2Fe2O3+8SO2(沸腾炉内进行)
2Fe2O3+8SO2(沸腾炉内进行)
2SO2+O2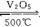 2SO3(接触室中进行)
2SO3(接触室中进行)
SO3+H2O=H2SO4(在吸收塔内用98.3%的浓H2SO4吸收)
(6)硝酸的工业制法:
氨催化氧化成NO(氧化炉):
4NH3+5O2 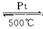 4NO+6H2O
4NO+6H2O
HNO3的生成(吸收塔)2NO+O2===2NO2,3NO2+H2O===2HNO3+NO↑(放出的NO被氧化再被吸收)得到50%的HNO3,经Mg(NO3)2或浓H2SO4处理再蒸馏浓缩,可得96%以上的浓HNO3。
(7)玻璃工业
Na2CO3+SiO2 Na2SiO3+CO2↑
Na2SiO3+CO2↑
CaCO3+SiO2 CaSiO3+CO2↑
CaSiO3+CO2↑
[典型例析]
例1:下列有关环境问题的说法正确的是
A.燃煤时加入适量石灰石,可减少废气中SO2的量
B.臭氧的体积分数超过10-4%的空气有利于人体健康
C.pH在5.6~7.0之间的降水通常称为酸雨
D.含磷合成洗涤剂易于被细菌分解,故不会导致水体污染
变式训练:
六价铬对人体有毒,含铬废水要经过化学处理后才能排放。方法是用绿矾(FeSO4·7H2O)把废水中的六价铬还原成三价铬离子,再加入过量石灰水后,使铬离子转化为氢氧化铬(Cr(OH)3)沉淀,其主要反应的化学方程式如下:H2Cr2O7+6FeSO4+6H2SO4==3Fe2(SO4)3+Cr2(SO4)3+7H2O。现用上法处理1×104 L含铬(+6价)78 mg·L-1的废水(Cr的相对原子质量为52),试回答:
(1)处理后沉淀除Cr(OH)3外,还有__(用化学式来表示)。
(2)需要用绿矾多少千克?
例2:已知某一硅酸盐可表示为Mga(Si4O10)(OH)b(其中a、b为正整数)。试问:
(1)a与b应满足的关系____________(填写表达式);
(2)a能否等于2?________(填“能”“不能”“无法确定”);
(3)分别写出a=4和b=6时硅酸盐的表达式_______(以氧化物的形式表示)。
变式训练:
下列有关新型高分子材料的说法不正确的是
A.高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工、酿造业等
B.复合材料一般是以一种材料作为基体,另一种材料作为增强剂
C.导电塑料是应用于电子工业的一种新型有机高分子材料
D.合成高分子材料制成的人工器官都受到人体的排斥作用,难以达到生理相容的程度
例3:下图是从铝土矿X中提取其主要成分的两种相互结合的方案,已知A为红褐色沉淀,D、F为白色沉淀,F经两次失水转化为G,Ⅰ、Ⅱ、Ⅲ、Ⅳ是相同的操作。

(1)操作Ⅰ的名称是__________,
(2)X的主要成分是________、_______、 (用氧化物的化学式表示)。
(3)写出下列转化的离子方程式:
B+C→D___________________________;
N→F ___________________________。
(4)要使X的利用率最高,则方案一与方案二所取矿石的质量比为__________。
(5)两方案结合的优点是 。
变式训练:
工业上从海水中提取溴采用下列方法:(1)向海水中通入Cl2,将海水中的溴化物氧化,其离子方程式为: 。
(2)向上述混合液中吹入热空气,将生成的溴吹出并用纯碱溶液吸收使其生成NaBr、NaBrO3,其化学方程式为 。(3)将(2)所得溶液用H2SO4酸化,使NaBr、NaBrO3中的溴转化为单质溴,再用有机溶剂提取溴后还可得到副产品Na2SO4,写出这一过程的化学方程式 。(4)这样得到的溴中还混有少量Cl2,怎样除去?
[当堂反馈]
2.材料
(1)新型无机材料:新型无机材料按其在使用中的作用和要求可分为结构材料和功能材料。结构材料主要是应用于具有耐高温、耐化学腐蚀的坚固耐用材料;功能材料是利用其所具有的特殊的力学、热学、光学、磁学及化学性质来完成特定功能的材料。如新型超导材料、纳米材料等。
(2)新型有机材料:新型有机材料是近年来大量合成的一类新型化学材料。它具有密度较小,强度较高,弹性、可塑性、绝缘性和耐腐蚀性好等优点。新型有机材料主要有塑料、合成纤维和合成橡胶等。合成新型有机材料的方法通常有加聚反应和缩聚反应。通过加聚反应合成的其单体一般含有不饱和碳原子(含C==C等)。通过缩聚反应合成的其单体一般含有-OH、-COOH、-NH2等官能团,且在合成过程中会脱去小分子物质(H2O、HCl等)。
(3)建议在复习过程中关注以下话题:金属;非金属;合金;半导体;超导材料;光导纤维;人造宝石;玻璃;水泥;纳米材料;航天材料;化学纤维;化学塑料;可降解塑料;陶瓷;高温结构陶瓷;半导体陶瓷;高分子导电材料;光功能高分子材料;橡胶;导电橡胶;环境材料;有机玻璃;玻璃钢;碳纤维;建筑材料;耐火材料;高强度材料;耐高温耐腐蚀材料;防弹玻璃;涂料;防水材料;建筑胶粘剂;复合材料;高吸水性树脂;离子交换树脂。
1.环境保护与环境污染
(1)环境污染:主要包括大气污染、水污染、土壤污染、食品污染等,还包括固体废弃物、放射性、噪声等污染。
(2)工业三废:废水、废气、废渣。
(3)常见的环境问题及它们对应的污染物。
|
环境问题 |
污染物 |
|
酸雨 |
SO2(主要)及NOx |
|
光化学烟雾 |
NOx及碳氢化合物 |
|
臭氧空洞 |
氟氯烃及NOx |
|
水体富营养化 |
含氮、磷的化合物 |
|
废旧电池污染 |
废旧电池中的汞、镉、铅等重金属离子 |
|
温室效应 |
主要是CO2,但CO2不算是大气污染物 |
|
白色污染 |
有机物如塑料等 |
①酸雨:pH小于5.6的降水称为酸雨。二氧化硫是导致酸雨的主要污染物:SO2+H2O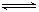 H2SO3,2H2SO3+O2==2H2SO4(主要因素),
H2SO3,2H2SO3+O2==2H2SO4(主要因素),
2SO2+O2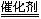 2SO3(催化剂指的是空气中的漂尘),SO3+H2O==H2SO4(次要因素)。
2SO3(催化剂指的是空气中的漂尘),SO3+H2O==H2SO4(次要因素)。
②臭氧层的破坏:一般氮氧化物和氯氟烃在破坏臭氧层的过程中起到催化剂的作用。
③温室效应:CO2、O3、CH4等气体能阻碍由地面反射回高空的红外辐射,这就像给地球罩上了一层保温膜,CO2等气体的过度排放,使地球表面的气温增加,产生温室效应。
(4)中学常见污染环境的气体及其防治
①SO2:工业上用浓氨水吸收,实验室用NaOH溶液吸收。②NOx:用NaOH溶液吸收,也可以用催化还原法。③H2S:用NaOH溶液吸收。④Cl2、Br2、HCl:实验室中常用NaOH溶液吸收,Cl2、Br2还可用Na2SO3吸收。工业上常用石灰乳吸收。⑤CO:用燃烧的方法除去。
39.(60分)环太平洋地区的发展在很大程度上影响着整个世界历史的发展进程,读下列图文资料后回答相关问题:
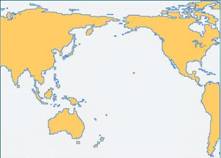
材料一 玉米是世界上分布最广的作物之一,从北纬58度到南纬35-40度的地区均有大量栽培。种植面积最大、总产量最多的国家依次是美国、中国、巴西、墨西哥。美国玉米带主要分布在中部中央大平原,我国玉米带主要分布在东北松辽平原。
材料二 中国东北地区是新中国建国之初重点建设的以重工业为主体的工业基地,在新中国工业发展的初期承担了历史的重任,创造了光荣的历史。2006年,中共中央政府将振兴东北老工业基地拟订为国策。
(1)根据材料一,试比较说明我国东北玉米带与美国玉米带的异同点。(10分)
(2)根据材料二,简述振兴我国东北老工业基地的主要措施。(10分)
材料三 1922年2月6日,美、英、法等九国与中国北洋政府签订了《九国公约》。条约规定:除中国外缔约各国协定,尊重中国之主权与独立暨领土与行政之完整;给予中国完全无碍之机会以发展并维持一有力巩固之政府。施用各国之权势以期切实设立并维持各国在中国全境之商务实业机会均等之原则。不得因中国状况乘机营谋特别权利,而减少友邦人民之权利,并不得奖许有害友邦安全之举动。
-- 摘自刘德斌《国际关系史》
 材料四 开罗会议期间罗斯福和蒋介石进行了多次会晤。罗斯福指出:“中国应取得四强之一的地位,并以平等的身份参加四强小组的机构,参与制订该机构的一切决定。”
“远东问题的关键是中国,美国的远东政策应以中美两国政府密切的工作关系为基础。当我们与俄国发生严重的政策冲突时,中国将毫无疑问地站在我们一边。”会后中关英三国发表的《开罗宣言》指出:“剥夺日本自一九一四年第一次世界大战开始后,在太平洋上所夺得或占领之一切岛屿,及使日本在中国所窃取之领土,如东北四省台湾澎湖列岛等归还中华民国。”
材料四 开罗会议期间罗斯福和蒋介石进行了多次会晤。罗斯福指出:“中国应取得四强之一的地位,并以平等的身份参加四强小组的机构,参与制订该机构的一切决定。”
“远东问题的关键是中国,美国的远东政策应以中美两国政府密切的工作关系为基础。当我们与俄国发生严重的政策冲突时,中国将毫无疑问地站在我们一边。”会后中关英三国发表的《开罗宣言》指出:“剥夺日本自一九一四年第一次世界大战开始后,在太平洋上所夺得或占领之一切岛屿,及使日本在中国所窃取之领土,如东北四省台湾澎湖列岛等归还中华民国。”
--摘自赵志辉《开罗会议新论》
(3)根据材料三,概括《九国公约》确定的对华侵略原则,(4分) 结合所学知识分析《九国公约》对亚太地区政治形势的主要影响。(6分)
(4)根据材料四和所学知识,指出20世纪四五十年代中国国际地位提高的主要表现,(6分)归纳中国国际地位提高的主要原因有哪些。(4分)
材料五 第五届东北亚投资贸易博览会于今年9月1日至6日在吉林召开。吉林省政府为此做了大量的工作:设置2100多个国际标准展位,发布东北亚经贸信息,举办了第五届东北亚经济合作论坛等国际会议,并扎扎实实地做好了博览会期间的安全保卫工作。同时,还举办了大型文艺演出,确保第五届东北亚博览会取得了预期成果。
材料六 在各种大型活动中,越来越多地活跃着志愿者的身影。经过对报名者综合素质进行测试,最终1095名志愿者在东北亚博览会会场内外参与志愿服务。志愿者崇高的奉献精神和国家荣誉感为博览会的成功举办作出了巨大贡献,他们的优质服务得到了参会各国客人和组委会的高度评价。志愿者表示,“我乐于为国家、社会和他人做些事情,奉献的人生最快乐。”
 (5)根据材料五分析吉林省政府在举办东北亚投资贸易博览会中是怎样履行国家职能的?(10分)
(5)根据材料五分析吉林省政府在举办东北亚投资贸易博览会中是怎样履行国家职能的?(10分)
(6)根据材料六,谈谈你对人生价值的理解。(10分)
重庆一中2010届高三年级第一次月考
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com