
16.(6分)已知在一定温度下可发生反应: NO2+SO2==NO+SO3(g),且此反应为不可逆。现将一定温度下的NO和SO2混合气体100 mL通入容积固定的密闭容器中,试回答下列问题。(不考虑NO2转化为N2O4,气体体积均在相同条件下测定)。
(1)若向容器中通入40 mL O2后,容器中才开始出现不再褪去的红棕色,则原混合气体中的体积分数为 。
(2)若向容器中通入V mL O2后,容器中只有NO2和SO3两种气体,则V= mL。
(3)若向容器中通入V mL O2时,要使容器内的压强保持不变,则V的取值范围是 。
15.(6分)某斑铜矿(Cu5FeS4)和黄铜矿(CuFeS2)的混合物按下列流程联合生成铜和硫酸。假定富集后的矿物中只含Cu5FeS4和CuFeS2两种物质,试回答下列问题(假定各步反应均完全)。

若混合物中含Fe1mol,实际生产中第①步消耗氧气_______mol;为使其中的铜全部转化为铜单质,依据配料第②步反应需再充入氧气的物质的量___________(填取值范围)。
14.将amL 0.1mol/L硫酸铝溶液与bmL 0.5mol/L氢氧化钠溶液混合,得到cmol氢氧化铝沉淀,若已知a、b、c中任意两个值,求另一个值,所求的值不止一个解的是(各选项中,单位均已略去)
A.a=100 b=90 c=?
B.a=100 c=0.015 b=?
C.b=90 c=0.015 a=?
D.a=75 c=0.015 b=?
第Ⅱ卷(非选择题,共72分)
13.许多小溪流经煤矿和金属矿,由于含硫矿床暴露在空气中或暴露到含氧的水中,使这些小溪中的水具有酸性,致使溪水中含有大量的硫酸亚铁,它们的浓度都很高。最常见的含硫矿是黄铁矿(FeS2),当富含铁的溪水和其他水混合时,溶于水的铁以针铁矿(FeO(OH))的形式沉淀出来,覆盖小溪的底部,而水仍保持酸性。如果黄铁矿全部转化成FeO(OH)和H+,那么要使1 L纯水的pH降到3.0,消耗FeS2的量为
A.2.5×10-4 mol B.1.25×10-4 mol
C.5×10-4 mol D.1×10-4 mol
12. t℃时,将100 g某物质A的溶液蒸发掉10 g水,恢复至t℃,析出2.5 g晶体;再蒸发掉10 g水,恢复至t℃,析出7.5 g晶体。下列说法中正确的是
A.t℃时原溶液是不饱和溶液
B.若A是CuSO4,则7.5 g晶体中含水2.7 g
C.t℃时A的溶解度为75 g
D.原溶液中A的质量分数为40%
11.有一钠块放置于潮湿空气中,表面氧化变质,但仍为白色块状固体,称其质量为25g,将其全部投入足量水中反应,得到溶液1000mL,并收集到气体2.24L(标准状况下的纯净物),再取此溶液100mL,用1mol/L的盐酸滴定至中性,用去70mL,并将滴定过程中产生的气体通入到足量的澄清石灰水中,得到干燥的沉淀1g,则金属钠的氧化率为
A.71.4% B.81.6% C.18.4% D.28.6%
10.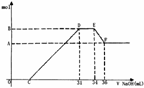 硝酸发生氧化还原反应的时候,一般硝酸浓度越稀,对应的还原产物中氮的化合价越低。现有一定量的铝铁合金与一定量稀HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入4mol /L NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示。下列说法中不正确的是
硝酸发生氧化还原反应的时候,一般硝酸浓度越稀,对应的还原产物中氮的化合价越低。现有一定量的铝铁合金与一定量稀HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入4mol /L NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示。下列说法中不正确的是
A.合金与硝酸反应时硝酸过量
B.合金中铝的物质的量为0.008mol
C.合金中金属的物质的量共为0.032mol
D.无法求出C点的值
9.下列说法正确的是(NA表示阿伏加德罗常数)
A.标准状况下,以任意比例混合的甲烷和丙烷混合物22.4L,则所含有的分子数为NA
B.标准状况下,1L辛烷完全燃烧后,所生成气态产物的分子数为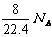
C.常温常压下,活泼金属从盐酸中置换出1molH2时发生转移的电子数为2NA
D.常温常压下,1mol氦气含有的核外电子数为2NA
8. 在25 ℃时向V mLpH=a的盐酸中,滴加pH=b的NaOH(aq)10V mL时,溶液中Cl-的物质的量恰好等于Na+的物质的量,则a+b的值是
A.13 B.14 C.15 D.不能确定
7.右图表示金属X、Y以及它们的合金Z分别与足量盐酸反应时产生氢气的情况,其中横坐标表示消耗金属的物质的量,纵坐标表示产物氢气的体积(标准状况)。下列对有关Z的组成的判断,正确的是
A.n(Na):n(Fe)=2:1 B.n(Mg):n(K)=1:2
C.n(Na):n(Al)=1:3 D.n(K):n(Al)=1:1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com