
1.X、Y、Z分别是三种单质,它们都是常见的金属或非金属.M、N、R是常见的三种氧化物.其中一种具有高熔点,而且有如下反应(条件未标出,方程未配平):
(1)X + Z → N;(2)M+X → N;(3)M+Y→ R+X 。若X是非金属,则组成Y单质的元素在周期表中的位置是
A.第二周期ⅣA族 B.第二周期ⅥA族
C.第三周期ⅡA族 D.第三周期ⅣA族
3.常能发生歧化反应和归中反应的元素有:Cl、Br、I、N、S、Fe、Cu等。
[典型例析]
例1:以下一些氧化物和单质之间可以发生如下图所示的反应:

其中,氧化物(I)是红棕色固体,氧化物(II)、(III)、(IV)在反应条件下都是气体。
(1)氧化物(I)的化学式(分子式)是 。氧化物(II)的化学式(分子式)是 。
(2)反应①的化学方程式是 。
反应②的化学方程式是_________________________。
反应③的化学方程式是_________________________。
变式训练:
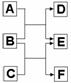 A、B、C、D、E、F六种中学化学中常见的物质,有转化关系(见右图):
A、B、C、D、E、F六种中学化学中常见的物质,有转化关系(见右图):
(1)若A、C、E皆为氧化物,且E为有毒气体,B、D、F皆为非金属单质,且D为气体。则A的结构简式为 ,单质F的晶体类型为 ,1molC中含有 个共价键。
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中C的相对分子质量最小;D、E、F皆为氧化物, 其中D、F为有毒气体。则:
①A、C、E沸点由高到低的顺序为 ,(填化学式);A、C、E三种气态氢化物稳定性最强的是
(填化学式)。
②B跟C反应生成E和F的化学方程式为 。③A跟D常温下反应可生成一种单质,化学方程式为 。
例2:A、B、C、D分别代表硝酸银、偏铝酸钠、稀盐酸、浓氨水四种无色溶液中的一种。甲、乙两同学分别用两两混合的方法进行了如下图所示的实验,现象有的相同,有的不同,不同部分已标出。
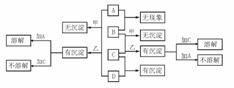
(1)试写出A、B、C、D所代表物质的化学式:
A:________、B:________、C:_______、D:________。
(2)写出B和C按物质的量之比为1:3时反应的化学方程式_____________________。
(3)写出A和D按物质的量之比为3:1时反应的离子方程式_____________________。
变式训练:
化合物A、D、F是中学化学中常见的物质,化合物B、C、E中含有两种相同的元素,这些化合物之间存在如下关系。其中A和B的反应是一种重要化工生产中的主要反应。据此推断:
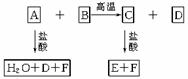
(1)在化合物A、C、F中含有相同的元素是 ;
(2)化合物C的化学式为 、化合物A的水溶液显 性。
(3)C的水溶液和D能否发生反应? ,其理由是 。
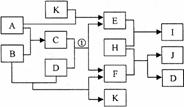 例3:下图中各物质均由常见元素(原子序数≤20)组成。已知A、B、K为单质,且在常温下A和K为气体,B为固体。D为常见的无色液体。I是一种常用的化肥,在其水溶液中滴加AgNO3,有不溶于稀HNO3的白色沉淀产生。J是一种实验室常用的干燥剂。它们的相互转化关系如下图所示(图中反应条件未列出)。
例3:下图中各物质均由常见元素(原子序数≤20)组成。已知A、B、K为单质,且在常温下A和K为气体,B为固体。D为常见的无色液体。I是一种常用的化肥,在其水溶液中滴加AgNO3,有不溶于稀HNO3的白色沉淀产生。J是一种实验室常用的干燥剂。它们的相互转化关系如下图所示(图中反应条件未列出)。
请回答下列问题:
(1)I的化学式为 ;J的电子式为 。
(2)反应①的化学方程式为 。
(3)F的水溶液与氯气反应的离子方程式为 。
变式训练:
下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。

请按要求填空:
(1)I的电子式是_______________;
(2)反应⑥的化学方程式是_______________________,反应③在工业上的一个重要用途是是______________;
(3)已知C的燃烧热是1300 kJ·mol-1,表示C的燃烧热的热化学方程式是____________________________。
(4)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是_________。
[当堂反馈]
2.由
1.由
4. 从数据中去寻找
根据计算或题给信息,可获取某些数据,这些数据也可使我们找到突破口。如物质的熔点较低,说明为分子晶体;反之,则可为离子晶体或原子晶体。
3. 从典型性质寻找
(1)同一元素的气态氢化物和气态氧化物反应,生成该元素的单质和水,元素可能是硫或氮。(2)同一元素的气态氢化物和最高价氧化物对应的水化物化合,生成盐的元素一定是氮。(3)两溶液混合生成沉淀和气体,这两种溶液的溶质可能分别是a.Ba(OH)2与(NH4)2SO4,b.可溶性铝盐与可溶性金属硫化物或可溶性碳酸盐或碳酸氢盐,c.可溶性铁盐与可溶性碳酸盐或碳酸氢盐,d.硫代硫酸盐与强酸(如盐酸、稀H2SO4等)。(4)既能与酸反应,又能与碱反应的物质可能是Al、Al2O3、Al(OH)3、氨基酸,弱酸的铵盐、弱酸的酸式盐等。(5)既能与强酸反应放出气体又能与强碱反应放出气体,常见的物质有:Al,弱酸的铵盐((NH4)2CO3、NH4HCO3、(NH4)2SO3、(NH4)2S、NH4HS等)。(6)在水中分解生成气体和难溶物或微溶物的物质可能是Al2S3、Mg3N2、CaC2等。(7)与水接触放出气体的常见物质有:Li、Na、K、Na2O2、F2等。(8)A物质加到B物质中,先生成沉淀,后沉淀又溶解,A、B可能分别是CO2与Ca(OH)2、NaOH与铝盐、NH3与AgNO3、HCl与NaAlO2、稀盐酸与Fe(OH)3 胶体等。
(9)使溴水褪色的物质有H2S、SO2、不饱和烃类、活泼金属、碱类等。
2. 从反应类型寻找
例如,同一元素的气态氢化物和气态氧化物反应生成该元素的单质和水,则该元素可能为S或N;两种溶液混合生成沉淀和气体,则反应可能为Ba(OH)2与(NH4)2SO4,或可溶性铝盐、可溶性铁盐与可溶性金属硫化物(如Na2S、NaHS)、可溶性碳酸盐、可溶性亚硫酸盐之间的双水解反应;遇水能分解成气体和难溶性物质的可能为Al2S3或Mg3N2;能“三合一”的反应有:NH3+H2O+CO2=NH4HCO3;
4Fe(OH)2+2H2O+O2=4Fe(OH)3;
4NO2+O2+2H2O=4HNO3。常见的一种物质能分解生成三种物质的反应,该物质可能为硝酸盐或NH4HCO3。电解某种盐溶液,能生成一种金属,放出一种气体及另一种物质,则该盐为不活泼金属的含氧酸盐,可为CuSO4、AgNO3等;如有物质发生下列转化关系:A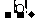 B
B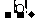 C,则必须对所学基础知识进行全面的总结与梳理,做到胸中有知识网络。如A为无机物单质,则可为C、S、N、Na等;如A为有机物,则可为乙烯或醇类,等等。
C,则必须对所学基础知识进行全面的总结与梳理,做到胸中有知识网络。如A为无机物单质,则可为C、S、N、Na等;如A为有机物,则可为乙烯或醇类,等等。
1. 从物质的组成、结构方面寻找
例如,具有正四面体结构的物质可能为甲烷或白磷或NH4+;不含金属元素的离子化合物为铵盐;组成为A2B2型的物质可能为Na2O2、H2O2、C2H2等。
1.(08枣庄三诊)氮是地球上含量丰富的一种元素,氮及其化合拖把在工农业生产、生活中有着重要作用。请回答:
 (1)右图是1molNO2和1molCO反应
(1)右图是1molNO2和1molCO反应
生成CO2和NO过程中能量变化
示意图,请写出NO2和CO反应
的热化学方程式
。
(2)在一定体积的密闭容器中,进行如
下化学反应:
 N2(g)+3H2(g) 2NH3(g),其化学
N2(g)+3H2(g) 2NH3(g),其化学
平衡常数K与温度t的关系如下表:
|
t/K |
298 |
398 |
498 |
… |
|
K/(mol·L-1)2 |
4.1×106 |
K1 |
K2 |
… |
完成下列问题:
①比较K1、K2的大小;K1 K2(填“>”、“=”或“<”)。
②判断该反应达到化学平衡状态的依据是 (填序号)。
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保护不变
(3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出墁酸肼第一步水解反应的离子方程式 。
②盐酸肼水溶液中离子浓度的排列顺序正确的是 (填序号)。
A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
C.2 c(N2H62+)+ c([N2H5·H2O+])+c(H+)= c(H+)+c(OH-)
D.c(N2H62+)> c(Cl-)>c(H+)>c(OH-)>
8.(08山东二模)可逆反应A(g)+3B(g)
 2C(g);△H<0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是
2C(g);△H<0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是
A.甲中A的转化率为75%
B.甲、乙中C的体积分数相同
C.达到平衡后,再向乙中加入0.25molA、0.75molB、1.5molC,平衡向生成C的方向移动
D.乙中的热化学反应方程式为2C(g)  A(g)+3B(g);△H=+3Q2
kJ·mol-1
A(g)+3B(g);△H=+3Q2
kJ·mol-1

|
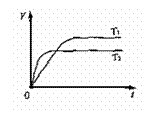 10.(08山东一模)已知反应2SO2(g)+O2(g) 2SO3(g);△H<0。向某体积恒定的密闭容器中按体积比2:1充入SO2和O2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度), Y可以是
( A )
10.(08山东一模)已知反应2SO2(g)+O2(g) 2SO3(g);△H<0。向某体积恒定的密闭容器中按体积比2:1充入SO2和O2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度), Y可以是
( A )
A.SO2的转化率 B.混合气体的密度
C.密闭容器内的压强 D.O2的体积分数
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com