
7. 10mL0.8mol/LMn+өДИЬТәЈ¬ЗЎәГДЬіБөн30mL0.4mol/LCO2Јӯ3өДИЬТәЈ¬ФтnОӘЎЎЎЎЎЎЎЎЎЎ (ЎЎ )
A. 1ЎЎЎЎ ЎЎЎЎЎЎB. 2 ЎЎЎЎЎЎЎЎC. 3ЎЎ ЎЎЎЎЎЎЎЎD. 4ЎЎЎЎ
6. ·ЦұрУГЕЁ¶И¶јОӘ0.1mol/LNaClөДИЬТәЎўMgCl2ИЬТәЎўAlCl3ИЬТәУлAgNO3ИЬТә·ҙУҰЈ¬ІъЙъЦКБҝПаөИөДВИ»ҜТшіБөнЎЈПыәДХвИэЦЦИЬТәөДМе»эұИОӘЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(ЎЎЎЎ )
A . 1ЎГ2ЎГ3ЎЎЎЎ B.ЎЎ 3ЎГ2ЎГ1ЎЎЎЎ C.ЎЎ 2ЎГ3ЎГ6ЎЎЎЎ D.ЎЎ 6ЎГ3ЎГ2ЎЎ
5. ФЪ9gЛ®ЦРН¶Ил1.15gҪрКфДЖЈ¬ФтЛщөГИЬТәЦРH2O·ЦЧУәНNa+ОпЦКөДБҝұИКЗЎЎЎЎЎЎ (ЎЎЎЎ )
A. 10ЎГ1ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ B. 9ЎГ1ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ C. 1ЎГ10ЎЎЎЎЎЎЎЎЎЎЎЎЎЎ C. 90ЎГ1
4. Ҫ«ДЖЎўМъЎўГҫЎўВБёчИЎ0.1molЈ¬·ЦұрН¶ИлЧгБҝөДПЎH2SO4ЦРЈ¬ід·Ц·ҙУҰәуЈ¬·ЕіцөДЖшМе(ЎЎ )
A. ДЖЧо¶аЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ B. Т»Сщ¶аЎЎЎЎЎЎЎЎЎЎЎЎ C. МъЧо¶аЎЎЎЎЎЎЎЎЎЎЎЎ D. ВБЧо¶а
3. NAҙъұн°ў·ьјУөВВЮіЈКэЈ¬ПВБРЛө·ЁХэИ·өДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(ЎЎЎЎ )
A. 16gСхЖшЛщә¬өДСхФӯЧУКэОӘ2NA
B. 18gЛ®Лщә¬өДөзЧУКэОӘNA
C. 2.4gҪрКфГҫУлСОЛб(ЧгБҝ)·ҙУҰК§ИҘөДөзЧУКэОӘ0.1NA
D. 17g°ұЖшЛщә¬өзЧУКэДҝОӘ10NA
2. ПВБРЗйҝцЦРә¬ОўБЈКэДҝЧо¶аөДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(ЎЎ ЎЎ)
A.
1mol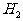 ЦРөДHФӯЧУЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ B. 0.5mol
ЦРөДHФӯЧУЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ B. 0.5mol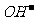 ЦРөДөзЧУ
ЦРөДөзЧУ
C.
0.6mol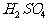 ЦРөДOФӯЧУЎЎЎЎЎЎЎЎЎЎЎЎЎЎ D.
1mol
ЦРөДOФӯЧУЎЎЎЎЎЎЎЎЎЎЎЎЎЎ D.
1mol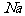 НкИ«·ҙУҰәуК§ИҘөДөзЧУ
НкИ«·ҙУҰәуК§ИҘөДөзЧУ
1. Ул12.8g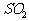 Лщә¬УРФӯЧУКэПаөИөДNOөДЦКБҝОӘЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(ЎЎЎЎ )
Лщә¬УРФӯЧУКэПаөИөДNOөДЦКБҝОӘЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(ЎЎЎЎ )
A. 3.0gЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ B. 6.0gЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ C. 9.0gЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ D. 18.0g
10. (09ДкЙПәЈ»ҜС§ЎӨ31)СМЖшЦРNOxКЗNOәНNO2өД»мәПОп(І»ә¬N2O4)ЎЈ
 (1)ёщҫЭ·ПЖшЕЕ·ЕұкЧјЈ¬1m3СМЖшЧоёЯФКРнә¬400mgNOxЎЈИфNOxЦРNOЦКБҝ·ЦКэОӘ0.85Ј¬Фт1m3СМЖшЦРЧоёЯФКРнә¬NOЎЎЎЎЎЎЎЎЎЎЎЎ
L(ұкЧјЧҙҝцЈ¬ұЈБф2О»РЎКэ)ЎЈ
(1)ёщҫЭ·ПЖшЕЕ·ЕұкЧјЈ¬1m3СМЖшЧоёЯФКРнә¬400mgNOxЎЈИфNOxЦРNOЦКБҝ·ЦКэОӘ0.85Ј¬Фт1m3СМЖшЦРЧоёЯФКРнә¬NOЎЎЎЎЎЎЎЎЎЎЎЎ
L(ұкЧјЧҙҝцЈ¬ұЈБф2О»РЎКэ)ЎЈ
 (2)№ӨТөЙПНЁіЈУГИЬЦКЦКБҝ·ЦКэОӘ0.150өДNa2CO3Л®ИЬТә(ГЬ¶И1.16g/mL)ЧчОӘNOxОьКХјБЈ¬ёГМјЛбДЖИЬТәОпЦКөДБҝЕЁ¶ИОӘЎЎЎЎЎЎЎЎЎЎЎЎ
mol/L(ұЈБф2О»РЎКэ)ЎЈ
(2)№ӨТөЙПНЁіЈУГИЬЦКЦКБҝ·ЦКэОӘ0.150өДNa2CO3Л®ИЬТә(ГЬ¶И1.16g/mL)ЧчОӘNOxОьКХјБЈ¬ёГМјЛбДЖИЬТәОпЦКөДБҝЕЁ¶ИОӘЎЎЎЎЎЎЎЎЎЎЎЎ
mol/L(ұЈБф2О»РЎКэ)ЎЈ
 (3)ТСЦӘЈәNO+NO2+Na2CO3=2NaNO2+CO2ЎЎЎЎ ўЩ
(3)ТСЦӘЈәNO+NO2+Na2CO3=2NaNO2+CO2ЎЎЎЎ ўЩ
 2NO2+Na2CO3=NaNO2+NaNO3+CO2ЎЎ ўЪ
2NO2+Na2CO3=NaNO2+NaNO3+CO2ЎЎ ўЪ
1m3 ә¬2000mgNOxөДСМЖшУГЦКБҝ·ЦКэОӘ0.150өДМјЛбДЖИЬТәОьКХЎЈИфОьКХВКОӘ80%Ј¬ОьКХәуөДСМЖшЎЎЎЎЎЎЎЎЎЎЎЎ
ЕЕ·ЕұкЧј(МоЎ°·ыәПЎұ»тЎ°І»·ыәПЎұ)Ј¬АнУЙЈәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЈ
ә¬2000mgNOxөДСМЖшУГЦКБҝ·ЦКэОӘ0.150өДМјЛбДЖИЬТәОьКХЎЈИфОьКХВКОӘ80%Ј¬ОьКХәуөДСМЖшЎЎЎЎЎЎЎЎЎЎЎЎ
ЕЕ·ЕұкЧј(МоЎ°·ыәПЎұ»тЎ°І»·ыәПЎұ)Ј¬АнУЙЈәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЈ
 (4)јУИлПхЛбҝЙёДұдСМЖшЦРNOәНNO2өДұИЈ¬·ҙУҰОӘЈә
(4)јУИлПхЛбҝЙёДұдСМЖшЦРNOәНNO2өДұИЈ¬·ҙУҰОӘЈә NO+2HNO3ЈҪ3NO2+H2O
NO+2HNO3ЈҪ3NO2+H2O
 өұСМЖшЦРn(NO)©Un(NO2)ЈҪ2©U3КұЈ¬ОьКХВКЧоёЯ
өұСМЖшЦРn(NO)©Un(NO2)ЈҪ2©U3КұЈ¬ОьКХВКЧоёЯ
 1m3СМЖшә¬2000mgNOxЈ¬ЖдЦРn(NO)©Un(NO2)ЈҪ9©U1ЎЈ
1m3СМЖшә¬2000mgNOxЈ¬ЖдЦРn(NO)©Un(NO2)ЈҪ9©U1ЎЈ
 јЖЛгЈә(i)ОӘБЛҙпөҪЧоёЯОьКХВКЈ¬1m3СМЖшРиУГПхЛбөДОпЦКөДБҝ(ұЈБф3О»РЎКэ)ЎЈ
јЖЛгЈә(i)ОӘБЛҙпөҪЧоёЯОьКХВКЈ¬1m3СМЖшРиУГПхЛбөДОпЦКөДБҝ(ұЈБф3О»РЎКэ)ЎЈ
 (ii)1m3СМЖшҙпөҪЧоёЯОьКХВК90%КұЈ¬ОьКХәуЙъіЙNaNO2өДЦКБҝ(јЩЙиЙПКцОьКХ·ҙУҰЦРЈ¬·ҙУҰўЩұИ·ҙУҰўЪСёЛЩЎЈјЖЛгҪб№ыұЈБф1О»РЎКэ)
(ii)1m3СМЖшҙпөҪЧоёЯОьКХВК90%КұЈ¬ОьКХәуЙъіЙNaNO2өДЦКБҝ(јЩЙиЙПКцОьКХ·ҙУҰЦРЈ¬·ҙУҰўЩұИ·ҙУҰўЪСёЛЩЎЈјЖЛгҪб№ыұЈБф1О»РЎКэ)
ҙр°ёЈә
 (1)0.25i
(1)0.25i
 (2)1.64
(2)1.64
 (3)І»·ыәПЎЎ ТтОьКХәуСМЖшЧЬМе»эјхРЎЈ¬NOxә¬БҝИФі¬№э
(3)І»·ыәПЎЎ ТтОьКХәуСМЖшЧЬМе»эјхРЎЈ¬NOxә¬БҝИФі¬№э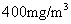
 (4)(i)
(4)(i)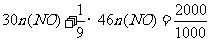 ЎЎЎЎЎЎ n(NO)=0.057mol
ЎЎЎЎЎЎ n(NO)=0.057mol
 ЎЎЎЎЎЎ
NO+2HNO3ЈҪ3NO2+H2O
ЎЎЎЎЎЎ
NO+2HNO3ЈҪ3NO2+H2O
 ЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎ 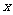 ЎЎЎЎ
ЎЎЎЎ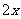 ЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎ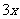
 ЎЎЎЎЎЎ
ЎЎЎЎЎЎ
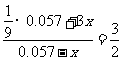 ЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎ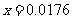 ЎЎЎЎЎЎn(HNO3)=2x=0.035mol
ЎЎЎЎЎЎn(HNO3)=2x=0.035mol
 (ii)
(ii)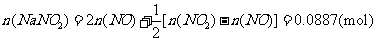
 ЎЎЎЎ
ЎЎЎЎ 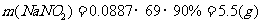

9. (09Дк№г¶«»ҜС§ЎӨ6)ЙиNA ҙъұн°ў·ьјУөВВЮіЈКэ(NA )өДКэЦөЈ¬ПВБРЛө·ЁХэИ·өДКЗ
AЈ®1 mol БтЛбјШЦРТхАлЧУЛщҙшөзәЙКэОӘNA
BЈ®ТТП©әН»·ұыНй(C3H6ЎЎ )ЧйіЙөД28g»мәПЖшМеЦРә¬УР3NA ёцЗвФӯЧУ
CЈ®ұкЧјЧҙҝцПВЈ¬22.4LВИЖшУлЧгБҝЗвСх»ҜДЖИЬТә·ҙУҰЧӘТЖөДөзЧУКэОӘNA
DЈ®Ҫ«0.1molВИ»ҜМъИЬУЪ1LЛ®ЦРЈ¬ЛщөГИЬТәә¬УР0.1NAЎЎ Fe3+
ҙр°ёЈәC
ҪвОцЈә K2SO4ЦРТхАлЧУОӘБтЛбёщЈ¬1molБтЛбёщЛщҙшөзәЙОӘ2molЈ¬AҙнОуЎЈТТП©әНC3H6өДЧојтКҪПаН¬ҫщОӘCH2Ј¬28g»мәПЖшУР2molCH2Ј¬ЛщТФә¬4molHФӯЧУЈ¬BҙнОуЎЈFe3+ФЪИЬТәЦР·ўЙъЛ®ҪвЈ¬0.1molFeCl3ИЬТәЦРЈ¬Fe3+өДОпЦКөДБҝТӘРЎУЪ0.1molЈ¬DҙнОуЎЈ
8. (09ДкҪӯЛХ»ҜС§ЎӨ4)УГNAұнКҫ°ў·ьјУөВВЮіЈКэөДЦөЎЈПВБРРрКцХэИ·өДКЗ
 AЈ®25ЎжКұЈ¬pH=13өД1.0L Ba(OH)2ИЬТәЦРә¬УРөДOHЈӯКэДҝОӘ0.2NA
AЈ®25ЎжКұЈ¬pH=13өД1.0L Ba(OH)2ИЬТәЦРә¬УРөДOHЈӯКэДҝОӘ0.2NA
 BЈ®ұкЧјЧҙҝцПВЈ¬2.24L Cl2Ул№эБҝПЎNaOHИЬТә·ҙУҰЈ¬ЧӘТЖөДөзЧУЧЬКэОӘ0.2NA
BЈ®ұкЧјЧҙҝцПВЈ¬2.24L Cl2Ул№эБҝПЎNaOHИЬТә·ҙУҰЈ¬ЧӘТЖөДөзЧУЧЬКэОӘ0.2NA
 CЈ®КТОВПВЈ¬21.0gТТП©әН¶ЎП©өД»мәПЖшМеЦРә¬УРөДМјФӯЧУКэДҝОӘ1.5NA
CЈ®КТОВПВЈ¬21.0gТТП©әН¶ЎП©өД»мәПЖшМеЦРә¬УРөДМјФӯЧУКэДҝОӘ1.5NA
 DЈ®ұкЧјЧҙҝцПВЈ¬22.4L јЧҙјЦРә¬УРөДСхФӯЧУКэОӘ1.0NA
DЈ®ұкЧјЧҙҝцПВЈ¬22.4L јЧҙјЦРә¬УРөДСхФӯЧУКэОӘ1.0NA
 ҙр°ёЈәC
ҙр°ёЈәC

 ҪвОцЈәAПоЈ¬pH=13ТІҫНКЗТвО¶ЧЕc(H+)=1ЎБ10-13molЎӨL-1Ј¬Фтc(OH-)=1ЎБ10-1molЎӨL-1Ј¬ЛщТФn(OHЈӯ)=n(OHЈӯ)ЎБV=1ЎБ10-1molЎӨL-1ЎБ1L=0.1molЈ¬ЛщТФN(OHЈӯ)=0.1NAЈ»BПоЈ¬·ўЙъөД»ҜС§·ҙУҰ·ҪіМКҪОӘCl2+2NaOH=NaCl+NaClO+H2O(ёГ·ҙУҰОӘЖз»Ҝ·ҙУҰ)Ј¬n(Cl2)=0.1molЈ¬ДЗГҙЧӘТЖөзЧУөДКэДҝУҰёГОӘ0.1NAЈ»CПоЈ¬ТТП©әН¶ЎП©өДЧојтКҪ¶јКЗCH2Ј¬Фтn(CH2)=
ҪвОцЈәAПоЈ¬pH=13ТІҫНКЗТвО¶ЧЕc(H+)=1ЎБ10-13molЎӨL-1Ј¬Фтc(OH-)=1ЎБ10-1molЎӨL-1Ј¬ЛщТФn(OHЈӯ)=n(OHЈӯ)ЎБV=1ЎБ10-1molЎӨL-1ЎБ1L=0.1molЈ¬ЛщТФN(OHЈӯ)=0.1NAЈ»BПоЈ¬·ўЙъөД»ҜС§·ҙУҰ·ҪіМКҪОӘCl2+2NaOH=NaCl+NaClO+H2O(ёГ·ҙУҰОӘЖз»Ҝ·ҙУҰ)Ј¬n(Cl2)=0.1molЈ¬ДЗГҙЧӘТЖөзЧУөДКэДҝУҰёГОӘ0.1NAЈ»CПоЈ¬ТТП©әН¶ЎП©өДЧојтКҪ¶јКЗCH2Ј¬Фтn(CH2)=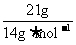 =1.5molЈ¬ЛщТФn(C)=01.5molЈ¬N(C)=1.5NAЈ»DПоЈ¬ұкЧјЧҙҝцПВЈ¬јЧҙјОӘТәМ¬Ј¬ДЗГҙјЧҙјөДОпЦКөДБҝҫНІ»КЗ1molЈ¬ФтЛщә¬УРөДСхФӯЧУёцКэТІІ»ОӘNAЎЈ
=1.5molЈ¬ЛщТФn(C)=01.5molЈ¬N(C)=1.5NAЈ»DПоЈ¬ұкЧјЧҙҝцПВЈ¬јЧҙјОӘТәМ¬Ј¬ДЗГҙјЧҙјөДОпЦКөДБҝҫНІ»КЗ1molЈ¬ФтЛщә¬УРөДСхФӯЧУёцКэТІІ»ОӘNAЎЈ
 [ҝјөг·ЦОц]ТФ°ў·ьЩӨөВВЮіЈКэОӘФШМеҝјІмИзПВЦӘК¶өгўЩҝјІй22.4L/molөДХэИ·К№УГЈ»ўЪҝјІйФЪСх»Ҝ»№Фӯ·ҙУҰЦРөГК§өзЧУКэөДјЖЛгЈ»ўЫХэИ·ұнКҫТ»¶ЁОпЦКөДБҝөДДіОпЦКОўБЈЛщә¬ДіЦЦОўБЈөДёцКэЈ»ўЬҝјІйФЪұкЧјЧҙҝцПВТ»¶ЁМе»эөДЖшМе·ЦЧУЛщә¬өД·ЦЧУКэәНФӯЧУКэЎЈ
[ҝјөг·ЦОц]ТФ°ў·ьЩӨөВВЮіЈКэОӘФШМеҝјІмИзПВЦӘК¶өгўЩҝјІй22.4L/molөДХэИ·К№УГЈ»ўЪҝјІйФЪСх»Ҝ»№Фӯ·ҙУҰЦРөГК§өзЧУКэөДјЖЛгЈ»ўЫХэИ·ұнКҫТ»¶ЁОпЦКөДБҝөДДіОпЦКОўБЈЛщә¬ДіЦЦОўБЈөДёцКэЈ»ўЬҝјІйФЪұкЧјЧҙҝцПВТ»¶ЁМе»эөДЖшМе·ЦЧУЛщә¬өД·ЦЧУКэәНФӯЧУКэЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com