
(三)卤素单质的化学性质(相似性及递变性)
由于最外层均为 个电子,极易 电子,因此碱金属都是 剂,但随着电子层数递增,原子半径渐 ,核对最外外层电子的引力渐 ,失电子能力渐 ,其还原性逐渐 。
试题枚举
[例1]:把小块金属钠分别投入饱和NaCl溶液、NH4Cl溶液、FeCl3的烧杯里的现象和反应?
|
|
现象 |
化学方程式 |
|
饱和NaCl |
|
|
|
饱和NH4Cl |
|
|
|
FeCl3溶液 |
|
|
(二)单质的物理性质
随碱金属元素核电荷数增加,原子结构的递变而使碱金属单质的物理性质呈规律性变化.
归纳:从Li →Cs
1.除 外,颜色都是 且都较 ,密度都比较 ,且呈 趋势, 熔趋势沸点逐渐(原因是 。)
2.焰色反应
钠的焰色是 ,钾的焰色是
(一)碱金属元素的原子结构
共同点:原子的最外层均为 个电子,都易 1个电子而表现 性;
不同点:核电荷数逐渐 ;电子层数逐渐 ;原子半径依次 ,得电子能力逐渐 ;单质还原性逐渐 。
3.Na2CO3与NaHCO3比较与鉴别
(1)Na2CO3与NaHCO3比较
|
名 称 |
碳酸钠 |
碳酸氢钠 |
|
|
俗 名 |
|
|
|
|
主要性质 |
色态 |
|
|
|
水溶性 |
|
|
|
|
稳定性 |
|
|
|
|
与H+反应 |
|
|
|
|
与碱NaOH和Ca(OH)2反应 |
|
|
|
|
主要用途 |
|
|
|
|
相互转化 |
|
|
思考:Na2CO3溶液与盐酸作用时,滴加顺序不同,现象一样吗?
(2)根据上叙性质用多种方法区别Na2CO3与NaHCO3
2.氢氧化钠(俗称: 、 、 )
(1)电子式: ,所含化学键为 、
(2)物理性质:有很强的 性,易 (用作 剂),溶于水时会 。
(3)化学性质:具有 碱性。
(4)制法(工业制法):
(5)保存:溶液 ; 固体 。
1.11、氧化钠和过氧化钠的比较
|
|
氧化钠 |
过氧化钠 |
|
化学式 |
|
|
|
氧元素的化合价 |
|
|
|
电子式 |
|
|
|
阴阳离子个数比 |
|
|
|
化合物类型 |
|
|
|
颜色状态 |
|
|
|
与H2O反应的方程式 |
|
|
|
与CO2反应的方程式 |
|
|
|
用途 |
|
|
2.钠的化学性质
Na - e- → Na+ 化学反应中表现为 性
(1)与非金属单质的反应(写出下列方程式)
a.与氯气反应:
b.与硫反应 :
c.与氧气反应①常温下,现象: 化学方程式:
②加热时,现象: 化学方程式:
(2)与水的反应、与醇、酚、羧酸等含-OH的有机物反应。
a.与水反应现象:
化学方程式:
思考:钠与水反应的现象说明钠具有哪些性质?
b.与乙醇反应 现象:
化学方程式: 。
c.与乙酸反应 : 。
(3)与稀酸溶液的反应
与盐酸反应 。
(4)与某些盐的反应
a.与熔融盐 Na+TiCl4 。
b.与盐溶液 (CuSO4溶液) 。
思考:钠在空气中放置一段时间,将发生哪些变化?最终产物是什么?如何保存?
1.钠的物理性质
钠是 色有 的 体,硬度较 , 低,密度比水 。
钠元素位于周期表__周期__族,自然界中钠只能以 的形态存在,主要以
的形式存在。
22.(本题10分)已知函数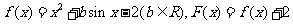 ,且对于任意实 数
,且对于任意实 数 ,恒有
,恒有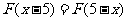 。
⑴求函数
。
⑴求函数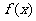 的解析式;
⑵已知函数
的解析式;
⑵已知函数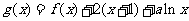 在区间
在区间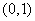 上单调,求实数
上单调,求实数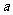 的取值范围;
⑶函数
的取值范围;
⑶函数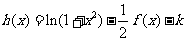 有几个零点?
有几个零点?
附加题:(本题5分,计入总分,总分超出100分时算100分
若 求证:
求证: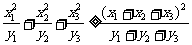 ,当且仅当
,当且仅当 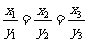 时等号成立;
时等号成立;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com