
26.(16分,每空2分)前20号主族元素W.X.Y.Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍。X,Y,Z分属不同的周期,它们的原子序数之和是W原子序数的5倍。元素Y形成晶体的晶胞属于六方最紧密堆积,在由元素W,X,Y,Z组成的所有可能的二元素化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W原子的电子排布式为 , W3分子中只有两个σ键,判断W3分子的空间构形是 。
(2)X元素氢化物的熔点比它下一周期同主族元素氢化物的熔点高的原因是 。
(3)化合物M的电子式为 , 其晶体结构与NaCl相同,而熔点高于NaCl,M熔点较高的原因是 。在化合物M的晶胞中,和Y离子距离最近且相等的W离子有 个,在空间形成 形。
(4)X、Y、Z可形成立方晶体的化合物,其晶胞中X占有棱的中心,Y位于顶角,Z位于体心位置,则该晶体的组成为X:Y:Z= 。
24.(6分,每空2分)某无色溶液若滴加盐酸产生无色无味能使澄清石灰水变浑浊的气体,若滴加氢氧化钠溶液产生白色沉淀,则①该溶液中一定含有(除OH-)的阴离子是 ,②下列阳离子中可能含有的是(Al3+.Fe3+.Ca2+.Ba2+) ,③欲确定含有哪种阳离子,可以取该无色溶液加入过量的浓盐酸后再滴加含有 (填离子符号)的溶液看是否产生沉淀。
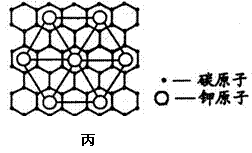
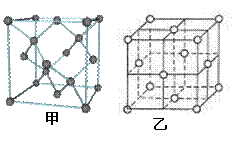
25(9分)如下图甲.乙.丙分别为四种晶体不同结构,
回答下列问题:
(1)甲为金刚石的晶胞示意图,在这个晶胞中含有 个碳原子。在金刚石晶体中,最小的碳原子环为 元环,碳原子在形成共价键时,以 形式杂化成键。12g金刚石晶体中含有的C-C共价键数目为 NA。(4分)
(2)乙为金属晶体中最常见的四种堆积方式之一,属于 型堆积(填“密置层”或“非密置层”),配位数为 ,空间利用率为 。(3分)
(3)石墨能与熔融金属钾作用,形成石墨间隙化合物,K原子填充在石墨各层碳原子中。比较常见的石墨间隙化合物是青铜色的化合物,其化学式可写作CxK,其平面图形见丙图,则x值为 。(2分)
23.(6分,每空1分)在横线上填写合适的除杂试剂和分离方法(萃取分液、过滤、蒸馏、洗气、结晶、升华、蒸发),括号内为杂质。
(1)NaCl溶液(碘) , ;
(2)乙醇(水) , ;
(3)CO2(HCl) , 。
22.(4分)利用右图所示装置收集以下6种气体(图中试管的位置不得变化):
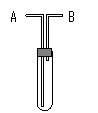 A.H2. B.Cl2. C.CH4. D.CO.
A.H2. B.Cl2. C.CH4. D.CO.
E.NH3. F.NO
(1)若试管是干燥的,则A口进气,可收集的气体
有 。(写序号下同)。
(2)若试管充满水,可收集的气体有A.C.D. ,这时气
体由 口进入。
(3)若在烧瓶内装入无水CaCl2进行气体干燥和收集,气体由B口进入,则可用此装置来干燥和收集的气体有A. 。
21.(本题包括2小题,共4分)化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。
(1)(2分)下列关于实验的叙述正确的有 。
A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
B.用托盘天平称量重11.72g氯化钠晶体
C.用碱式滴定管量取25.00mL酸性KMnO4溶液
D.测量溶液的pH时,应先将PH试纸润湿
E.分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
F.用溴水除去乙烯中混有的二氧化硫气体
G.配制一定物质的量浓度的溶液时,容量瓶必须干燥
(2)(2分)下图为常见仪器的部分结构(有的仪器被放大)
A图中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量一液体的
体积,平视时读数为n mL,仰视时读数为m mL,若m>n,则所使用的仪器是
(填字母标号)。
20.实验室里需用480 mL 0.1mol·L-1的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是 ( )
A.称取7.68g硫酸铜,加入500mL水
B.称取12.0g胆矾配成500mL溶液
C.称取8.0g硫酸铜,加入500mL水
D.称取12.5g胆矾配成500 mL溶液
第Ⅱ卷 非选择题(共55分)
19.下列叙述正确的是 ( )
A.相同条件下,(CN)2和O2的混合气体与等体积的N2所含原子数相等
B.等物质的量的甲基(-CH3)与羟基(-OH)所含电子数相等
C.常温常压下28 g CO与22.4 L O2所含分子数相等
D.16 g CH4与19 g NH4+所含质子数相等
18.某溶液中含有较大量的Cl-.CO32-.OH-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是 ( )
①滴加Mg(NO3)2溶液; ②过滤; 、
③滴加AgNO3溶液; ④滴加Ba(NO3)2溶液
A.①②④②③ B.④②①②③ C.①②③②④ D.④②③②①
17.下列说法正确的是 ( )
A.124g P4含有的P-P键的个数为6NA
B.12g石墨中含有的C-C键的个数为2NA
C.12g金刚石中含有的C-C键的个数为1.5NA
D.60gSiO2中含Si-O键的个数为2NA
16.石英晶体的平面示意图如图所示,它实际上是网状结构,其
中硅.氧原子的个数比是m:n,有关叙述正确的是( )
A.m:n=1:2
B.m:n=2:1
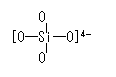 C.六聚硅酸根[Si6O18]y-中的y=10
C.六聚硅酸根[Si6O18]y-中的y=10
D.原硅酸根SiO44-的结构为 ,则二聚硅酸根离子Si2O7x-中的x=8
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com