
26、氢化钠(NaH)是一种白色的离子晶体,其中钠是+1价,NaH和水反应放出氢气,下列叙述中正确的是
(A)NaH在水中显酸性 (B)NaH中氢离子电子层排布与氦原子的相同
(C)NaH中氢离子半径比锂离子大 (D)NaH中氢离子可被还原成氢气
25、AB型的离子化合物中,A、B两种离子的核外电子数之和为20,可知A、B两元素在元素周期表中的周期序数分别为
(A)同在第二周期 (B)第二周期和第三周期
(C)同在第三周期 (D)第三周期和第二周期
24、下列离子化合物中阴、阳离子间距离最大的是
(A)LiCl (B)NaCl (C)KCl (D)KBr
23、与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的化合物是
(A)Na2S (B)CCl4 (C)KCl (D)KF
22、X与Y两元素的单质能反应生成X2Y型离子化合物,若Y为ⅥA族,则X的族序数为
(A)ⅠA (B) ⅡA (C) ⅢA (D) ⅣA
21、下列说法中正确的是
A 两个原子或多个原子之间的相互作用叫做化学键
B 阴阳离子间通过静电作用而形成的化学键叫做离子键
C 只有金属元素和非金属元素化合时才能形成离子键
D 大多数的盐、碱和低价金属氧化物中含有离子键
20、下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是 ( )
A.常温时,A能从水中置换出氢,而B不能
B.a原子电子层数比b原子的电子层数多
C.1mol a 从酸中置换H+生成的H2比1 mol b从酸中置换H+生成的H2多
D.a原子的最外层电子数比B原子的最外层电子数少
19、原子核外电子层数大于5、电子式为 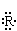 的元素及其单质和化合物不可能具备的性质是
的元素及其单质和化合物不可能具备的性质是
( A )不能形成稳定的气态氢化物 ( B )R的离子的还原性很强
( C )与IIA族元素M形成MR型的离子化合物
( D )R2易与水作用,其反应按下式进行:R2+H2O==HR+HRO翰林汇
18、下列各组原子序数所表示的两种元素,能形成AB2型离子化合物的是 ( )
A. 6和8 B. 11和13 C. 11和16 D. 12和17
17、下列说法正确的是 ( )
A. 离子化合物中可能含共价键 .B. 共价化合物中可能含离子键
C. 离子化合物中只含离子键 D. 共价化合物中一定含离子键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com