
13.(11分)(08年广东化学·19)
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(钝度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺路线如下:
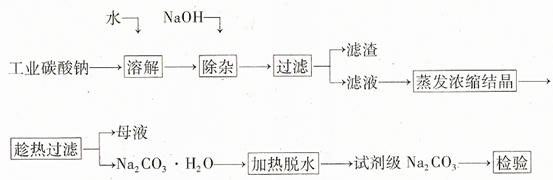
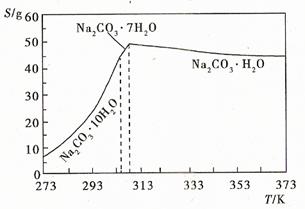
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
 回答下列问题:
回答下列问题:
(1)滤渣的主要成分为 。
(2)“趁热过滤”的原因是 。
(3)若在实验室进行“趁热过滤”,可采取的措施是
(写出1种)。
(4)若“母液”循环使用,可能出现的问题及其原因是 。
(5)已知:
Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH1=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式 。
答案:(1)Mg(OH)2、Fe(OH)3、CaCO3
(2)使析出的晶体为Na2CO3·H2O,防止因温度过低而析出Na2CO3·10H2O晶体,令后续的加热脱水耗时长
(3)用已预热的布氏漏斗趁热抽滤
(4)溶解时有大量沉淀生成,使Na2CO3损耗且产物Na2CO3混有杂质 其原因:"母液"中,含有的离子有Ca2+,Na+,Cl-,SO42-,OH-,CO32-,当多次循环后,使用离子浓度不断增大,溶解时会生成CaSO4,Ca(OH)2,CaCO3等沉淀
(5)Na2CO3·H2O(s)=== Na2CO3(s) + H2O(g)△H= +58.73kJ·mol-1
解析:
(1) 因工业碳酸钠中含有Mg2+,Fe3+,Ca2+,所以“除杂”中加入过量的NaOH溶液,可生成Mg(OH)2、Fe(OH)3、Ca(OH)2沉淀。
(2) 观察坐标图,温度减少至313K时发生突变,溶解度迅速减少,弱不趁热过滤将析出晶体。
(3) 思路方向:1.减少过滤的时间 2.保持过滤时的温度。
(4) 思路:分析“母液”中存在的离子,若参与循环,将使离子浓度增大,对工业生产中哪个环节有所影响。
(5) 通过观察两个热化学方程式,可将两式相减,从而得到Na2CO3·H2O(S)====== Na2CO3(s)+ H2O(g)。
12. (07年山东理综·28)(11分)二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
(07年山东理综·28)(11分)二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g)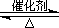 2SO3(g)
2SO3(g)
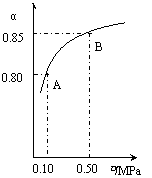
某温度下,SO2的平衡转化率(a)与体系总压强(p)的关系如右图所示。根据图示回答下列问题:
①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于_____。
②平衡状态由A变到B时.平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2整个过程中转移的电子总数为______(阿伏加德罗常数的值用NA表示),放出的热量为______kJ。
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox 3<x<4,M=Mn、Co、Zn或Ni=由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示:
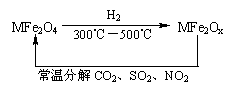

请写出MFe2Ox分解SO2的化学方程式 (不必配平)。
答案:(1)①800L·mol-1 ②= (2)1.60NA(或1.6NA) 173.4 (3)MFe2Ox+SO2→MFe2O4+S
解析:(1)据题意当容器中总压强为0.10MPa时,SO2的平衡转化率为0.80,据此可计算得出平衡时c(SO2)=0.040mol·L-1;c(O2)=0.020mol·L-1;c(SO3)=0.16mol·L-1。根据平衡常数的计算式:K=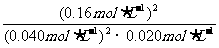 =800L·mol-1;只要温度不变,平衡常数就不改变,在此变化过程中,只有压强的改变,温度未发生变化,故K(A)=K(B)。
=800L·mol-1;只要温度不变,平衡常数就不改变,在此变化过程中,只有压强的改变,温度未发生变化,故K(A)=K(B)。
(2)用标准状况下4.48LCH4还原NO2 至N2,4.48LCH4的物质的量为0.20mol,在此过程中CH4中碳元素的化合价有-4价升高到+4价,转化为CO2,失去电子的总物质的量为0.20mol×8= 1.60mol,故转移电子数为1.60NA。由题目给知的热化学方程式,根据盖斯定律可以得出CH4还原NO2至N2的热化学方程式为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1,则0.2molCH4反应放出的热量为867 kJ·mol-1×0.2mol=173.4kJ。
(3)此题中反应物已知为MFe2OX和SO2,反应后生成MFe2O4,由MFe2OX转化为MFe2O4,氧原子数增加,故SO2失去氧原子转化为S,反应式为:MFe2OX+SO2=MFe2O4+S。
10.(09年广东文基·68)下列说法正确的是
A.废旧电池应集中回收,并填埋处理
B.充电电池放电时,电能转变为化学能
C.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
D.所有燃烧反应都是放热反应,所以不需吸收能量就可以进行
答案:C
解析:A项废旧电池应集中回收但不能填埋处理因为电池里的重金属会污染土地,人吃了这些土地里的蔬菜后,,就会引发疾病;B项充电电池放电时,化学能转变为电能;D项有的燃烧反应是需要吸收一定热量才可以反应的比如碳的燃烧。
[考点分析]垃圾的处理、电化学、影响化学反应速率因素、化学反应与能量。
11 .(09年海南化学·12)已知:Fe2O2(s)+C(s)= CO2(g)+2Fe(s) △H=234.1kJ·mol-1
.(09年海南化学·12)已知:Fe2O2(s)+C(s)= CO2(g)+2Fe(s) △H=234.1kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
 则2Fe(s)+O2(g)=Fe2O3(s)的△H是
则2Fe(s)+O2(g)=Fe2O3(s)的△H是
A.-824.4kJ·mol-1 B.-627.6kJ·mol-1
C.-744.7kJ·mol-1 D.-169.4kJ·mol-1
答案:A
解析: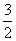 (2)=(1)就可得2 Fe(s)+
(2)=(1)就可得2 Fe(s)+ 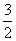 O2(g) = Fe2O3(s),则ΔΗ=
O2(g) = Fe2O3(s),则ΔΗ= ΔΗ2-ΔΗ1=-824.4 kJ·mol-1。
ΔΗ2-ΔΗ1=-824.4 kJ·mol-1。
8.(09年广东理基·26)下列措施不符合节能减排的是
A.大力发展火力发电,解决广东电力紧张问题
B.在屋顶安装太阳能热水器为居民提供生活用热水
C.用石灰对煤燃烧后形成的烟气脱硫,并回收石膏
D.用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气
答案:A
解析:节能减排指的是减少能源浪费和降低废气排放,大力发展火力发电,既不利于节能也不利于减排,故A选项符合题意。其余选项的措施或做法都符合节能减排的原则。
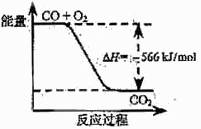
9 .(09年天津理综·6)已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566
kJ/mol
.(09年天津理综·6)已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566
kJ/mol
 Na2O2(s)+CO2(g)=Na2CO3(s)+
Na2O2(s)+CO2(g)=Na2CO3(s)+
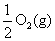 ΔH=-226 kJ/mol
ΔH=-226 kJ/mol
 根据以上热化学方程式判断,下列说法正确的是
根据以上热化学方程式判断,下列说法正确的是
 A.CO的燃烧热为283 kJ
A.CO的燃烧热为283 kJ
 B.右图可表示由CO生成CO2的反应过程和能量关系
B.右图可表示由CO生成CO2的反应过程和能量关系
 C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
 D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
答案:C
解析:A项,燃烧热的单位出错,应为kJ/mol,错;图中的量标明错误,应标为2molCO和2molCO2,故错。CO2气体的能量大于固体的能量,故C项中放出的能量应小于452kJ,而△H用负值表示时,则大于-452Kj/mol,正确;将下式乘以2,然后与上式相加,再除以2,即得CO与Na2O2的反应热,所得热量为57kJ,故D项错。
7.(08年海南化学·8)白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P a kJ·mol-1、P-O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。
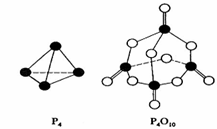
根据图示的分子结构和有关数据估算该反应的△H,其中正确的是A
A.(6a+5d-4c-12b)kJ·mol-1 B(4c+12b-6a-5d)kJ·mol-1
C.(4c+12b-4a-5d)kJ·mol-1
D.(4a+5d-4c-12b)kJ·mol-1
答案:A
解析:由图可以看出:P4中有6mol的P-P,5mol的O2中含有5molO=O,1mol的P4O10中含有4mol的P=O,12mol的P-O,所以△H=(6a+5d-4c-12b)kJ·mol-1。
6.(08年广东化学·14)下列有关能量转换的说法正确的是AB
A.煤燃烧是化学能转化为热能的过程
B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
答案:AB
解析:葡萄糖氧化放出热量,化学能转化为热能,C错;选项D应该太阳能转化为化学能,D错。
5.(08年宁夏理综·13)已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为
A.-44.2 kJ·mol-1 B.+44.2 kJ·mol-1
C.-330 kJ·mol-1 D.+330 kJ·mol-1
答案:A
解析:由题意可知:C2H4(g)+3O2(g) 2CO2(g)+2H2O(l);△H=-1411.0kJ·mol-1,
2CO2(g)+2H2O(l);△H=-1411.0kJ·mol-1,
C2H5OH(1)+3O2(g) 2CO2(g)+3H2O(l);△H=-1366.8kJ·mol-1,将上述两个方程式相减得:C2H4(g)+H2O(l)
2CO2(g)+3H2O(l);△H=-1366.8kJ·mol-1,将上述两个方程式相减得:C2H4(g)+H2O(l) C2H5OH(l);△H=-44.2kJ·mol-1。
C2H5OH(l);△H=-44.2kJ·mol-1。
4.(2007海南·06)已知:
(1)Zn(s)+1/2O2(g)==ZnO(s);ΔH=-348.3kJ/mol
(2)2Ag(s)+1/2 O2(g)== Ag2O(s);ΔH=-31.0kJ/mol
则Zn(s)+ Ag2O(s)== ZnO(s)+ 2Ag(s)的ΔH等于( )
A.-317.3kJ/mol B.-379.3kJ/mol C.-332.8 kJ/mol D.+317.3 kJ/mol
答案:A
考点:本题考查了热化学方程式书写规律。
解析:由已知⑴、 ⑵热化学方程式可知:⑴-⑵ 即可得出答案。
3.(07年广东理基·19)下述做法能改善空气质量的是
A.以煤等燃料作为主要生活燃料
B.利用太阳能、风能和氢能等能源替代化石能源
C.鼓励私人购买和使用汽车代替公交车
D.限制使用电动车
答案:B
解析:以煤等燃料作为主要生活燃料时会产生大量的空气污染物;私人汽车代替公交车会使汽油的消耗量增加,带咯啊的空气污染物增多,限制使用电动车会增加有害气体的排放。因此正确的选项为B
2.(07年广东文基·62)下列说法正确的是
A.需要加热的化学反应都是吸热反应
B.中和反应都是放热反应
C.原电池是将电能转化为化学能的一种装置
D.水力发电是将化学能转化为电能的过程
答案:B
解析:需要加热的化学反应也可能是放热反应,如可燃物的燃烧反应,A选项错误;原电池是将化学能转化为电能的装置,故C选项错误;水力发电是将机械能转化为电能的过程,故D选项错误。正确选项为B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com