
6.(09年广东化学·17)常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+H+下列说法正确的是
A.H2O2的氧化氢比Fe3+强,其还原性比Fe2+弱
B.在H2O2分解过程中,溶液的pH逐渐下降
C.在H2O2分解过程中, Fe2+和Fe3+的总量保持不变
D.H2O2生产过程要严格避免混入Fe2+
答案:CD
解析:由氧化还原反应的强弱律可知,氧化性是氧化剂大于氧化产物,还原性是还原剂大于还原产物,由方程一可知,氧化剂H2O2氧化性比氧化产物Fe3+强,由方程二可知,还原剂H2O2还原性比,原产物为Fe2+强,所以A错误;方程一和方程二相加,即H2O2分解生成H2O和O2,H2O2呈弱酸性,所以随着反应进行,pH升高,B错误;H2O2分解Fe3+或Fe2+作催化剂,所以总量不变,C正确;因为Fe2+可导致H2O2分解,所以H2O2生产过程要避免混入Fe2+,D正确。
5. (09年福建理综·6)下列类型的反应,一定发生电子转移的是
(09年福建理综·6)下列类型的反应,一定发生电子转移的是
 A.化合反应 B.分解反应 C.置换反应 D.复分解反应
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
答案:C
解析:置换反应中肯定有单质参加,一定属于氧化还原反应,即一定有电子转移,C项正确。
4.(08年海南化学·4)锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为D
A.2 mol B.1 mol C.0.5 mol D.0.25 mol
答案:D
解析:此题主要考查氧化还原反应的配平:Zn+HNO3(稀) Zn(NO3)2+NH4NO3+H2O,Zn:0→+2,化合价改变值为:(2-0)×1=2,N:+5→-3,化合价的改变值为:(5+3)×1=8,根据化合价升降总值相等得:在Zn(NO3)2前配4,NH4NO3前配1,然后根据反应前后各元素的原子个数相等,找出其他物质的系数。配平后的化学方程式为:4Zn+10HNO3(稀)===4Zn(NO3)2+NH4NO3+3H2O,当生成1mol的Zn(NO3)2时,被还原的HNO3为0.25mol。
Zn(NO3)2+NH4NO3+H2O,Zn:0→+2,化合价改变值为:(2-0)×1=2,N:+5→-3,化合价的改变值为:(5+3)×1=8,根据化合价升降总值相等得:在Zn(NO3)2前配4,NH4NO3前配1,然后根据反应前后各元素的原子个数相等,找出其他物质的系数。配平后的化学方程式为:4Zn+10HNO3(稀)===4Zn(NO3)2+NH4NO3+3H2O,当生成1mol的Zn(NO3)2时,被还原的HNO3为0.25mol。
3.(08年广东理基·33)氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应:Al2O3+N2+3C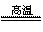 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮的化合价为+3
D.AlN的摩尔质量为41 g
答案:B
解析: 该反应中 N2降价为氧化剂,C升价为还原剂,每生成1molAlN转移3mol电子,AlN中Al为+3价,N为-3价。D中摩尔质量的单位为g/mol。
2.(07年广东化学·5)氯气是一种重要的工业原料。工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应
D.生成1molN2有6mol电子转移
答案:C
解析:本题原理大多同学已在平时练习中接触过,06年高考题实验题21题⑵考到:将NH3通入溴水中,有N2生成,反应的化学方程式为 ,也与此题原理类似属氧化还原反应,故C错。当NH3过量时会与HCl反应生成NH4Cl白烟故A对,反应氯气为氧化剂,NH3为还原剂,氮由-3价升高至0价故生成1molN2有6mol电子转移,D对。
1.(07年山东理综·15)一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O。若用0.1000mol·L-1的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L-1)为
提示:①H2C2O4是二元弱酸
②10KHC2O4·H2C2O4+8KMnO4+17H2SO4=8MnSO4+9K2SO4+40CO2↑+32H2O
A.0.008889 B.0.08000 C.0.1200 D.0.2400
答案:B
解析:此题类型属于信息给予题,据题意并结合提示,H2C2O4为二元弱酸,可写出氢氧化钠与KHC2O4·H2C2O4·2H2O反应的方程式:
6NaOH+2KHC2O4·H2C2O4·2H2O=3Na2C2O4+K2C2O4+8H2O;
10[KHC2O4·H2C2O4]+8KMnO4+ 17H2SO4=8MnSO4+9K2SO4+40CO2+32H2O 。可得关系式:6NaOH~2KHC2O4·H2C2O4·2H2O,10[KHC2O4·H2C2O4]~8KMnO4 ;综合以上两式可得:15NaOH ~ 4KMnO4 , 结合题意:V(NaOH)=3V(KMnO4)可得出关系:
15NaOH ~ 4KMnO4
15 4
3V(KMnO4)×0.1000mol·L-1 V(KMnO4)×c(KMnO4)
列式得:15×V(KMnO4)×c(KMnO4)=4×3V(KMnO4)×0.1000mol·L-1,整理得:0.08000mol·L-1,答案选B。
34.(07年广东化学·23)(11分)
已知某混合金属粉末中,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol·L-1硫酸、2mol·L-2硝酸、2mol·NaOH溶液、20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设:
假设1:该混合金属粉末中除铝外还含有 元素;
假设2:该混合金属粉末中除铝外还含有 元素;
假设3:该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案基于假设3,设计出实验方案(不要在答题卡上作答)。
(3)实验过程
根据(2)的实验方案,叙述实验操作、预期现象和结论。
[提示]Ⅰ.在答题卡上按以下方式作答,注意前后内容对应;
33.(07年广东化学·21)(10分)
以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
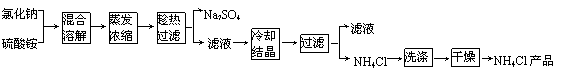

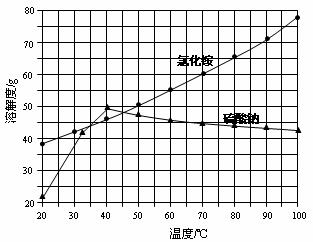
氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需NaCl g。
(2)实验室进行蒸发浓缩用到的主要仪器有 、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为 。
(4)不用其它试剂,检查NH4Cl产品是否纯净的方法及操作是 。
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是 。
答案:(10分)
(1)11.7
(2)蒸发皿
(3)35℃(33~40℃均可得分)
(4)加热法;取少量氯化铵产品于试管底部,加热,若试管底部无残留物,表明氯化铵产品纯净。
(5)重结晶
解析:难度,中,本题考查学生对质量守恒定律的理解以及对化学实验室常用的仪器主要用途的了解,考查学生应用基础知识解决简单化学问题的能力以及学生对图表的观察、分析能力。根据氯守恒可列关系求m(NaCl)= 10.7g·58.5g /mol ¸53.5g/mol=11.7g,氯化铵的溶解度随温度变化较大,而硫酸钠在30~100℃变化不大,故可有冷却结晶法以。但温度不能太低以防硫酸钠析出。所以应大约在33~40℃。
32.(09年海南化学·3)除去NaHCO3溶液中混有的少量Na2CO3可采取的方法是:
A.通入二氧化碳气体 B.加入氢氧化钡溶液
C.加入澄清石灰水 D.加入稀盐酸
答案:A
解析:除杂方法要操作简便、效果好、不带来新的杂质、保留非杂质成份。溶液中可用这样的方法: Na2CO3 + H2O + CO2 = 2NaHCO3。
31.(09年海南化学·1)将等体积的苯、汽油和水在试管中充分混合后静置。下列图示现象正确的是:
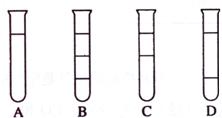
答案:D
解析:题中苯、汽油和水的密度有差别,其中苯和汽油密度比水小,且能互溶,所以分两层,上下层比例为2∶1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com