
5.将下列物质分别加入溴水中,溴水颜色不变浅的是
A.NaOH溶液 B.KI固体 C.CCl4 D.Mg
4.升高温度,下列数据不一定同时增大的是
A.化学反应速率v B.弱电解质的电离平衡常数Ka
C.化学平衡常数K D.水的离子积常数Kw
3.某品牌消毒液的商品标识上注明:①本品为无色液体呈碱性;②使用时应加水稀释;③可对餐具进行消毒,并能漂白浅色衣物。据此判断其有效成分可能是
A.Cl2 B.SO2 C.H2O2 D.NaClO
2.能证明醋酸是弱酸的事实是
A.能溶于水
B.能使紫色石蕊试液变红
C.能被弱碱氨水中和
D.常温下,0.1 mol·Lˉ1醋酸溶液中的c(H+)为1.32×10ˉ3 mol·Lˉ1
1.工业上常用氯气给自来水消毒。某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是
A.碳酸钠 B.硝酸银 C.亚硫酸钠 D.氯化铁
8.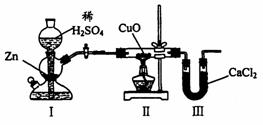 用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H):m(O)>1:8。下列对导致这一结果的原因的分析中,一定错误的是
用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H):m(O)>1:8。下列对导致这一结果的原因的分析中,一定错误的是
A.CuO没有全部被还原
B.I、Ⅱ装置之间缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝
D.Ⅲ装置后缺少干燥装置
7.下列各选项所述的两个量,前者一定大于后者的是
①HF和HBr的沸点,②纯水在25℃和80℃时的pH,③同温下分别在100g水中最多能溶解的无水CuSO5和CuSO5·5H2O的质量,④25℃时,等体积的pH都等于3的盐酸和AlCl3溶液中,已电离的水分子数,⑤在NH3+NO→N2+H2O反应中,被氧化和被还原的N原子数,⑥耐火材料MgO和CaO的熔点,⑦H-和H+离子半径,⑧金刚石晶体和石墨晶体中,每个最小碳环里所含的实际碳原子数
A、①②⑥ B、①②③⑤ C、⑤⑥⑦ D、①②⑥⑦
6.在无土栽培中,需配制一定量含50 mol NH4Cl、16 mol KCl和24 mol K2SO4的营养液。若用KCl、NH4Cl和(NH4)2SO4三种固体为原料来配制,三者的物质的量依次是
A.2mol、64mol、24mol B.16mol、50mol、24mol
C.64mol、2mol、24mol D.32mol、50mol、12mol
5.下列离子方程式正确的是:( )
A.向澄清石灰水中通入过量CO2:OH-+CO2=HCO3-
B.Cu与浓HNO3反应:Cu+4HNO3(浓)=Cu2++2NO3-+2NO2↑+2H2O
C.实验室制氨气:NH4++OH- NH3↑+H2O
NH3↑+H2O
D.Na投入水中:Na+2H2O=Na++2OH-+H2↑
4.金属钾的冶炼可采用如下方法: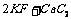 ========
========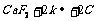 。下列有关说法合理的是
。下列有关说法合理的是
A转移1mol 电子时,生成39g K
B.该反应能说明C的还原性大于K
C.该反应的氧化剂是KF,氧化产物是K
D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2∶1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com