
2.(10分)设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) △H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) △H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)  FeO(s)+H2(g) △H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) △H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
|
T/K |
K1 |
K2 |
|
973 |
1.47 |
2.38 |
|
1173 |
2.15 |
1.67 |
(1)从上表可推断,反应①是________(填“放”或“吸”)热反应;
(2)现有反应③H2(g)+CO2(g)  CO(g)+H2O(g) △H=Q3
CO(g)+H2O(g) △H=Q3
 ①根据反应①与②推导出K1、K2、K3的关系式K3=_____________;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有__________________。
①根据反应①与②推导出K1、K2、K3的关系式K3=_____________;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有__________________。
A.缩小容器体积 B.降低温度
C.使用合适的催化剂 D.设法减少CO的量 E.升高温度
②根据反应①与②推导出Q1、Q2、Q3的关系式Q3=_____________;
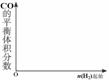
(3)现在恒容密闭容器中通入一定量CO2,再慢慢通入H2,使发生上述反应③,在其他条件不变时,若改变H2的起始量,容器中CO的体积分数也随之改变,使在右图中画出CO的体积分数随n(H2)变化的示意图。
1.(10分)材料是人类赖以生存和发展的重要物质基础,划时代的材料可作为人类文明的里程碑。目前人类使用的材料主要有无机非金属材料、金属材料和有机高分子材料。
回答下列问题: ⑴ 普通玻璃是传统的无机非金属材料。以石英砂、石灰石和纯碱为主要原料,经过高温熔融后,石英砂、石灰石和纯碱转化为Na2SiO3、CaSiO3,再经成型、缓慢冷却后制得。上述过程中,碳酸盐不断转化为硅酸盐的原因是 ;
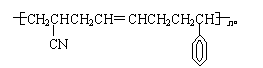 ⑵ 氮化硅(Si3N4)是一种新型无机非金属材料,熔点高、硬度大、化学性质稳定。化学气相沉降法(CVD)是目前生产氮化硅的方法:在H2的保护下,使SiCl4与N2反应生成氮化硅。写出该反应的化学方程式 ▲ ;
⑵ 氮化硅(Si3N4)是一种新型无机非金属材料,熔点高、硬度大、化学性质稳定。化学气相沉降法(CVD)是目前生产氮化硅的方法:在H2的保护下,使SiCl4与N2反应生成氮化硅。写出该反应的化学方程式 ▲ ;
⑶ ABS工程塑料是合成高分子材料,其结构简式为
请写出合成ABS的单体的结构简式 ▲ 。
⑷ 金属铝是人类使用最广泛的金属材料之一,右图为工业冶炼铝的电解槽示意图。
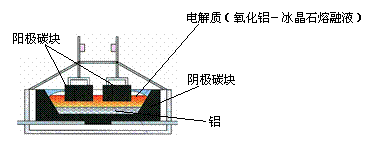
工业冶炼铝的生产过程中,电解槽工作一段时间后,因部分材料不断损耗,需定期更换 ▲ ;生产铝的原料铝土矿中除含有Al2O3外还含有SiO2、Fe2O3。请你设计一个实验方案,从铝土矿中提取Al2O3 ▲ 。
18. C70分子也已经制得,它的分子结构模型可以与C60同样考虑面推知。通过计算确定C70分子中五边形和六边形的数目。
17.通过计算,确定C60分子所含单键数。C60分子所含单键数为 。
16.试估计C60跟F2在一定条件下,能否发生反应生成C60F60(填“可能”或“不可能”)_________________________,并简述其理由:
________________________________________________________。
15.固体C60与金刚石相比较,熔点较高者应是____________,理由是:
_________________________________________________________.
14.如图为NaCl晶体结构图,图中直线交点处为NaCl晶体中Na+与Cl-所处的位置(不考虑体积的大小)。
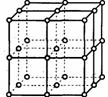
(1)请将其代表Na+的用笔涂黑圆点,以完成 NaCl晶体结构示意图。
(2)确定晶体的晶胞,分析其构成。
(3)从晶胞中分Na+周围与它最近时且距离相等的 Na+共有多少个?
 [拓展提高]
[拓展提高]
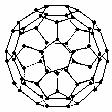
1996年诺贝化学奖授予对发现C60有重大贡献的三位科学家。C60分子是形如球状的多面体(如图),该结构的建立基于以下考虑:
①C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②C60分子只含有五边形和六边形;
③多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:
顶点数+面数-棱边数=2
据上所述,可推知C60分子有12个五边形和20个六边形,C60分子所含的双键数为30。
请回答下列问题:
13.在干冰晶体中每个CO2分子周围紧邻的 CO2分子有___________个 在晶体中截取一个最小的正方形;使正方形的四个顶点部落到CO2分子的中心,则在这个正方形的平面上有___________个C02分子。
12.
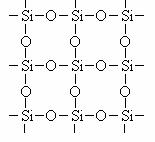 右图是石英晶体平面示意图,它实际上是立体的网状结构,其中硅、氧原子数之比为 。原硅酸根离子SiO44-的结构可表示为
右图是石英晶体平面示意图,它实际上是立体的网状结构,其中硅、氧原子数之比为 。原硅酸根离子SiO44-的结构可表示为
二聚硅酸根离子Si2O76-中,只有硅氧键,它的结构可表示为
。
11.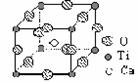 右图是超导化合物----钙钛矿晶体的晶胞结构。请回答:
右图是超导化合物----钙钛矿晶体的晶胞结构。请回答:
(1)该化合物的化学式为 。
(2)在该化合物晶体中,与某个钛离子距离最近且相等的其他钛离子共有 个。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com