
9. 在一定条件下,可逆反应:N2+3H2 2NH3;△H<0
在一定条件下,可逆反应:N2+3H2 2NH3;△H<0
达到平衡,当单独改变下列条件后,有关叙述错误的是( )
A.加催化剂,v正、v逆都发生变化且变化的倍数相等
B.加压,v正、v逆都增大,且v正增大倍数大于v逆增大倍数
C.降温,v正、v逆都减小,且v正减小倍数大于v逆减小倍数
D.加入氩气,v正、v逆都增大,且v正增大倍数大于v逆增大倍数
8. 将A与B的混合气体1
mol放入容积为2 L的密闭容器内,在一定条件下发生反应:2A(g)+3B(g) C(g)+ 2D(g) ,经过4min达到平衡,此时容器内的压强是反应前的3/5,则以各气体的浓度变化表示的反应速率正确的是( )
将A与B的混合气体1
mol放入容积为2 L的密闭容器内,在一定条件下发生反应:2A(g)+3B(g) C(g)+ 2D(g) ,经过4min达到平衡,此时容器内的压强是反应前的3/5,则以各气体的浓度变化表示的反应速率正确的是( )
A.vA=0.050 mol·(L·min)-1
B.vB=0.150mol·(L·min)-1
C.vC=0.025mol·(L·min)-1
D.vD=0.015mol·(L·min)-1
7.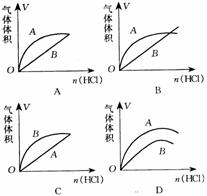 进行如下实验,在A锥形瓶中放入10g块状CaCO3,在B锥形瓶中放入5g粉末状CaCO3,分别加入50mL2mol/L盐酸。右图中能正确表示实验结果的是( )
进行如下实验,在A锥形瓶中放入10g块状CaCO3,在B锥形瓶中放入5g粉末状CaCO3,分别加入50mL2mol/L盐酸。右图中能正确表示实验结果的是( )
6.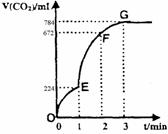 用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积)。下列分析正确的是( )
用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积)。下列分析正确的是( )
A.OE段表示的平均速率最快
B.EF段,用盐酸表示该反应的平均反应速率为0.4mol/(L·min)
C.OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2:6:7
D.G点表示收集的CO2的量最多
5.煅烧硫铁矿产生SO2,为了提高SO2的生成速率,下列措施可行的是( )
A.把硫铁矿石碾成粉末
B.增大O2的压强,向炉内喷吹氧气
C.使用Fe2O3作催化剂
D.降低温度
4.0.1mol/L硫代硫酸钠溶液和0.1mol/L硫酸溶液各10mL和5mL水混合,反应速率为ν1mol/(L•s);0.2mol/L硫代硫酸钠溶液和0.2 mol/L硫酸溶液各5mL与20mL水混合,反应速率为ν2mol/(L•s);则ν1和ν2的关系是( )
A.大于 B.小于 C.等于 D.不能肯定
3.增大压强对下列反应的速率无影响的是( )
A.CO2(g)+Ca(OH)2=CaCO3↓+H2O
B.H2+I2(g) 2HI
2HI
C.NaCl+AgNO3=AgCl↓+NaNO3
D.N2+3H2
 2NH3
2NH3
2.已知4NH3+5O2=4NO+6H2O,若反应速率分别用ν(NH3)、ν(O2)、ν(H2O)[mol·(L·min)-1]表示,则正确的关系是( )
A.4/5ν(NH3)=ν(O2) B.5/6ν(O2)=ν(H2O)
C.2/3ν(NH3)=ν(H2O) D.4/5ν(O2)=ν(NO)
1.甲、乙两容器都在进行A→B的反应,甲容器每分钟减少了4molA,乙容器内每分钟减少了2molA,则甲容器内的反应速率比乙容器内的反应速率要( )
A.快 B.慢 C.相等 D.无法判断
5.亚硫酸钠和碘酸钾在酸性溶液里反应的化学方程式式是:Na2SO3+KIO3+ H2SO4-Na2SO4+ K2SO4+I2+H2O
(1)其中氧化剂是 ,若反应中有5mol e-转移,则生成的碘是 mol。
该反应过程和机理较复杂,一般认为分以下几步:
①IO3-+ SO32-→IO2-+ SO42-(慢)
②IO2-+2SO32-→I-+2SO42-(快)
③5I-+6H++IO3-→3I2+3H2O(快)
④I2+SO32-+H2O→2I-+SO42-+2H+(快)
(2)根据上述条件推测,此反应总的反应速率由
步反应决定。
(3)若预先加入淀粉溶液,由题述看必在 离子消耗完时,才会有使淀粉变蓝的现象产生。
检测提高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com