
3ЃЎЫцзХТБЫидзгАыОЖЕФдіДѓЃЌЯТСаБфЛЏЙцТЩе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁЁЁ )
AЃЎЕЅжЪЕФШлЗаЕуж№НЅНЕЕЭ
BЃЎТБЫиРызгЕФЛЙдадж№НЅдіЧП
CЃЎЦјЬЌЧтЛЏЮяЮШЖЈадж№НЅдіЧП
DЃЎЕЅжЪбѕЛЏадж№НЅдіЧП
(БОЬтПМВщСЫТБзхдЊЫиЕФаджЪЕнБфЙцТЩЃЌвЊИљОндЊЫижмЦкТЩВЂНсКЯТБзхдЊЫиЕФЬиЕуРэНтЁЂЪьМЧЃЁ)
2ЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁЁЁ )
AЃЎЦЏАзЗлЕФгааЇГЩЗжЪЧТШЫсФЦ
BЃЎЗњЛЏЧтдкПеЦјжаГЪЯжАзЮэЃЌетжжАзЮэгаОчЖО
CЃЎЕтЛЏМиШмвКФмЪЙЕэЗлБфРЖ
DЃЎЗњЦјЭЈШыЫЎжагабѕЦјЩњГЩ
ЁЁЁЁ (БОЬтПМВщСЫЯрЙиЮяжЪЕФВПЗжаджЪЃЌЪьСЗеЦЮнетаЉЮяжЪЕФаджЪЪЧНтЬтЕФЛљДЁЁЃ)
1ЃЎэСЪЧЕкСљжмЦкЂїAзхдЊЫиЃЌЭЦВтЯТСаЕЅжЪЛђЛЏКЯЮяЕФаджЪжагаУїЯдДэЮѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁЁЁ )
AЃЎэСЕЅжЪЮЊКкЩЋЕФЙЬЬх
BЃЎэСЕФЧтЛЏЮяВЛЮШЖЈ
CЃЎэСЕЅжЪВЛвзШмгкЫЎ
DЃЎэСЕФзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяЮЊЧПЫс
(БОЬтПМВщСЫэСМАЦфЛЏКЯЮяЕФаджЪЃЌгЩТБзхдЊЫиЕФгаЙиаджЪЧЈвЦПЩЕУГіНсТлЁЃ)
4ЃЎ(2001ФъЩЯКЃИпПМЬт)ЮЊСЫдЄЗРЕтШБЗІВЁЃЌЙњМвЙцЖЈУПЧЇПЫЪГбЮжагІКЌга40-50КСПЫЕФЕтЫсМиЁЃЮЊМьбщФГжжЪГбЮЪЧЗёЮЊМгЕтЕФКЯИёЪГбЮЃЌФГЭЌбЇШЁЪГбЮбљЦЗ428ПЫЃЌЩшЗЈШмНтГіЦфжаШЋВПЕФЕтЫсМиЁЃНЋШмвКЫсЛЏВЂМгШызуСПЕФЕтЛЏМиЕэЗлШмвКЃЌШмвКГЪРЖЩЋЃЌдйгУ0.030mol/LЕФСђДњСђЫсФЦШмвКЕЮЖЈЃЌгУШЅ18.00mLЪБРЖЩЋИеКУЭЪШЅЁЃЪдЭЈЙ§МЦЫуЫЕУїИУМгЕтЪГбЮЪЧЗёЮЊКЯИёВњЦЗЁЃгаЙиЗДгІШчЯТЃК
IO3Ѓ+5IЃ+6 H+Ёњ3I2+3H2O
I2+2S2O32ЃЁњ2IЃ+S4O62Ѓ
ЁЁ (БОЬтПМВщЛЏбЇМЦЫуЕФФмСІЃЌЯШевГіЙиЯЕЪНЃЌдйСаБШР§НтЬтЃЌПЩДѓДѓМђЛЏМЦЫуЙ§ГЬЁЃ)
аТЛюЬтЭјеО
3ЃЎ(1996ФъЩЯКЃИпПМЬт)(1)1986Фъ,ЛЏбЇЩЯЕквЛДЮгУЗЧЕчНтЗЈжЦЕУЗњЦј,ЪдХфЦНИУЗДгІЕФЛЏбЇЗНГЬЪНЃК
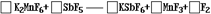 ЁЁ
ЁЁ
ЗДгІжаЁЁЁЁЁЁЁЁ дЊЫиБЛЛЙдЁЃ
(2)Чш(CN)2ЁЂСђЧш(SCN)2ЕФЛЏбЇаджЪКЭТБЫи(X2)КмЯрЫЦ,ЛЏбЇЩЯГЦЮЊФтТБЫи
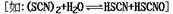 ЃЌЫќУЧвѕРызгЕФЛЙд
ЃЌЫќУЧвѕРызгЕФЛЙд
адЧПШѕЮЊЃКCl-<Br-<CN-<SCN-<I-ЁЃЪдаДГіЃК
Ђй(CN)2гыKOHШмвКЗДгІЕФЛЏбЇЗНГЬЪНЃК
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЃЛ
ЂкNaBrКЭKSCNЕФЛьКЯШмвКжаМгШы(CN)2ЗДгІЕФРызгЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
(БОЬтПМВщСЫбѕЛЏЛЙдЗДгІЕФХфЦНЁЂЙцТЩвдМАжЊЪЖЧЈвЦКЭгІгУаХЯЂЕФФмСІЁЃгУЛЏКЯМлЩ§НЕЗЈХфЦНВЂНсКЯТШЦјЕФвЛаЉЗДгІНјааЧЈвЦЁЃ)
2ЃЎ(2002ФъШЋЙњИпПМЬт)ЕтИњбѕПЩвдаЮГЩЖржжЛЏКЯЮяЃЌЦфжавЛжжГЦЮЊЕтЫсЕтЃЌдкИУЛЏКЯЮяжаЃЌЕтдЊЫиГЪ+3КЭ+5СНжжМлЬЌЃЌетжжЛЏКЯЮяЕФЛЏбЇЪНЪЧ
AЃЎ I2O3ЁЁ ЁЁЁЁЁЁBЃЎ12O4ЁЁ
CЃЎ I4O7ЁЁ ЁЁЁЁЁЁDЃЎI4O9
(БОЬтПМВщЮяжЪЛЏбЇЪНЕФЪщаДФмСІЃЌЗТеебЮЕФЛЏбЇЪНВЂУїШЗСНДІЕтЕФЛЏКЯМлДгЖјЕУГіНсТлЁЃ)
5ЃЎЮЊЗРжЙЕтШБЗІВЁЃЌГЃдкЪГбЮжаМгШывЛЖЈСПЕФЕтЫсМиЁЃ
ЕфаЭЬтЕуЛї
4ЃЎТБЛЏвјЕФаджЪМАТБЫиРызгЕФМьбщ
AgFАзЩЋвзШмгкЫЎЃЌAgClЁЂAgBrЁЂAgIбеЩЋгЩАзЩЋЕНЕЛЦЩЋЕНЛЦЩЋЃЌОљВЛШмгкЫЎЧвШмНтЖШдНРДдНаЁЃЌТБЛЏвјОпгаИаЙтадЁЃРћгУТБЛЏвјЕФаджЪПЩвдгУЫсЛЏЕФAgNO3(aq)РДМьбщТБЫиРызг(Cl-ЁЂBr-ЁЂI-)ЁЃДЫЭтЃЌвВПЩвддкКЌгаТБЫиРызгЕФШмвКжаЕЮШыТШЫЎЃЌдйМгШыгаЛњШмМСеёЕДКѓЃЌЙлВьгаЛњВубеЩЋЁЃ
3ЃЎТБЫиЕЅжЪЕФЛЏбЇаджЪ
гыТШЦјРрЫЦЃЌАДF2ЁЂCl2ЁЂBr2ЁЂI2ЕФЫГађбѕЛЏадж№НЅМѕШѕЁЃ(1)гыН№ЪєЗДгІЃЌгыОјДѓЖрЪ§Н№Ъє(дкЕуШМЛђзЦЩеЕФЬѕМўЯТ)жБНгЗДгІЃЌЩњГЩИпМлТБЛЏЮя(I2Г§ЭтЃЌШчгыЬњЗДгІЩњГЩбЧЬњбЮ)ЁЃ(2)гыH2ЗДгІЃЌЕнБфЙцТЩШчЯТЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
F2ЁЁ Cl2ЁЁЁЁЁЁЁЁЁЁ Br2ЁЁЁЁ I2
ЬѕЁЁЁЁЁЁ МўЁЁ АЕДІЁњЙтее(ІЄ)Ёњ МгШШЁњБпМгШШБпЗжНт
ЯжЁЁЁЁЁЁ ЯѓЁЁ БЌеЈЁњБЌеЈ(ЛђШМЩе)ЯжЁЁ ЯѓЁЁ ВЛЁЁ УїЁЁ Яд
 ВњЮяЮШЖЈадЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
МѕШѕ
ВњЮяЮШЖЈадЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
МѕШѕ
 ВњЮяЫсадЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁдіЧП
ВњЮяЫсадЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁдіЧП
 ВњЮяЛЙдадЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
діЧП
ВњЮяЛЙдадЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
діЧП
(3)гыЫЎЗДгІЃЌF2гыЫЎОчСвЗДгІЙЪЖјЮоЁАЗњЫЎЁБЃЌBr2ЁЂI2гыЫЎзїгУдНРДдНЮЂШѕЁЃ(4)ТБЫиЕЅжЪМфЕФжУЛЛЗДгІЃЌАДCl2ЁЂBr2ЁЂI2ЕФЫГађЃЌЧАУцЕФЕЅжЪФмДгбЮШмвКжажУЛЛГіКѓУцЕФЕЅжЪЃЌF2гібЮШмвКЯШКЭЫЎЗДгІЁЃ(5)гыЕЭМлЬЌЮяжЪЗДгІЃЌШчSO2ЁЂNa2SO3ЕШЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com