
4.密度为0.91 g·cm-3的氨水,质量百分比浓度为25%(即质量分数为0.25),该氨水用等体积的水稀释后,所得溶液的质量百分比浓度 ( )
A.等于12.5% B.大于12.5%
C.小于12.5% D.无法确定
此题考查氨水稀释的质量分数的计算及计算技巧。)
3.试管中盛有白色晶体,检验它是否是铵盐的方法中不可行的是 ( )
A.加热,将湿润的红色石蕊试纸放在管口
B.加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口
C.加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在试管口
D.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在管口
(此题考查铵盐的检验方法,要求能设计实验进行铵盐的检验。)
2.以下哪个性质不是所有铵盐的通性 ( ) [ ]
A.都易溶于水 B.都可分解放出氨气
C.都能与碱反应且均放出氨气
D.都是离子化合物能形成离子晶体
(此题考查铵盐的结构及性质,要求能熟记。)
1.以下实验室制取氨气的试剂组合中,最合适的是( )
A.固体氯化铵和消石灰 B.氯化铵溶液和石灰水
C.硝酸铵和碱石灰 D.稀氨水和碱石灰
(此题考查氨气的实验室制法原理。)
2.铵盐 由铵离子和酸根离子构成的化合物叫做铵盐。铵盐都是晶体,并且都能溶于水。
铵盐的化学性质
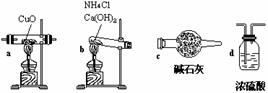 (1) 铵盐受热分解 氯化铵受热时分解,生成氨气和氯化氢,冷却时氨气和氯化氢又重新结合,生成氯化铵。氯化铵有假升华现象。碳酸氢铵受热时也会分解,生成氨气、水和二氧化碳。水的状态由受热温度决定。但不是所有的铵盐受热分解都产生氨气,其它铵盐分解不作要求。
(1) 铵盐受热分解 氯化铵受热时分解,生成氨气和氯化氢,冷却时氨气和氯化氢又重新结合,生成氯化铵。氯化铵有假升华现象。碳酸氢铵受热时也会分解,生成氨气、水和二氧化碳。水的状态由受热温度决定。但不是所有的铵盐受热分解都产生氨气,其它铵盐分解不作要求。
(2) 铵盐与碱的反应 铵盐与碱共热都能产生氨气,这是铵盐的共同性质。常用此性质检验铵盐的存在,即取样品加氢氧化钠,产生的气体能使湿润的红色石蕊试纸变蓝色,说明样品含铵盐。
典型题点击
1.氨 氮气和氢气在一定条件下反应生成氨。在自然界中,氨是动物体特别是蛋白质腐败后的产物。
(1)氨的物理性质 氨是无色、有刺激性气味的气体,在标准状况下,密度是0.771g/L,比空气的小,易液化。液氨汽化时要吸收大量的热,使周围的温度急剧下降,所以液氨常做致冷剂。
(2) 氨的化学性质 氨分子呈三角锥形,是极性分子。氨分子中的氮原子有一对孤对电子。
氨气与水反应 氨气极易溶于水,通常情况下,1体积水能溶解700体积氨。氨的水溶液叫氨水。氨溶于水时,大部分氨分子和水分子形成一水合氨分子(NH3·H2O)。一水合氨分子(NH3·H2O)可以部分电离成铵根离子(NH4+)和氢氧根离子(OH-),所以氨水显碱性,使酚酞变红色。一水合氨分子(NH3·H2O)不稳定,受热时分解为氨气和水。
①氨气与氯化氢的反应 蘸浓氨水和蘸浓盐酸接近(不接触)时,产生大量白烟。氨气与氯化氢反应生成氯化铵。
②氨与氧气的反应 氨气在催化剂(如铂等)、加热的条件下,生成一氧化氮和水,并放出热量。此反应是放热反应,是工业制硝酸的基础。
 (3)氨的实验室制法 实验室里用铵盐和碱在加热条件下反应制氨气。常用熟石灰和氯化铵在加热条件下反应制氨。该反应符合强碱制弱碱的原理。属于固体加热制气体的反应,用实验室制氧气的装置。由于氨水受热分解可产生氨气,在实验室有时也用加热浓氨水的方法制氨气。
(3)氨的实验室制法 实验室里用铵盐和碱在加热条件下反应制氨气。常用熟石灰和氯化铵在加热条件下反应制氨。该反应符合强碱制弱碱的原理。属于固体加热制气体的反应,用实验室制氧气的装置。由于氨水受热分解可产生氨气,在实验室有时也用加热浓氨水的方法制氨气。
17. 8.43%
16.A:NO,B:O2。
A= 20mL。 20mL< V <60Ml
15.(1)NH3、CO2、NO,N2、NO2,
(2)2Na2O2+ 2CO2= 2Na2CO3 + O2, 2NO+O2=2N02
(3)CO2 ,NO 。3:2。
14.(1)1,2,2,1,2,4。
(2)硬度大,熔沸点高,不导电。
(3)B与N之间以共价键相结合,形成平面网状结构,层与层之间以分子间作用力相接合。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com